Clear Sky Science · de
In-vitro-Modellierung von Veränderungen der extrazellulären Matrix bei Hautalterung: von statischem 2D zu 3D-dynamischen mikrophysiologischen Systemen
Warum es wichtig ist, Hautalterung im Reagenzglas zu untersuchen
Falten, Erschlaffung und Altersflecken sind mehr als kosmetische Makel – sie spiegeln tiefgreifende Veränderungen in der Architektur unserer Haut wider. Da Tierversuche zunehmend eingeschränkt sind, arbeiten Forschende intensiv daran, menschenähnliche Hautmodelle im Labor zu entwickeln, um zu verstehen, wie und warum Haut altert und um sicherere, wirksamere Anti-Aging-Behandlungen zu testen. Dieser Artikel erklärt, wie Wissenschaftlerinnen und Wissenschaftler von flachen Zellschichten zu komplexen 3D‑„Mini‑Häuten auf Chips“ übergehen, die das echte Altern nachahmen, und liefert einen Ausblick auf die Zukunft von Hautpflege, Medizin und Sicherheitsprüfungen.
Das verborgene Gerüst unter unseren Falten
Das jugendliche Aussehen und die Widerstandsfähigkeit der Haut beruhen auf der extrazellulären Matrix, einem mikroskopischen Gerüst aus Proteinen und Zuckerbausteinen, das Zellen stützt und die äußere Epidermis mit der tieferen Dermis verbindet. Mit zunehmendem Alter und durch Sonneneinwirkung wird dieses Gerüst ständig umgebaut: Kollagen- und Elastinfasern brechen ab, zuckervermittelte Quervernetzungen machen das Gewebe steifer, und die Verbindung zwischen oberer und unterer Schicht flacht ab. Diese Veränderungen verdünnen die Epidermis, verringern die Elastizität und begünstigen Falten und Erschlaffung. Umweltstressoren wie UV‑Licht, Schadstoffe und Zigarettenrauch verschärfen die Schäden und erzeugen eine chronische niedriggradige Entzündungsreaktion – oft als „Inflammaging“ bezeichnet. Da dieser Umbau dynamisch und nicht statisch ist, muss ein überzeugendes Labormodell der alternden Haut nicht nur zeigen, welche Moleküle vorhanden sind, sondern auch, wie sie sich im Laufe der Zeit verändern und auf Stress reagieren.
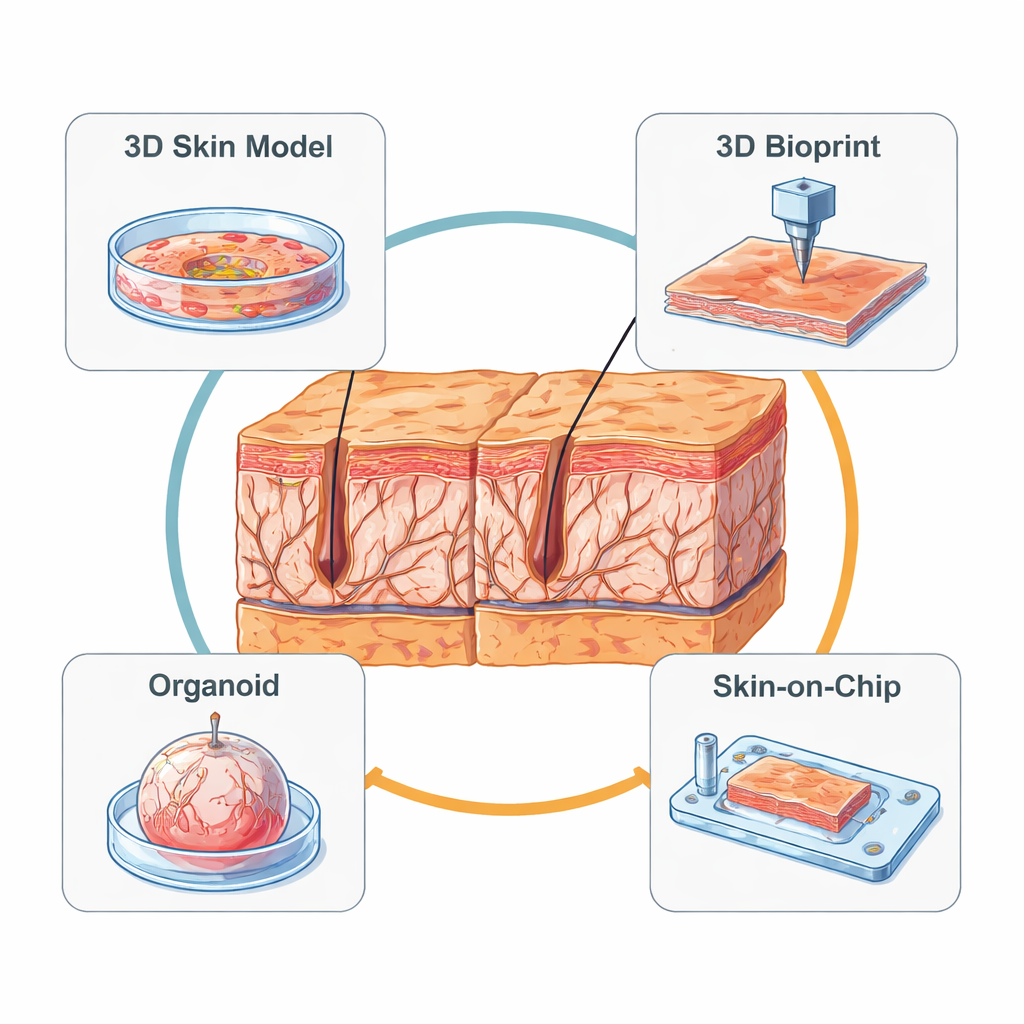
Von flachen Zellschichten zu 3D‑Mini‑Haut
Frühe Labormodelle basierten auf einfachen zweidimensionalen Schichten von Hautzellen. Diese flachen Kulturen sind leicht zu handhaben und nützlich, um einzelne Marker wie Kollagen, Elastin oder Matrix‑abbauende Enzyme zu messen. Sie erfassen jedoch nicht die geschichtete Struktur der echten Haut und können nicht reproduzieren, wie Zellen ein 3D‑Gerüst wahrnehmen und daran ziehen. Um der Realität näher zu kommen, entwickelten Forschende rekonstruierte menschliche Haut: ein 3D‑Hydrogel mit Fibroblasten (den wichtigsten Matrix-produzierenden Zellen), das mit einer geschichteten Epidermis an einer Luft‑Flüssigkeits‑Grenzfläche überzogen ist. Diese Modelle können bräunen, eine Barriere ausbilden und altersähnliche Merkmale zeigen, wenn Forscher „alte“ Fibroblasten einbringen, UV‑Bestrahlung anwenden oder die Matrix chemisch versteifen. Dennoch fehlen Blutgefäße, Immunzellen und realistische mechanische Kräfte, und sie sind schwer über lange Zeiträume zu erhalten, um langsame Alterungsprozesse zu verfolgen.
Drucken, Wachsen und Selbstorganisieren von Mini‑Häuten
Neuere Ansätze verbinden ingenieurtechnische Präzision mit Biologie. Dreidimensionales Bioprinten verwendet Düsen oder lichtbasierte Drucker, um Zellen und weiche „Bioinks“ schichtweise in definierten Mustern zu platzieren. Damit können Forschende künstliche Haut mit kontrollierter Oberflächentextur gestalten, einschließlich in‑vitro‑Falten, deren Tiefe und Abstand justiert und gemessen werden können. Biogedruckte Modelle können zudem frühe Gefäßstrukturen und Immunzellen enthalten, wodurch sie leistungsfähige Testsysteme für Anti‑Aging‑Produkte und Wundtherapien werden, obwohl Drucker und Materialien weiterhin teuer und technisch anspruchsvoll sind. Parallel dazu starten Organoid‑Technologien mit Stammzellen, die sich selbst zu winzigen, kugeligen, hautähnlichen Strukturen organisieren. Bemerkenswerterweise können diese Mini‑Organe Haarfollikel und andere Anhangsgebilde ausbilden und zeigen realistische Reaktionen auf sonnenähnliche UV‑Bestrahlung, darunter Kollagenverlust, Entzündungen und sogar Ausdünnung der Haarstämme – Effekte, die in früheren Modellen schwer zu beobachten waren.
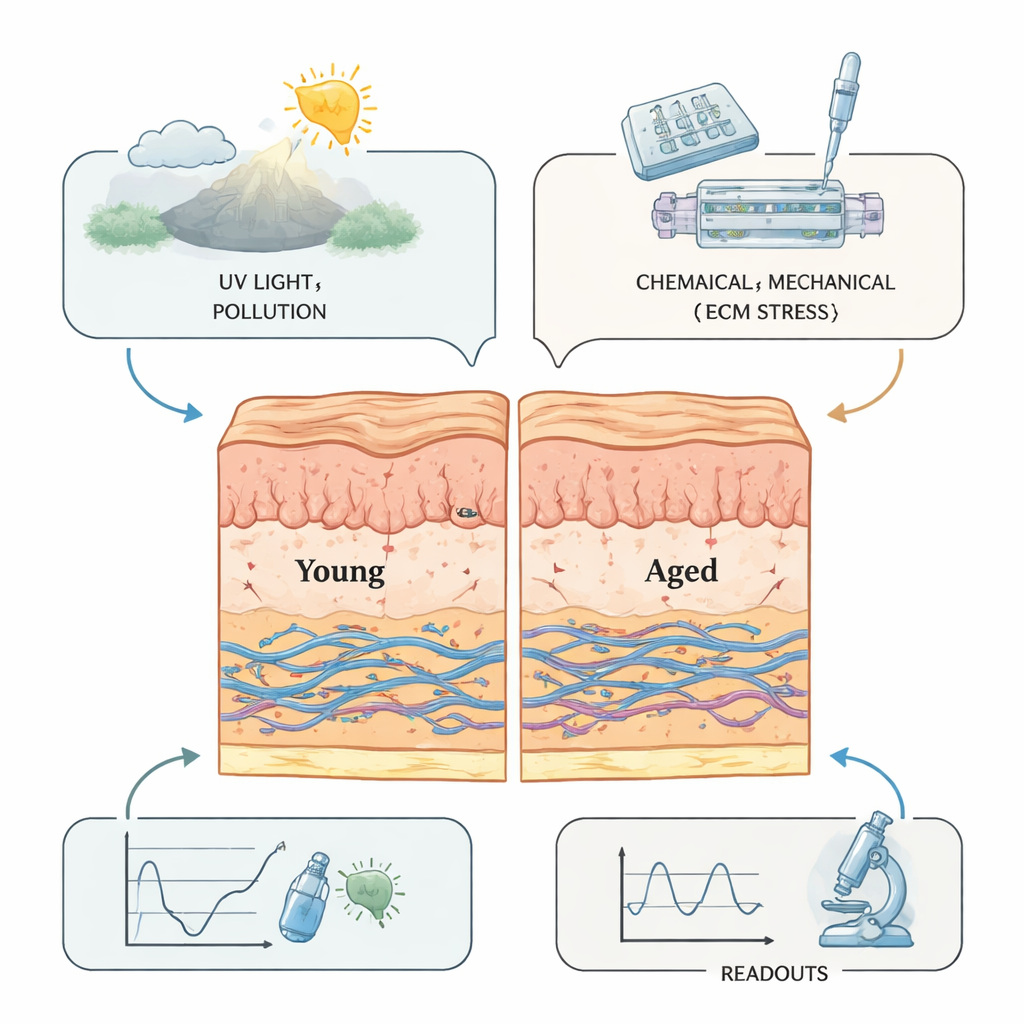
Skin‑on‑a‑Chip: Bewegung und Fluss in die Alterung bringen
Vielleicht sind die futuristischsten Systeme die „Skin‑on‑a‑Chip“‑Geräte, die Hautgewebe in eine transparente mikrofluidische Kartusche einbetten. Winzige Kanäle bringen Nährstoffe und führen Abfallstoffe ab, während integrierte Mechanismen das Gewebe sanft dehnen oder komprimieren, um Mimik oder Tag‑Nacht‑Druckzyklen nachzuahmen. Durch präzise Anpassung der Stärke und Häufigkeit dieser Kräfte können Forschende Hautmodelle dazu bringen, tiefere Falten, erhöhte Entzündungssignale und reduziertes Kollagen zu entwickeln – ganz ähnlich dem realen Altern. Diese Chips können auch miniaturisierte Blutgefäße und Immunzellen beherbergen, sodass untersucht werden kann, wie zirkulierende Zellen in die Haut eindringen und die Alterung beeinflussen. Nationale und internationale Standards entstehen bereits, um zu harmonisieren, wie diese Geräte gebaut und getestet werden, und ebnen den Weg für eine breitere Nutzung in Industrie und Regulierung.
Was das für künftige Anti‑Aging‑Lösungen bedeutet
In der Summe deuten diese Fortschritte auf Hautmodelle der nächsten Generation hin, die 3D‑Struktur, kontrollierte Mechanik, lebende Mikrovaskulaturen, Immunzellen und sogar die normalerweise auf unserer Haut lebenden Mikroben kombinieren. Solche Systeme lassen sich so einstellen, dass sie eine „junge“ oder „alte“ Mikroumgebung repräsentieren und verwendet werden können, um zu verfolgen, wie das Hautgerüst sich im Laufe der Zeit unter realistischen Sonnen‑, Schadstoff‑ oder Kosmetikeinflüssen erweicht, verhärtet oder fragmentiert. Für Verbraucherinnen und Verbraucher bedeutet das, dass künftige Anti‑Aging‑Cremes und Behandlungen wahrscheinlicher in humanrelevanten, tierversuchsfreien Systemen getestet werden, die die echte Biologie alternder Haut erfassen — was sowohl die Sicherheit verbessert als auch die Wahrscheinlichkeit erhöht, dass versprochene Wirkungen im echten Leben eintreten.
Zitation: Yao, Y., Zhang, Z., Zhang, J. et al. In vitro modelling of extracellular matrix changes during skin aging: from static 2D to 3D dynamic microphysiological systems. Microsyst Nanoeng 12, 70 (2026). https://doi.org/10.1038/s41378-026-01170-y
Schlüsselwörter: Hautalterung, extrazelluläre Matrix, 3D-Hautmodelle, Organoide, Skin-on-a-Chip