Clear Sky Science · ar
توجيه تفريغ الكلية عبر الجلد بواسطة منظار التصوير المقطعي البصري القائم على الشبكات العصبية الالتفافية
لماذا يهم الوصول الآمن إلى الكلية
أصبحت أمراض حصى الكلى أكثر شيوعًا، ويحتاج كثير من المرضى لأنبوب صغير يوضع مباشرة في الكلية لتصريف البول أو إزالة الحصى. تُجرى هذه العملية، المسماة تفريغ الكلية عبر الجلد (percutaneous nephrostomy)، عن طريق توجيه إبرة من ظهر المريض إلى المركز المفرغ للكلية. على الرغم من صغر الثقب، فإن اختيار مسار خاطئ قد يمزق تركيبات الكلية الدقيقة أو يضر بالأوعية الدموية، مما يؤدي إلى نزف ومضاعفات أخرى. تقدم هذه الدراسة مسبار تصويري جديدًا عالي الدقة، مقرونًا بالذكاء الاصطناعي، يركب داخل طرف الإبرة لمساعدة الأطباء على رؤية وجهتهم بدقة وتجنب الأذى.
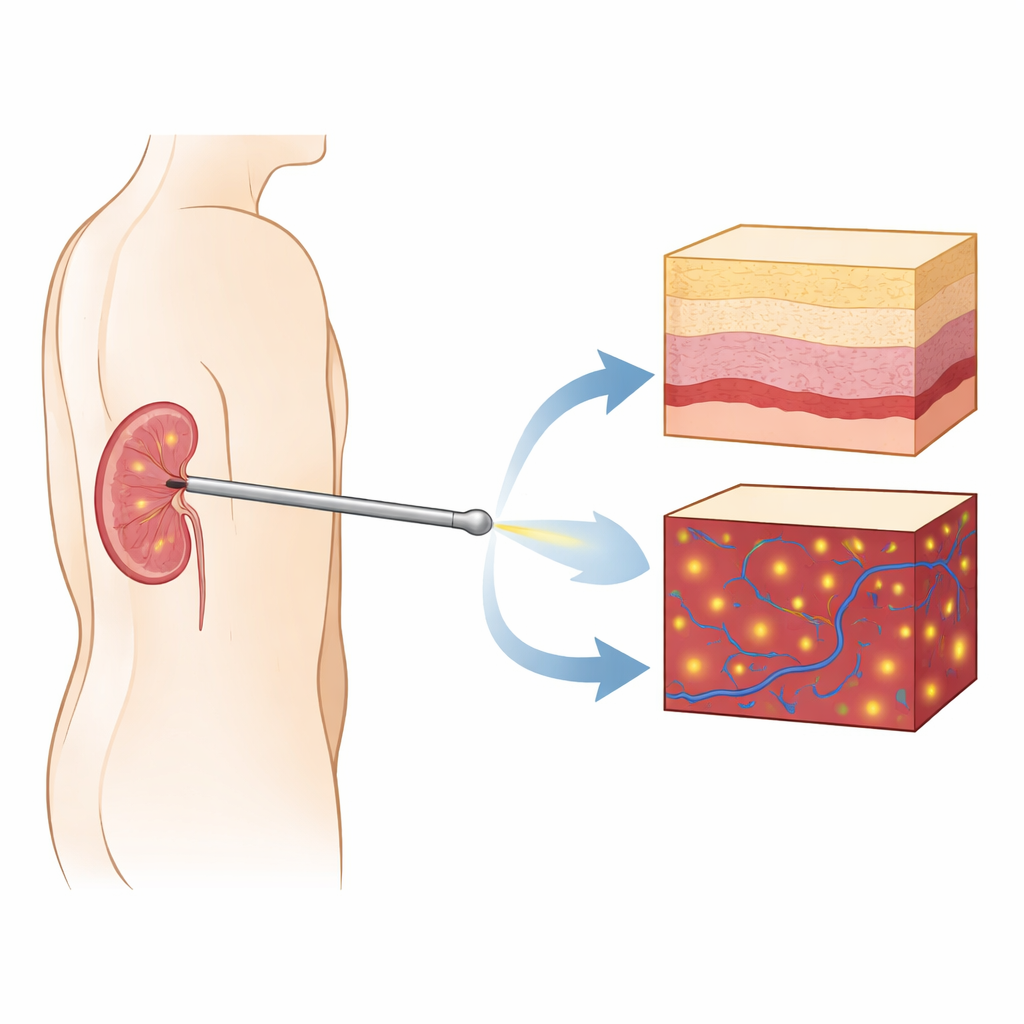
كاميرا صغيرة داخل الإبرة
بنى الباحثون مسبارًا تصويريًا متجهًا إلى الأمام قائمًا على التصوير المقطعي البصري (OCT)، وهي طريقة ضوئية تلتقط «شرائح» مقطعية من الأنسجة بدقة ميكرومترية—أي أعلى بحوالي عشرة أضعاف من دقة الموجات فوق الصوتية الطبية التقليدية. ضمنوا عدسة رقيقة ذات معامل تدرجي داخل إبرة تفريغ كلية قياسية بحيث يمكن للمسبار أثناء الإدخال أن ينظر مباشرة أمامه إلى داخل الكلية. على خلاف المناظير العادية التي تعرض غالبًا مناظر سطحية، يوفر هذا النظام صورًا مفصولة بحسب العمق، كاشفًا كيف تتغير بنية النسيج تحت الطرف. يمكن لنفس المسبار أن يعمل أيضًا في وضع دوبلر، الذي يبرز خلايا الدم الحمراء المتحركة وبذلك يكشف عن الأوعية الدموية أمام الإبرة قبل ثقبها.
تمييز طبقات الكلية في الوقت الحقيقي
لاختبار ما إذا كان النظام قادرًا على التفريق بين أنسجة الكلية المختلفة، أجرى الفريق تجارب على 31 كلية بشرية متبرع بها وحفظت في ظروف تقريبًا طبيعية. في الإجراءات الحقيقية، يجب أن تمر الإبرة عبر القشرة الخارجية والنخاع الداخلي، ثم تدخل منطقة شبيهة بالكأس تُسمى الكأسية (calyx) وتخرج أخيرًا إلى الحوض المركزي المcollect للبول. الخروج عن المسار يعرض الإبرة للعبور عبر فراغات دهنية بين البنى وتمزق الجدران الرقيقة. لامس الباحثون بصورة منهجية المسبار بخمسة أنواع من الأنسجة—القشرة، النخاع، الكأسية، دهن الجيب (sinus fat)، والحوض—وسجلوا ملايين من صور OCT تُظهر أنماطها المميزة. على سبيل المثال، بدت القشرة والنخاع ناعمتين لكنهما اختلفتا في العمق، أظهرت الكأسية انتقالات مُخططة، أنتج دهن الجيب شبكات متناثرة براقة، وظهر الحوض كمساحة فارغة تحت المسبار.
تدريس نظام ذكي لرصد الخطر
بما أن الخبراء البشريين سيحتاجون وقتًا وتدريبًا لتفسير هذه الصور الجديدة أثناء العملية، لجأ الفريق إلى التعلم العميق. دربوا عدة شبكات عصبية التفافية لتصنيف كل إطار OCT إلى واحد من الأنواع الخمسة للأنسجة، ثم اختاروا بنية تُدعى Inception كأفضل أداء. في اختبارات داخلية، تعرف هذا النموذج على الأنسجة بدقة تقارب 99.6%، وحافظ على أداء عالٍ على كلوى إضافية لم يسبق له رؤيتها. في مهمة منفصلة، استخدموا تصميمًا شبكيًا آخر، nnU‑Net، لتحديد محيط الأوعية الدموية في صور دوبلر OCT. تعلم هذا النموذج تمييز الدم المتدفق عن نسيج الخلفية بمطابقة عالية لملصقات الخبراء المرسومة يدويًا، حتى للأوعية الأصغر من 0.2 ملم التي يصعب رؤيتها بالأدوات القياسية.
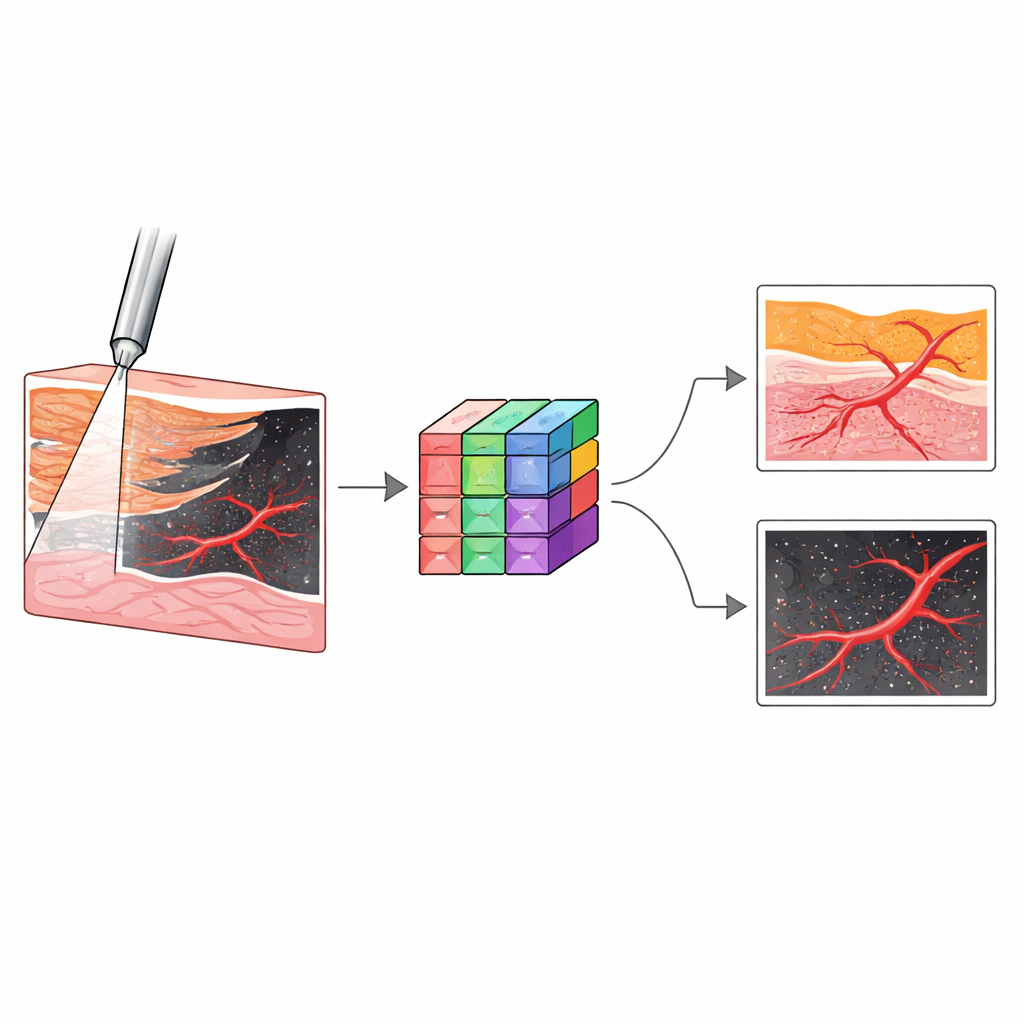
كيف يقارن مع أدوات اليوم
عادةً ما يعتمد الأطباء حاليًا على التصوير بالموجات فوق الصوتية أو الفلوروسكوبي القائم على الأشعة السينية لتوجيه إبر التفريغ. تعرض هذه التقنيات الموضع العام للكلية والمسار العام للإبرة، لكن دقتها النسبية الخشنة تجعل من الصعب معرفة أي نسيج يقع عند الطرف بدقة، أو مدى قرب وعاء دموي. في تجارب ضابطة، واجه أطباء الأشعة ذوو الخبرة صعوبة في تحديد النسيج الدقيق عند طرف الإبرة باستخدام الموجات فوق الصوتية الهيكلية ودوبلر، ولم يتمكنوا من تصور الأوعية الدقيقة بشكل موثوق. بالمقابل، قدم نظام OCT رؤية محلية مفصلة بالإضافة إلى تحليل آلي يعمل في جزء بسيط من الثانية على وحدات معالجة الرسوميات الحديثة، ما يتيح تغذية راجعة سريعة أثناء تقدم الإبرة.
ماذا قد يعني هذا للمرضى
تشير الدراسة إلى أن الجمع بين مسبار OCT المثبت داخل الإبرة والتعلم العميق قد يجعل إجراءات الوصول إلى الكلية أكثر أمانًا وكفاءة. في المستقبل، يمكن للطبيب إدخال الإبرة المعتادة مع المسبار بداخلها، مشاهدة صور دقيقة تظهر في الوقت الحقيقي، والاعتماد على البرنامج لإشارة دخول الطرف إلى الحجرة الصحيحة أو اقترابه من وعاء دموي. يقلل قلة محاولات الوخز من رضّ النسيج، وخطر النزف، وربما يقصر زمن الإجراءات ومدة الإقامة بالمستشفى. وعلى الرغم من أن العمل أُجري على كلوى متبرع بها وليس مرضى أحياء، فإنه يمهد الطريق لأنظمة سريرية قد تساعد أيضًا في توجيه تدخلات مُعتمدة على الإبرة الأخرى، من الخزعات وكتل التخدير إلى توصيل الأدوية المستهدفة.
الاستشهاد: Wang, C., Calle, P., Yan, F. et al. Percutaneous nephrostomy guidance by a convolutional-neural-network-based optical coherence tomography endoscope. Commun Eng 5, 47 (2026). https://doi.org/10.1038/s44172-026-00613-8
الكلمات المفتاحية: جراحة حصى الكلى, توجيه الإبرة, التصوير المقطعي البصري, الذكاء الاصطناعي في التصوير الطبي, كشف الأوعية الدموية