Clear Sky Science · ar
معلومات خلوية مفردة حول تغايرية الخلايا العُرفية واضطراب التكيّف في تقييد النمو الجنيني الانتقائي
عندما يتأخر توأم واحد
بالنسبة للأهل المنتظرين توأمين، قد يكون مصدر قلق كبير عندما يتوقف أحد الأطفال عن النمو بمعدل مماثل للآخر، حتى لو كانا يشتركان في نفس الرحم والمشيمة. هذه الحالة، المسماة تقييد نمو الجنين الانتقائي، لا تهدد صحة التوأم الأصغر قبل الولادة فحسب، بل قد تؤثر أيضاً على مساره التطوري بعيد المدى. تستخدم هذه الدراسة تحليلاً خلوياً متقدماً لتفحص داخل المشيمة المشتركة في مثل هذه حالات التوائم، كاشفة كيف أن تغيّرات دقيقة في خلايا مشيمية محددة والاستجابات المناعية يمكن أن تُزِن الفارق بين نمو سليم ونقص خطير.
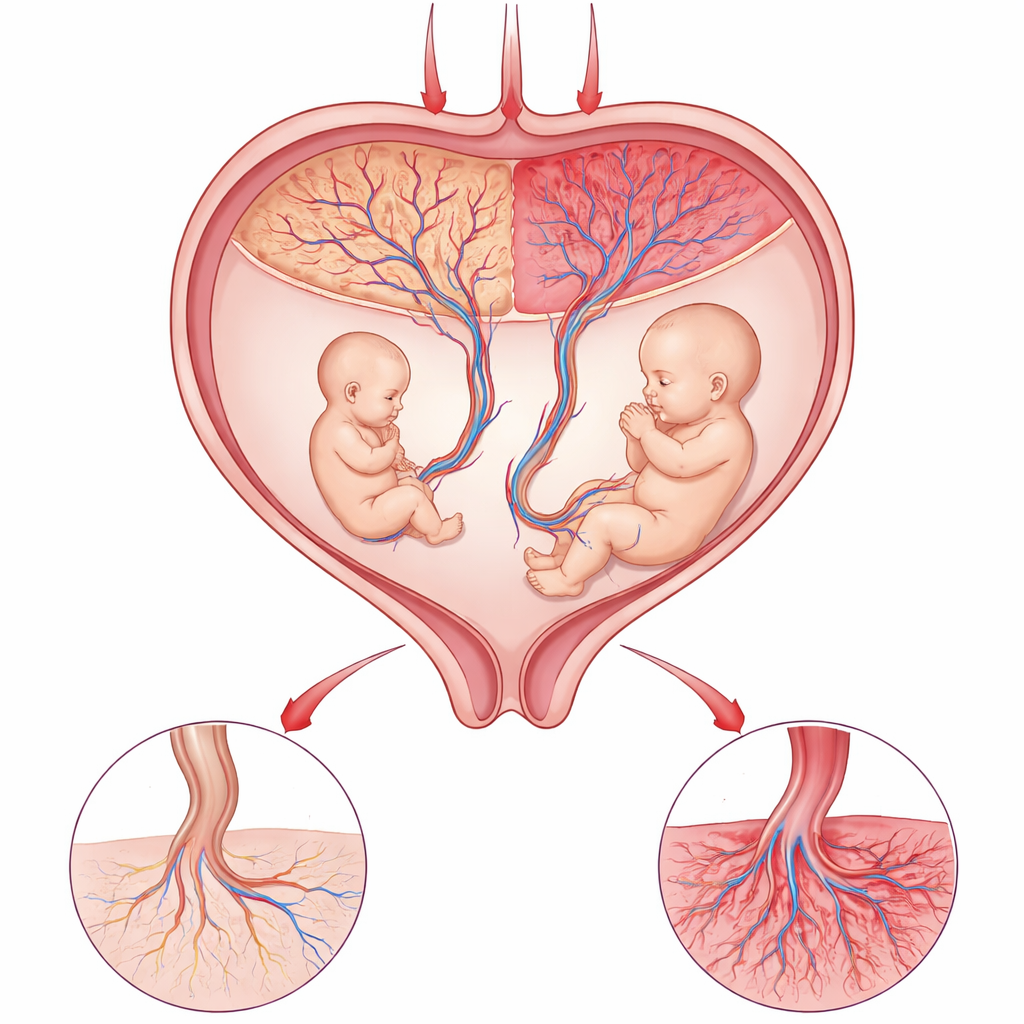
توازن المشيمة الهش
المشيمة هي خط الحياة بين الأم والجنين، تنقل الأكسجين والمواد المغذية وتزيل الفضلات. في بعض حالات توائم متماثلة، يشترك الطفلان في مشيمة واحدة لكن لكل منهما إقليم مختلف داخلها. عندما يصبح أحد التوأمين أصغر بكثير من الآخر، يعرف الأطباء أن هناك خللاً موضعياً في ذلك العضو المشترك. وبما أن التوأمين يتقاسمان الأم ونحو نفس الجينات، فإنهما يشكّلان تجربة طبيعية قوية: أي اختلاف كبير في النمو من المرجح أن ينبع من كيفية عمل أجزاء المشيمة المخصصة لكل جنين، لا من اختلافات بين الأطفال أنفسهم.
التكبير حتى مستوى الخلايا المشيمية الفردية
جمع الباحثون عينات مشيمية من ثلاث حالات حمل كان فيها أحد التوأمين أصغر بكثير من الآخر. باستخدام تسلسل الحمض النووي الريبي لخلايا مفردة—وهي طريقة تقرأ نشاط الآلاف من الجينات في خلايا فردية—سوّوا أكثر من 175,000 خلية من مناطق مشيمية مختلفة. سمح ذلك بفرز الخلايا إلى أنواع متميزة، بما في ذلك خلايا الدعم، وخلايا الأوعية الدموية، وأنواع متعددة من الخلايا المناعية. ركزوا على مجموعة رئيسية اسمها الخلايا العُرفية السَدَفية (villous cytotrophoblasts)، وهي طبقة من الخلايا تبطن النتوءات الصغيرة حيث يلتقي الدم الأمومي مع الدورة الجنينية وتعمل على تجديد وإصلاح سطح المشيمة باستمرار.
حالتان خلويتان رئيسيتان: البناء مقابل وضع البقاء
داخل هذه الخلايا العُرفية السَدَفية، اكتشف الفريق حالتين رئيسيتين تلعبان أدواراً مختلفة للغاية. كانت مجموعة واحدة، تميّزها جزيئة تسمى TP63، تعمل كمشرفين على البنية: دعمت الحاجز بين الأم والجنين، حافظت على الاتصالات بين الخلايا، وساعدت في تنظيم النسيج. أما المجموعة الأخرى، المعلمة بإنزيم يُدعى LDHA، فكانت مهيَّأة لإنتاج طاقة مكثفة ومواجهة الإجهاد، مع تنشيط مسارات مرتبطة بالميتوكوندريا والإجهاد التأكسدي ومراقبة جودة البروتين. في مناطق المشيمة التابعة للتوأم الأصغر، نُقِصَت خلايا TP63 الواقية، بينما توسعت خلايا LDHA المدفوعة بالإجهاد وكانت أكثر نشاطاً في دورة الخلايا. أشارت تحليلات «المسار» الحاسوبية إلى أن الخلايا كانت تدفع صوب مسار من الأدوار البنائية الصحية نحو وضع البقاء، مع قلة الخلايا التي تصل إلى الحالة المندمجة تماماً التي تحافظ عادةً على سطح تبادل أملس وفعال.
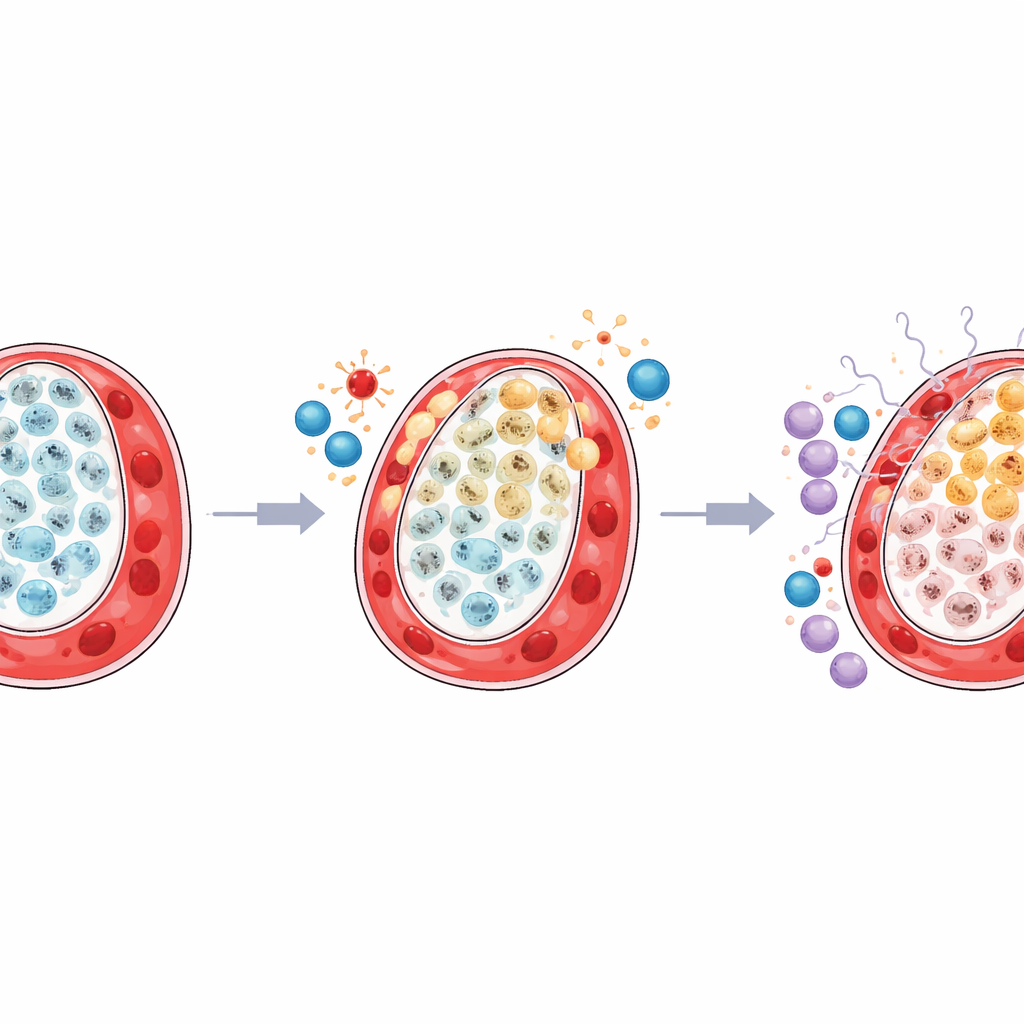
حي مُلتَهِب حول الخلايا المُجهدة
وجدت الدراسة أيضاً أن البيئة المناعية المحيطة في إقليم المشيمة التابع للتوأم الأصغر أعيد تشكيلها بطريقة ضارة. نوع مفيد من البلعميات المقيمة، المعروف بخلايا هوفباورر (Hofbauer cells)، والتي تدعم عادة صحة النسيج وتدير الأيض، كان قد انخفضت أعداده. في الوقت نفسه، ازدادت وفرة بعض الخلايا القاتلة الطبيعية، المهيأة للاستجابات المضادة للفيروسات والالتهابية، وأصبحت أكثر نشاطاً. أظهرت الخرائط التفصيلية للإشارات المتبادلة بين الخلايا أن الخلايا العُرفية من نوع LDHA المُجهدة ارتبطت بقوة أكبر مع الخلايا المناعية عبر مسارات يقودها الإنتيرفيرون وجزيئات إنذار مشابهة. وفي المقابل، ضعفت الاتصالات بين خلايا TP63 البنائية والخلايا النسيجية الداعمة وخلايا الأوعية الدموية، مما يشير إلى فقدان كل من الدعم البنيوي وتنظيم المناعة الهادئ.
انهيار ثلاثي يقيّد نمو الجنين
معاً، ترسم هذه النتائج صورة واضحة ومباشرة لما يختل في المشيمة عندما يتأخر توأم واحد. خلايا الدعم البنيوي التي تحافظ على سطح التبادل مشدوداً ومنظماً تستنفد، تهيمن خلايا مجهدة جائعة للطاقة، وينحرف الجهاز المناعي إلى حالة أكثر التهابية. هذه الخيوط الثلاثة—فقدان البنية، التحميل الأيضي، والالتهاب المزمن—تعزز بعضها البعض وتُضعف تدريجياً قدرة المشيمة على توصيل الأكسجين والمواد المغذية الكافية للجنين الأصغر. من خلال تحديد أنواع الخلايا ومسارات الإشارات المحددة المتورطة، توفر هذه الدراسة خارطة طريق للاختبارات والعلاجات المستقبلية التي تستهدف اكتشاف مشاكل المشيمة مبكراً وربما دفع هذه الخلايا نحو توازن أكثر صحة.
الاستشهاد: Bi, Y., Yang, J., Li, X. et al. Single-cell insights into trophoblast heterogeneity and adaptive dysfunction in selective fetal growth restriction. Commun Biol 9, 387 (2026). https://doi.org/10.1038/s42003-026-09798-2
الكلمات المفتاحية: المشيمة, حمل التوائم, تقييد نمو الجنين, تسلسل الحمض النووي الريبي لخلايا مفردة, خلايا العُرف