Clear Sky Science · ar
البلعميات المناظرة للأور tumor المرتبطة بالورم CD19+ تحفِّز بيئة مجهرية مثبطة للمناعة في سرطان الكبدة الخلوية
لماذا يساعد دفاع الجسم أحيانًا سرطان الكبد
يُعد سرطان الكبد واحدًا من أخطر السرطانات عالميًا، ويرجع ذلك جزئيًا إلى قدرة الأورام على تحويل جهاز المناعة في الجسم ليعمل ضدّه. تكشف هذه الدراسة عن مجموعة مفاجئة من الخلايا المناعية داخل أورام الكبد التي بدلاً من محاربة السرطان، تساعده فعليًا على الاختفاء والنمو. وفهم هوية هذه الخلايا "الخائنة" وكيف تعمل يفتح سبلًا جديدة لجعل العلاج المناعي أكثر فعالية لدى مرضى سرطان الخلايا الكبدية، وهو الشكل الأكثر شيوعًا لسرطان الكبد.
مجموعة خاصة من الخلايا المناعية داخل الأورام
ركز المؤلفون على البلعميات المرتبطة بالورم، وهي خلايا مناعية تبتلع الميكروبات والحطام عادةً لكنها كثيرًا ما تُفسد داخل السرطانات. من خلال تحليل عينات أورام الكبد من العديد من المرضى، اكتشفوا فرعًا مميزًا من البلعميات يحمل جزيئًا سطحيًا يُدعى CD19، الذي يوجد عادةً على خلايا B وليس على البلعميات. كانت هذه البلعميات الموجبة لـ CD19 أكثر وفرة بكثير في أورام الكبد مقارنة بأنسجة الكبد السليمة المجاورة أو الدم، وكانت أيضًا مركزة في عدة سرطانات صلبة أخرى. أكدت تحليلات الخلية المفردة أن هذه الخلايا بلعميات حقيقية ذات ملف جيني وبروتيني فريد، وليست خلايا B تم تعريفها خطأ.
كيف تشكّل هذه الخلايا حيًا ملائمًا للورم
المرضى الذين احتوت أورامهم على عدد كبير من البلعميات الموجبة لـ CD19 كانوا يميلون إلى امتلاك أورام أكبر وأكثر عدوانية ومدة بقاء أقصر. أظهرت عينات الأورام الغنية بهذه الخلايا عددًا أقل من خلايا CD8 القاتلة للسرطان والمزيد من الخلايا التائية المنظمة، وهو نمط نموذجي لبيئة شديدة التثبيط المناعي. في نماذج الفئران، أدى إضافة بلعميات موجبة لـ CD19 إلى خلايا سرطان الكبد إلى تسريع نمو الأورام وتقليل وجود الخلايا التائية المفيدة، مع زيادة خلايا نقيية مُثبطة أخرى. والأهم من ذلك، عندما استخدم الباحثون خلايا تائية مهندسة تتعرف على CD19 لاستهداف هذه البلعميات وإزالتها انتقائيًا، تقلصت أورام الكبد حتى في فئران تفتقر إلى خلايا B الطبيعية، مما يحدد البلعميات نفسها كأهداف علاجية.
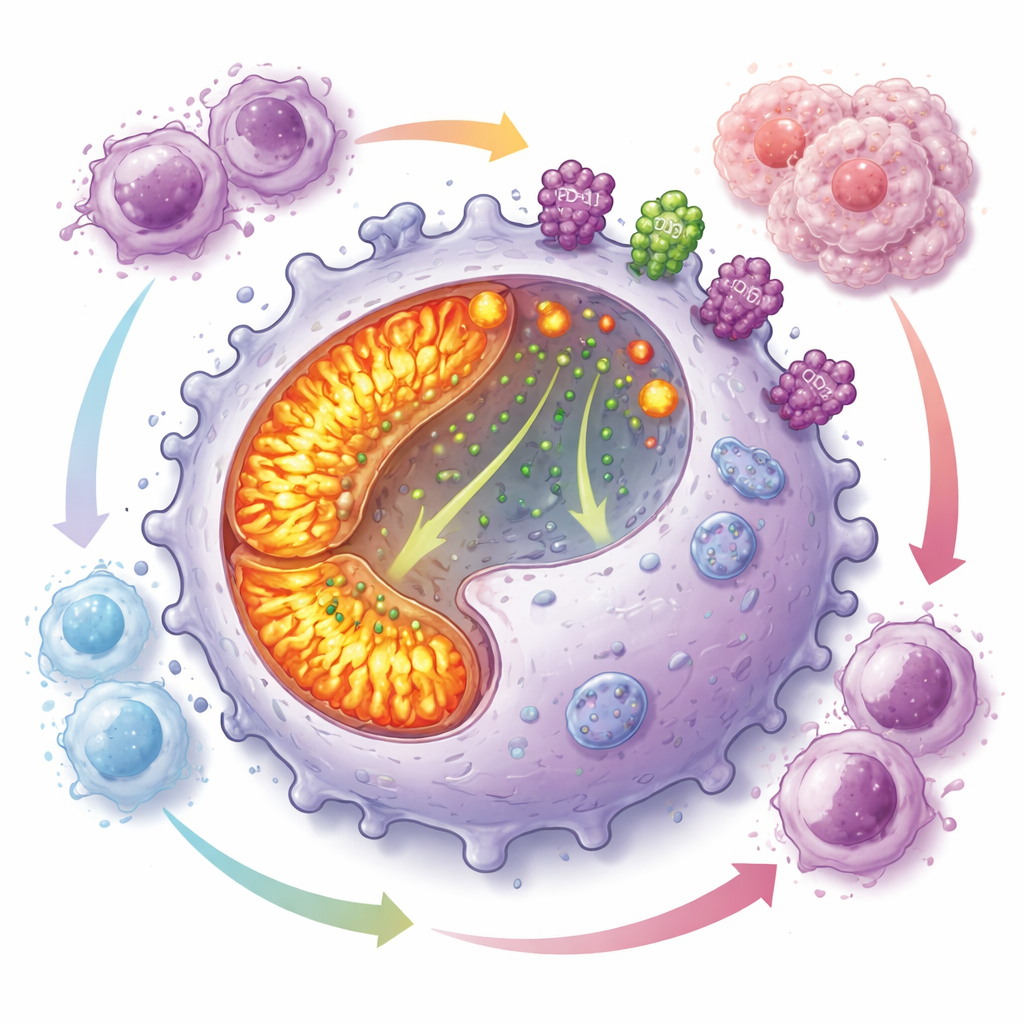
برنامج طاقي نهم يثبط الهجوم المناعي
بالغوص أعمق، وجد الفريق أن البلعميات الموجبة لـ CD19 تُشغّل "محطات الطاقة" الداخلية لديها بكثافة. كانت ميتوكوندرياتها، العضيات المسؤولة عن توليد الطاقة، أكثر عددًا ونشاطًا من تلك في البلعميات الأخرى، مع زيادة في الفسفرة التأكسدية وأنواع الأكسجين التفاعلية. على الرغم من هذه الحالة الطاقية، كانت هذه الخلايا ضعيفة في ابتلاع الأهداف لكنها تتكاثر بسرعة، ما يساعدها على التراكم داخل الأورام. في الوقت نفسه، أظهرت مستويات عالية من PD-L1 وCD73 على سطحها—جزيئتان معروفتان بإيقاف استجابات الخلايا التائية وتوليد الأدينوزين، الجزيء الصغير الذي يثبط المناعة بقوة. أظهرت تجارب التعايش الخلوي أن هذه البلعميات تثبط بقوة نمو أنواع متعددة من الخلايا التائية.
المفتاح الرئيسي خلف البلعميات الخائنة
حدد الباحثون عامل نسخ يُدعى PAX5 كسائق مركزي لهذا البرنامج الضار في البلعميات. يشتهر PAX5 بتوجيه تطور خلايا B، ومع ذلك وُجد هنا نشطًا بشدة في البلعميات الموجبة لـ CD19. أدى إجبار خلايا شبيهة بالبلعميات على التعبير عن PAX5 إلى تعزيز إنتاج الميتوكوندريا، وزيادة إنتاج الطاقة، ورفع مستويات البروتين—وليس الرنا المرسال—لـ PD-L1 وCD73 وCD19. أظهرت تجارب ميكانيكية أن PAX5 يجذب الكالسيوم إلى الميتوكوندريا، ما يخفض مستوى الكالسيوم في السيتوزول ويمنع عاملًا رئيسيًا مُنظمًا يُدعى TFEB من دخول النواة. ومع تأخير دخول TFEB، ينخفض إنتاج الليزوزومات ووظيفتها، فلا تُتَحلَّل البروتينات مثل PD-L1 وCD73 بكفاءة بل تتراكم على سطح الخلية، مما يعزز التثبيط المناعي.
تحويل الاكتشاف إلى خيارات علاجية أفضل
بما أن هذه البلعميات تعتمد اعتمادًا كبيرًا على نشاط CD73 والأيض الميتوكوندري، اختبر المؤلفون ما إذا كان حجب هذه المسارات يمكن أن يجعل العلاج المناعي أكثر فعالية. في سرطان الكبد لدى الفئران، أدى الجمع بين حجب PD-L1 مع أضداد CD73 أو مع مثبط لـ CD73 إلى أورام أصغر، ودخول المزيد من الخلايا التائية، وتقليل تكاثر خلايا السرطان. وبالمثل، أدى اقتران أضداد PD-L1 مع مثبط للفسفرة التأكسدية الميتوكوندرية إلى تحسن في السيطرة على الورم وزيادة دخول الخلايا المناعية إلى الأورام. وبشكل لافت، اختفت هذه الفوائد في فئران تفتقر بلعمياتها إلى PAX5، مؤكدة أن آثار الأدوية كانت مرتبطة تعطيل برنامج البلعميات المدفوع بـ CD19 وPAX5. مجتمعة، تشير النتائج إلى أن استهداف هذه الفئة الفرعية من البلعميات—عبر علاجات خلوية موجهة ضد CD19 أو تثبيط CD73 أو أدوية أيضية—قد يساعد في تحويل ورم الكبد المناعي "البارد" إلى ورم يستجيب بشكل أفضل بكثير لعلاجات تثبيط نقاط التفتيش المتاحة.
الاستشهاد: Wang, J., Cao, W., Huang, J. et al. Tumor-associated CD19+ macrophages induce immunosuppressive microenvironment in hepatocellular carcinoma. Nat Commun 17, 3250 (2026). https://doi.org/10.1038/s41467-026-69638-z
الكلمات المفتاحية: سرطان الخلايا الكبدية, البلعميات المرتبطة بالورم, العلاج المناعي, PD-L1 و CD73, الأيض الميتوكوندري