Clear Sky Science · ar
يعطّل التعبير النوعي لِـ HORMAD1 في الأورام توقّف الطور الانفصالي ويدفع نحو الحساسية لمثبطات كيناز الطور الانفصالي
لماذا يهم هذا لعلاج السرطان
عندما تنقسم خلايانا، تعتمد على فحوصات أمان معقدة لضمان نقل مجموعة الكروموسومات الصحيحة. غالباً ما تختطف السرطان هذه الضمانات أو تُضعفها، ما يؤدي إلى جينومات فوضوية تغذي المرض وتشكل استجابة الأورام للأدوية. تكشف هذه الدراسة كيف أن بروتينًا غير مألوف يُدعى HORMAD1، ينشط عادةً في الخلايا التناسلية فقط، يُعاد تشغيله في كثير من سرطانات الثدي العدوانية وأنواع أورام أخرى. عن طريق تخريب دقيق لنقطة تفتيش رئيسية في انقسام الخلايا، يجعل HORMAD1 الخلايا السرطانية أكثر عدم استقرار—ولكن أيضًا أكثر عرضة لفئة جديدة من الأدوية التجريبية.
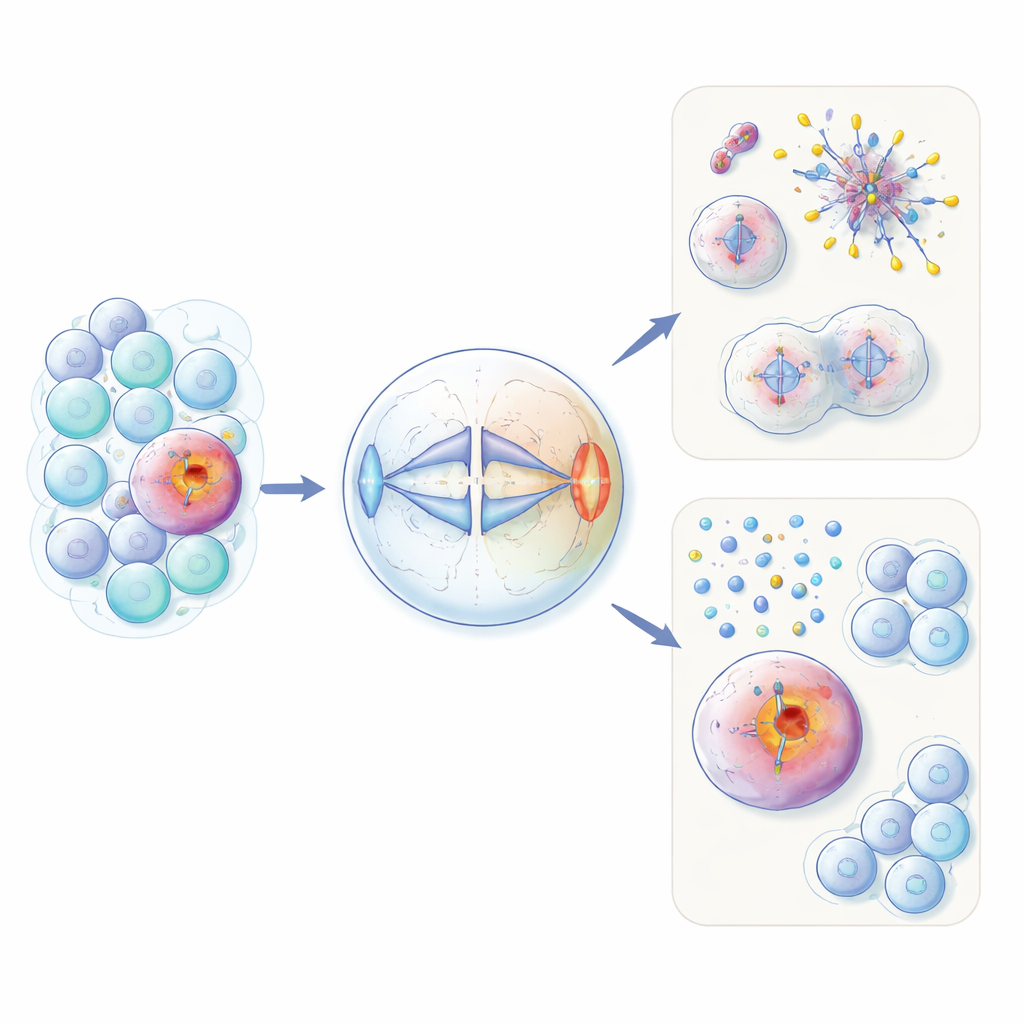
بروتين خصوبة في المكان الخطأ داخل خلايا السرطان
يظهر HORMAD1 عادةً في الخلايا الجرثومية فقط، حيث تتكوّن البويضات والحيوانات المنوية. هناك يساعد في إدارة إعادة ترتيب الحمض النووي ومراقبة الجودة أثناء نوع الانقسام الخاص المسمى الانقسام الاختزالي. يبين المؤلفون أن هذا البروتين يُعاد تفعيله بشكل غير مناسب في نحو 60% من سرطانات الثدي ثلاثية السلبية—وفي مجموعات فرعية من عدة أنواع أورام أخرى. باستخدام خلايا معدلة غير سرطانية وخطوط خلايا سرطانية، وجدوا أن وجود HORMAD1 الزائد يعيق الفصل المتساوي للكروموسومات أثناء الانقسام الخلوي العادي. ظهرت في الخلايا المعبرة عن HORMAD1 كروموسومات متأخرة أكثر، وكروموسومات زائدة أو ناقصة (تغيُّر عدد الصبغيات)، وبِذَر نووية صغيرة تحتوي على حمض نووي («ميكرونوكليي»)، كلها علامات مميزة للفوضى الجينومية التي تُرى في الأورام العدوانية.
كيف تعمل فحوصات أمان انقسام الخلايا عادةً
للانقسام بشكل صحيح، تبني الخلية مغزلًا من ألياف الدقيقات الميكروتيوبية التي تتصل بكل كروموسوم. يعمل نظام مراقبة يُعرف بنقطة تفتيش تركيب المغزل كفرملة حساسة للشد: إذا لم تكن أي كروموسوم متصلة بشكل صحيح، تمنع الفرملة التقدم وتبطل الانفصال حتى تُصحح الأخطاء. تساعد عدة إنزيمات تُدعى كينازات الطور الانفصالي، بما في ذلك MPS1 وAurora B وBUB1، في استشعار الاتصالات الخاطئة وتعزيز «تصحيح الأخطاء» حتى تحصل كل خلية بنت على مجموعة الكروموسومات الصحيحة. يمكن أن يؤدي تعطيل هذا النظام إلى تغذية تطور السرطان وفي الوقت نفسه خلق نقاط ضعف خاصة تستهدفها أدوية معينة.
HORMAD1 يضعف الفرملة بهدوء
اكتشف الباحثون أن HORMAD1 يقوّض هذه الفرملة بشكل دقيق لكن مهم. بدلًا من التداخل مع مكوّنات نقطة التفتيش التقليدية مثل بروتين HORMA المعروف MAD2L1، يرتبط HORMAD1 مباشرةً بالكيناز Aurora B. عادةً يتعاون Aurora B مع بروتين آخر، INCENP، ليصبح نشطًا بالكامل ويعدّل بروتينات عند السنتروميرات والكينيتيكور—مواقع حاسمة على الكروموسومات حيث تتصل ألياف المغزل. عندما يكون HORMAD1 موجودًا في الخلايا الورمية المنقَسمة، يتنافس مع INCENP على الوصول إلى Aurora B، مما يقلّل شراكتهما ويضعف نشاط Aurora B. نتيجة لذلك تضعف إشارات الفسفرة المميزة لـ Aurora B على عدة أهداف، يصبح تصحيح الأخطاء أقل فعالية، وتصبح نقطة التفتيش «متسربة»: تخرج الخلايا من الطور الانفصالي مبكرًا جدًا، حتى عندما تكون الاتصالات خاطئة، مما يؤدي إلى فصل غير صحيح للكروموسومات وعدم استقرار جينومي.
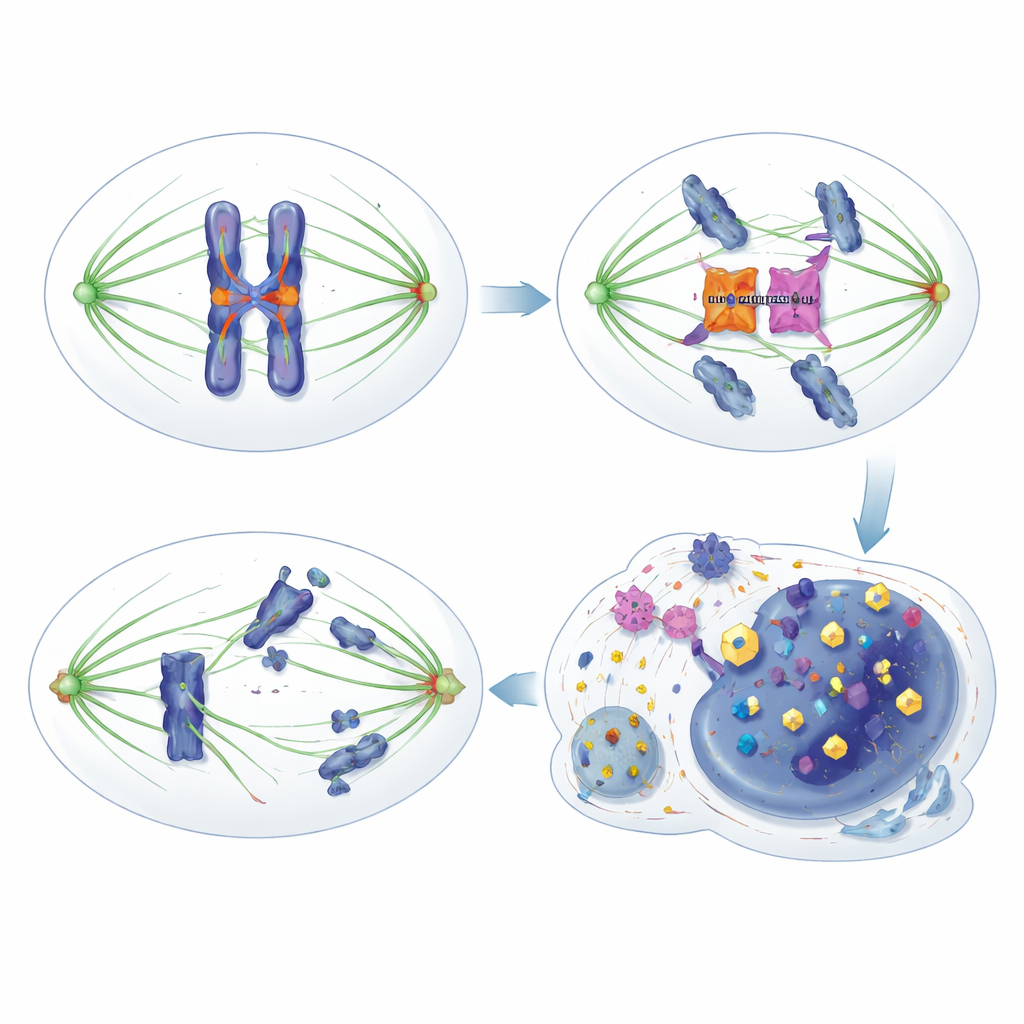
من الضعف إلى فرصة علاجية
لأن HORMAD1 يعيق جزئيًا فقط Aurora B والضوابط ذات الصلة، تبقى الخلايا السرطانية قابلة للحياة بدرجة كافية للنمو، لكنها تعتمد بشدّة على الوظائف المتبقية لكنازات الطور الانفصالي للبقاء على قيد الحياة بعد انقساماتٍ خاطئة متكررة. اختبر الفريق ذلك بتعرّض خلايا موجبة وسالبة التعبير عن HORMAD1 لمثبطات تجريبية لـ MPS1 وAurora B وBUB1. عبر نماذج متعددة، جعل تعبير HORMAD1 الخلايا أكثر حساسية لهذه الأدوية بكثير، مما قلّل بشكل دراماتيكي قدرتها على التكاثر أو تكوين مستعمرات. كان تقليل BUB1 وراثيًا مميتًا بشكل خاص فقط في وجود HORMAD1، كاشفًا عن اعتماد انتقائي قوي. في نماذج فأرية باستخدام أورام ثدي ثلاثية السلبية مشتقة من مرضى، انكمشت أو نمت الأورام ذات مستويات HORMAD1 العالية ببطء أكبر عندما عُولِجت بصيغة نانوية لمثبط Aurora B، بينما كانت الأورام السالبة لـ HORMAD1 مقاومة إلى حد كبير لنفس العلاج.
ماذا يعني هذا للمرضى
للمراقب العادي، يعمل HORMAD1 كسيف ذي حدين في السرطان: يدفع خلايا الورم نحو اضطراب كروموسومي أكبر، ما قد يغذي المرض، لكنه في نفس الوقت يجعلها معتمدة بشكل هش على عدد قليل من ضوابط انقسام الخلايا المتبقية. تُظهر الدراسة أن هذا البروتين الخصصي للخصوبة يضعف نقطة تفتيش رئيسية عن طريق تحويل توجيه Aurora B، مما يجعل الأورام الموجبة لـ HORMAD1 هشة بشكل خاص تجاه الأدوية التي تستهدف Aurora B أو MPS1 أو BUB1. وبما أن HORMAD1 غائب إلى حد كبير عن الأنسجة الطبيعية لكنه موجود بوضوح في مجموعة فرعية من السرطانات، فقد يعمل كمؤشّر حيوي لتحديد المرضى الأكثر احتمالًا للاستفادة من هذه المثبطات الناشئة لكنازات الطور الانفصالي، مما يفتح فرص علاجية مستهدفة جديدة لأورام يصعب علاجها مثل سرطان الثدي ثلاثي السلبية.
الاستشهاد: Walker, C., Kollarovic, G., Weekes, D. et al. Tumour specific HORMAD1 expression perturbs mitotic arrest and drives sensitivity to mitotic kinase inhibitors. Nat Commun 17, 2157 (2026). https://doi.org/10.1038/s41467-026-69561-3
الكلمات المفتاحية: HORMAD1, سرطان الثدي ثلاثي السلبية, عدم استقرار كروموسومي, كيناز أورورا B, مثبطات نقطة تفتيش الانقسام