Clear Sky Science · ar
استعادة Bifidobacterium longum والتدخلات قبل الحيوية للتغلب على تغيُّرات السلوك الغذائي الناجمة عن نظام غذائي عالي الدسم/السكر في مرحلة مبكرة لدى الفئران البالغة
لماذا قد تستمر عادات الوجبات الخفيفة المبكرة لتؤثر في مرحلة البلوغ
ما نتناوله في أيامنا الأولى قد يضبط بهدوء أدمغتنا وأمعاءنا لسنوات قادمة. تطرح هذه الدراسة على الفئران سؤالاً ذا صدى واضح لدى البشر: إذا تعرَّضَت الصغار لأطعمة غنية وعالية الدهون والسكريات، هل يتغير أسلوب أكلهم في البلوغ—وهل يمكن لبكتيريا الأمعاء الصديقة وألياف غذائية خاصة أن تساهم في تدارك الضرر؟ بمتابعة الفئران منذ الولادة وحتى البلوغ، تتبّع الباحثون كيف يعيد نظام غذائي «سريع» مبكر تشكيل ميكروبات الأمعاء وخلايا الدماغ التي تتحكم في الشهية وتفضيلات الطعام على المدى الطويل، وبطرق تختلف بين الإناث والذكور.
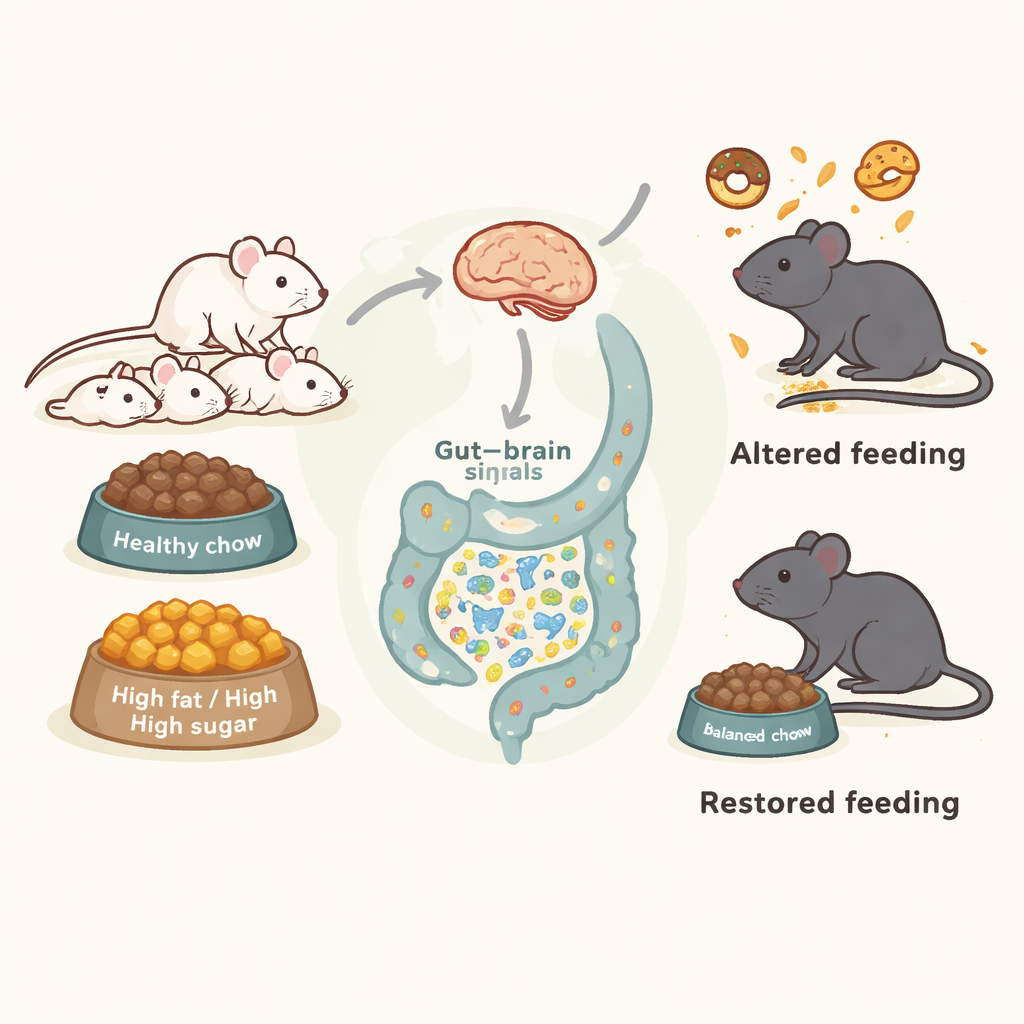
بصمة خفيّة يتركها الطعام السريع المبكر
أُطعِمت الفئران الوليدة وأمهاتها إما علفاً قياسياً صحياً أو نظاماً غذائياً عالي الدهون والعالي السكر (HFHS) يحاكي نمط الوجبات السريعة الغربي. أُعطي الغذاء الغني فقط خلال وقت مبكر من الحياة—من الولادة وحتى الفطام وفترة قصيرة بعدها—ثم عُوِّضَت جميع الحيوانات لاحقاً بالعلف الطبيعي. ورغم هذا «تصحيح المسار» المتأخر وتشابه أوزان البالغين في النهاية، ترك التعرض المبكر للنظام HFHS آثاراً دائمة. كبالغين، أظهرت الفئران التي تعرّضت سابقاً هذا النظام، من كلا الجنسين، تفضيلاً أقوى للطعام اللذيذ HFHS عند إعطائهم خياراً، ومارَسُوا مزيداً من «تفتت الطعام»—سلوك تلاعبي يقومون فيه بنزع الطعام وطحنه دون أكله بالكامل. تشير هذه التحولات إلى أن النظام الغذائي المبكر يمكنه تهيئة مدى جاذبية الأطعمة الغنية وطريقة تفاعل الحيوانات معها.
الميكروبات المعوية كوسطاء بين الغذاء والدماغ
تابع الفريق عن كثب ميكروبيوتا الأمعاء—التريليونات من الميكروبات التي تعيش في الأمعاء—ووجد أن النظام HFHS المبكر قلل من البكتيريا التابعة لمجموعة Bifidobacterium، والتي تكون عادة وفيرة في أوائل الحياة ومرتبطة بالصحة الأيضية. رافقت تغيُّرات الميكروبيوم تغيرات في مستويات العديد من المواد الكيميائية في الدم، بما في ذلك الأحماض الأمينية وجزيئات مرتبطة بالصفراء ومركبات مشتقة من التريبتوفان التي يمكن أن تؤثر في وظائف الدماغ والمزاج. والأهم أن هذه الآثار لم تكن متطابقة لدى الإناث والذكور. أبدت الإناث اضطراباً أكبر في المسارات المرتبطة بأيض الأرجينين والتريبتوفان، بينما أظهر الذكور تغييرات في جزيئات مرتبطة بالصفراء والستيرويدات وفي كيفية استشعار أجسامهم لمكونات جدران الخلايا البكتيرية. تشير هذه الأنماط الخاصة بالجنس إلى أن النظام الغذائي المبكر قد يزيد خطر المرض عبر مسارات بيوكيميائية مختلفة لدى النساء والرجال.
إعادة توصيل دوائر الدماغ المسؤولة عن الشهية
بما أن الشهية منسقة في منطقة تحت المهاد، وهي منطقة عميقة في الدماغ تجمع الإشارات من الجسم، فحص الباحثون هذه البُنية بتفصيل. وجدوا تغييرات واسعة وطويلة الأمد في نشاط الجينات هناك، لا سيما لدى الإناث، حيث تأثرت آلاف الجينات أكثر مما حدث لدى الذكور. داخل محور مهم في تحت المهاد يُدعى النواة القوسية، لوحظ وجود خلايا أقل تُنتج POMC، وهو جزيء يساعد عادة على كبح الأكل، وكذلك خلايا أقل تحمل مستقبلات لهرمون الليبتين والغريلين، اللذين ينبهان الشبع والجوع. كما انخفض عدد مجموعة من الخلايا العصبية المثبطة والمعلمة بجزيء PNOC، والخلايا الحاملة لمستقبل استشعار البكتيريا NOD2. مجتمعةً، تُشير هذه التغيرات إلى أن النظام HFHS المبكر يضعف قدرة الدماغ على قراءة إشارات توازن الطاقة وميكروبات الأمعاء، مما يهيئ الحيوانات للإفراط في الأكل أو اضطراب السلوك الغذائي حتى بعد عودة الوزن إلى وضعه الطبيعي.
الألياف الصديقة والبكتيريا تقدم جزئياً إعادة ضبط
اختبرت الدراسة بعد ذلك استراتيجيتين لمستهدفات الميكروبيوتا أُعطيتا في ماء الشرب منذ الولادة فصاعداً: مزيج ألياف قبل حيوية (فركتو‑وغالاكتي‑أوليغوسaccharides، FOS+GOS) مصمم لتغذية الميكروبات المفيدة، وسلالة محددة من Bifidobacterium longum (APC1472). عزَّزت كلتا الاستراتيجيتين إما مجموع Bifidobacterium العام (FOS+GOS) أو هذه السلالة المحددة (APC1472)، وكلاهما خفف العديد من التغيرات السلوكية الناتجة عن نظام HFHS المبكر. انخفضت عادة تفتت الطعام والاستهلاك المفرط للطعام اللذيذ، وفي الذكور عاد الميل المتزايد لمُحلٍّ خالٍ من السعرات إلى مستواه الطبيعي. في الدماغ، أعادت التدخلات كلاهما أعداد خلايا POMC وPNOC والعديد من الخلايا الإيجابية لـ NOD2 في النواة القوسية، مع تعافٍ قوي بشكل خاص لدى الإناث. ومع ذلك اختلفت الآليات: أحدثت FOS+GOS تحولات واسعة في تركيب الميكروبيوم ومسارات مرتبطة بالمحور أمعاء‑دماغ، بينما أحدثت B. longum APC1472 تغييرات أيضية ودماغية أكثر استهدافاً مع إعادة تشكيل متواضعة نسبياً للمجتمع الميكروبي الكلي.
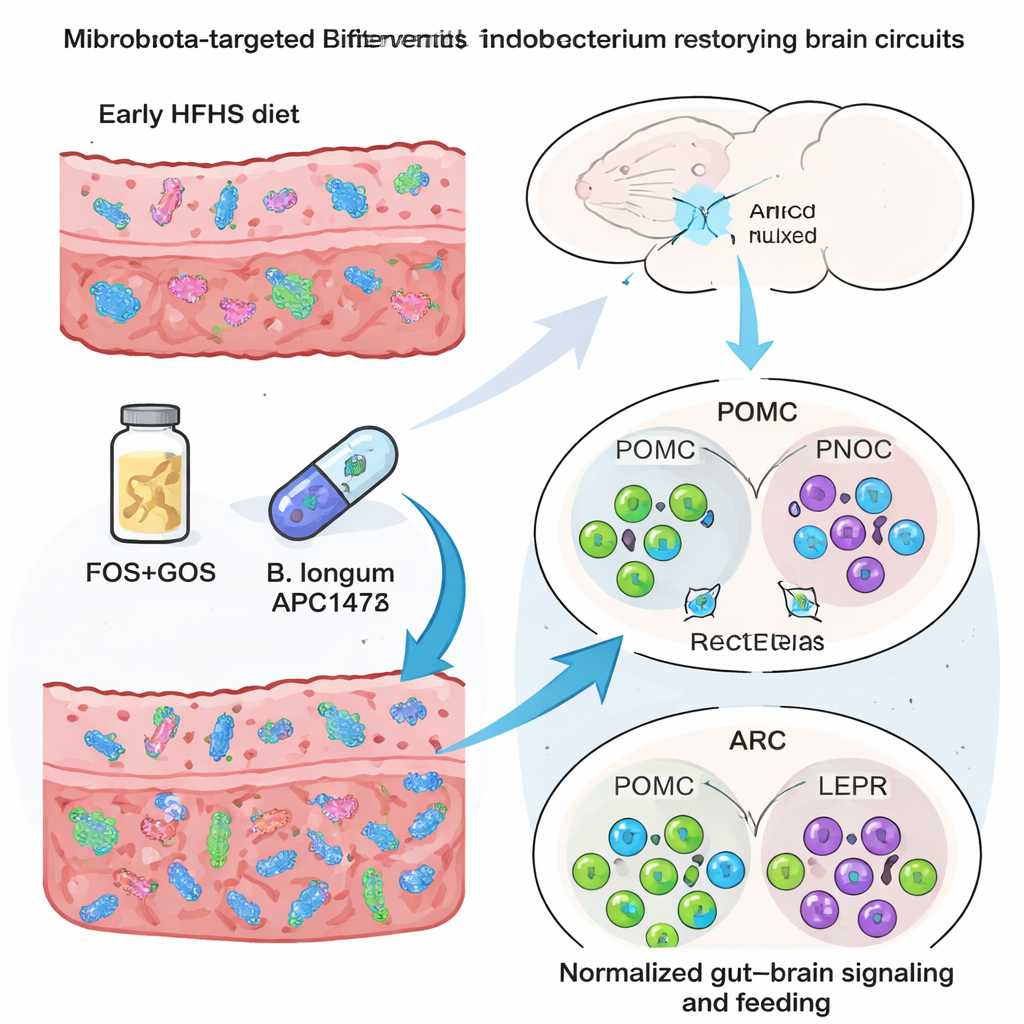
ماذا يعني ذلك للأنظمة الغذائية والعلاجات المستقبلية
للقارئ العام، الرسالة حازمة لكنها متفائلة. يمكن لنظام غذائي غير صحي عالي الدهون والسكريات في وقت مبكر من الحياة أن يترك «برمجة» عميقة على ميكروبات الأمعاء وكيمياء الدم ودوائر الدماغ التي توجه الشهية، وتستمر هذه البصمات حتى بعد عودة مؤشرات ظاهرية مثل وزن الجسم إلى الطبيعي. تبدو الإناث أكثر عرضة على مستوى شبكات الجينات الدماغية، بينما يُظهر الذكور تغييرات مميزة في كيفية استشعارهم لمنتجات البكتيريا والهرمونات. في الوقت نفسه، يمكن لألياف قبل حيوية وسلالات بروبيوتيك مختارة بعناية أن تصلح إلى حد كبير هذه التغيرات الخفية في الفئران، مهدئةً السلوك الغذائي المضطرب ومعيدةً توازن اتصال الأمعاء‑الدماغ. رغم الحاجة لمزيد من العمل قبل ترجمة هذه النتائج إلى البشر، تعزز الدراسة فكرة أن دعم ميكروبيوم صحي خلال الحمل والطفولة المبكرة—عبر النظام الغذائي وربما مكمّلات مستهدفة—قد يساعد على حماية سلوك الأكل طوال الحياة وتقليل خطر السمنة والاضطرابات ذات الصلة.
الاستشهاد: Cuesta-Marti, C., Ponce-España, E., Uhlig, F. et al. Bifidobacterium longum and prebiotic interventions restore early-life high-fat/high-sugar diet-induced alterations in feeding behavior in adult mice. Nat Commun 17, 1653 (2026). https://doi.org/10.1038/s41467-026-68968-2
الكلمات المفتاحية: ميكروبيوم الأمعاء, التغذية في وقت مبكر من الحياة, بروبيوتيك, السلوك الغذائي, مخاطر السمنة