Clear Sky Science · ar
بوليمرات مقلدة للبروتينات ذات وظيفتين مختلفتين للتحلّل المستهدف لبروتينَي MYC وKRAS
أدوات جديدة لإسقاط أخطر بروتينات السرطان
كثير من البروتينات الأكثر خطورة في دفع السرطان، مثل MYC وKRAS، وُصفت طويلاً بأنها "غير قابلة للعلاج" لأن الأدوية لا تستطيع الالتصاق بها بسهولة. تكشف هذه الدراسة عن نوع جديد من المواد الاصطناعية اللينة — المسماة بوليمرات HYDRAC — التي تستطيع الإمساك بهذه البروتينات الزلقة وإرسالها إلى نظام التخلص الخلوي. بالنسبة للقراء، يقدم هذا العمل لمحة عن كيفية فتح الكيمياء وتكنولوجيا النانو لخيارات علاجية لأنواع من السرطان التي قاومت الأدوية التقليدية.
هيكل مرن بدلًا من حبة واحدة
معظم أدوية السرطان الموجّهة هي جزيئات صغيرة تدخل جيوبًا على سطح البروتين، مثل المفتاح في القفل. لكن بروتينات مثل MYC مرنة وتفتقر إلى جيوب مناسبة، بينما يتغيّر KRAS غالبًا بطرق تذهب دون متناول الأدوية الكلاسيكية. صمّم الباحثون بدلاً من ذلك بوليمرات طويلة على شكل سلاسل مكونة من وحدات متكررة. على هذه السلاسل يركّبون نوعين من المكوّنات: قطع قصيرة تربط البروتين تتعرف على هدف مثل MYC أو RAS، ومقاطع "ديغرون" تجذب آلية التخلص الخلوية. وبما أن نسخًا عديدة من كل مكوّن تزيّن نفس السلسلة، يمكن لجزيء HYDRAC واحد الوصول إلى بروتينات وإنزيمات متعددة في آن واحد، وهو أمر يصعب تحقيقه بجزيء دوائي واحد صلب.
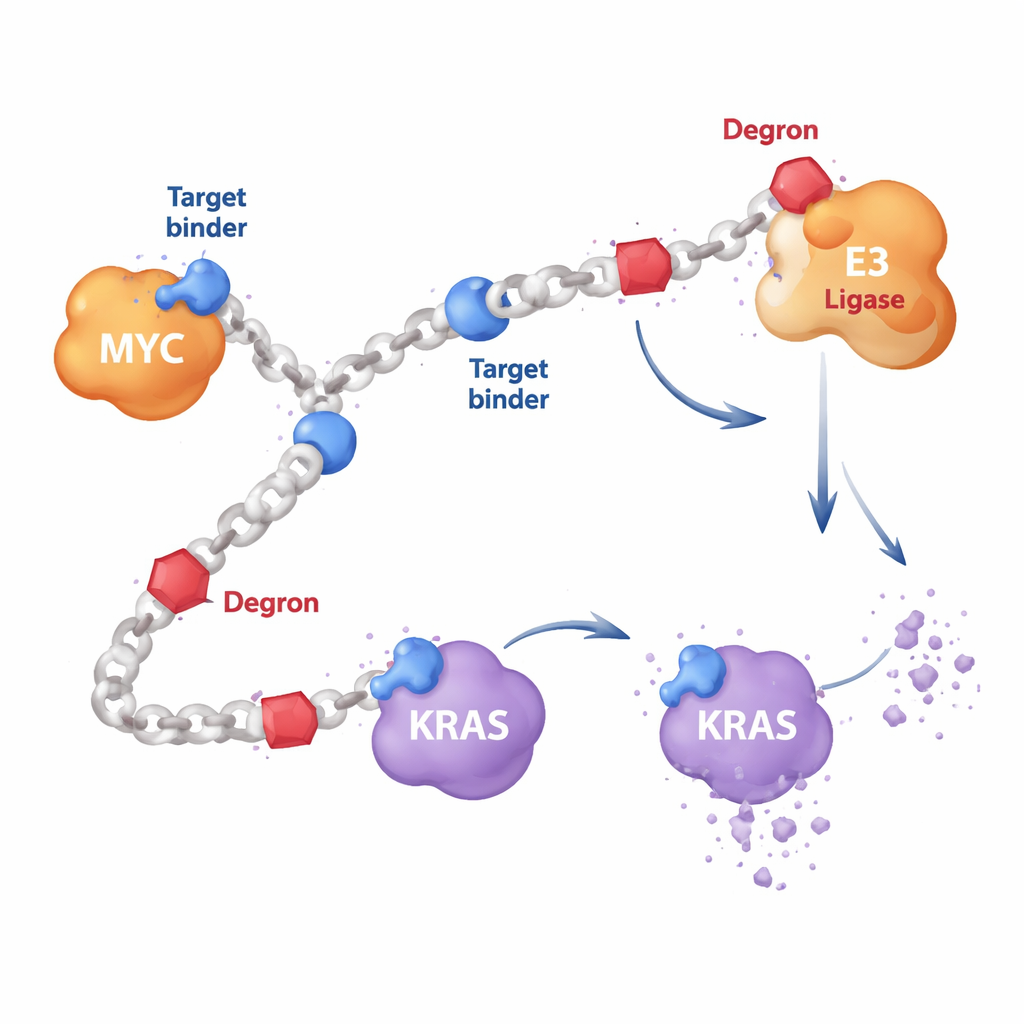
تعليم الخلايا على تكسير MYC
كمحكّ أولي، ركز الباحثون على MYC، وهو مفتاح رئيسي يدفع النمو في العديد من السرطانات لكنه قاوم الهجوم المباشر لعقود. بنوا بوليمرات HYDRAC تعرض ببتيدًا معروفًا رابطًا لـ MYC إلى جانب نمط ديغرون بسيط يشير إلى البروتينات لتدميرها عبر البروتيازوم، المقطّعة البروتينية الرئيسة في الخلية. في تجارب أنابيب الاختبار، طوت هذه البوليمرات نفسها إلى أشكال مدمجة شبيهة بالبروتين وربطت بقوة بـ MYC لكن ليس ببروتينات غير ذات صلة. في خلايا سرطانية، دخلت HYDRACs بسهولة، وعطّلت برامج الجينات التي يتحكم بها MYC، وأحدثت موتًا خلويًا — تأثيرات كانت تعتمد على وجود مكوّنَي الاستهداف والديغرون معًا على نفس السلسلة البوليمرية.
من زراعة الخلايا إلى تصغير الأورام
داخل الخلايا، أدت معالجة HYDRAC إلى انخفاض حاد في مستويات بروتين MYC دون تقليل RNA الخاص به، مما يدل على تدمير حقيقي وليس فقط إيقافًا مؤقتًا للنسخ. إن حجب البروتيازوم أو إنزيمات رئيسية تفعل مسارات التحلل أنقذ مستويات MYC، مما يبيّن أن البوليمرات تعمل بإعادة توجيه أنظمة التخلص الخلوية. كشفت تحليلات شاملة للبروتيوم أن القليل جدًا من البروتينات الأخرى تأثرت، مشيرة إلى انتقائية ملحوظة. في نماذج الفئران للأورام المدفوعة بـ MYC، تراكمت HYDRACs المعلمة فلوريسنتيًا بشكل تفضيلي في الأورام بعد الحقن وبقيت هناك لأيام. أدت الجرعات المتكررة إلى إبطاء نمو الأورام دون فقدان وزن كبير أو تلف أنسجة واضح، وأظهرت عينات الأورام خلايا أقل انقسامًا ومزيدًا من علامات الموت المبرمج.
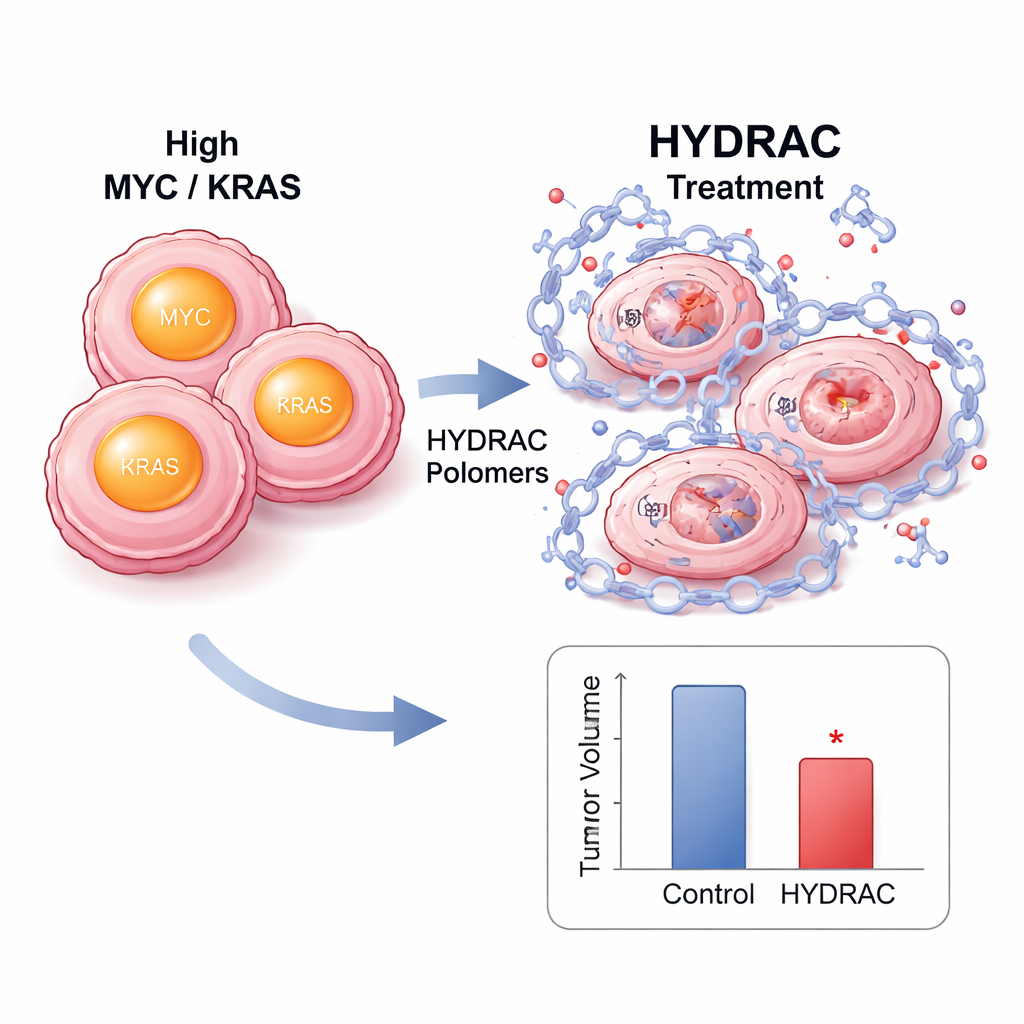
منصة قابلة للتبديل للعديد من أهداف المرض
أحد نقاط قوة نهج HYDRAC هو أن المجموعات الجانبية يمكن تبديلها مثل قطع قابلة للإحلال. استبدل الفريق الديغرون الأصلي بعناصر تجنيد أخرى تستدعي إنزيمات خلوية مختلفة، بما في ذلك تلك التي تتعرف على عقار ثاليدوميد. كل نسخة حرّمت MYC فقط عندما كان الإنزيم المقصود موجودًا وفعّالًا، مؤكدة أن البوليمرات يمكن ضبطها لاستخدام مسارات خلوية متميزة. لاختبار العمومية، بنى الباحثون بعد ذلك HYDRACs موجهة لـ RAS باستخدام ببتيد يتعرف على بروتينات RAS. نجحت هذه البنى في تحلل KRAS المتحور في خطيْن خلوييْن سرطانِيَيْن مختلفين، ملمحةً إلى إمكانات "شاملة لـ KRAS" لا تعتمد على طفرة معينة — وهو خطوة هامة للأورام حيث تتعايش عدة متغيرات من KRAS.
لماذا هذا مهم لرعاية السرطان المستقبلية
يقدّم هذا العمل HYDRACs كفئة جديدة من المواد القابلة للبرمجة التي لا تقتصر على حجب البروتينات المزعجة — بل تساعد الخلايا على محوها. من خلال تجميع وحدات استهداف وتحلل عديدة على بوليمر مرن، تتجاوز HYDRACs قيود التصميم للأدوية الجزيئية الصغيرة التقليدية وPROTACs، التي عادةً ما تحمل واحدًا من كل نوع فقط. وبينما ما يزال هناك الكثير لفعله قبل أن تصل هذه المواد إلى العيادة، تشير النتائج في نماذج مدفوعة بـ MYC وKRAS إلى أن بروتينات السرطان التي اعتُبرت "غير قابلة للعلاج" قد تكون، في الواقع، عُرضة للهجوم عندما يشبه الطب أكثر فرشاة جزيئية مصممة من مكوّنات متعددة بدلاً من حبة صغيرة واحدة.
الاستشهاد: Wang, M.M., Truica, M.I., Gattis, B.S. et al. Heterobifunctional proteomimetic polymers for targeted degradation of MYC and KRAS. Nat Commun 17, 1706 (2026). https://doi.org/10.1038/s41467-026-68913-3
الكلمات المفتاحية: التحلل الموجّه للبروتينات, MYC, KRAS, علاجات بوليمرية, طب النانو في السرطان