Clear Sky Science · ar
المشهد الإبيجيني التكاملي لأدمغة مرض الزهايمر يكشف اضطرابات جزيئية في الخلايا قليلة التغصن مرتبطة بالتاو
لماذا تهمنا هذه الأبحاث الدماغية
يشتهر مرض الزهايمر بفقدان الذاكرة وتراكم بروتينين مضطربين في الدماغ: الأميلويد والتاو. ومع ذلك يمكن أن يظهر لدى المصابين أنماط أضرار مختلفة جداً، حتى عندما يتشاركون نفس التشخيص. تطرح هذه الدراسة سؤالاً أساسياً: ما هي المفاتيح داخل خلايا الدماغ التي تساعد في تحديد مقدار تراكم هذه البروتينات الضارة، وكيف تؤثر على أنواع الخلايا المختلفة؟ من خلال فحص علامات كيميائية على الحمض النووي في مئات الأدمغة، يكشف الباحثون عن صلة مفاجئة بين التاو والخلايا المسؤولة عن عمل توصيلات الدماغ.
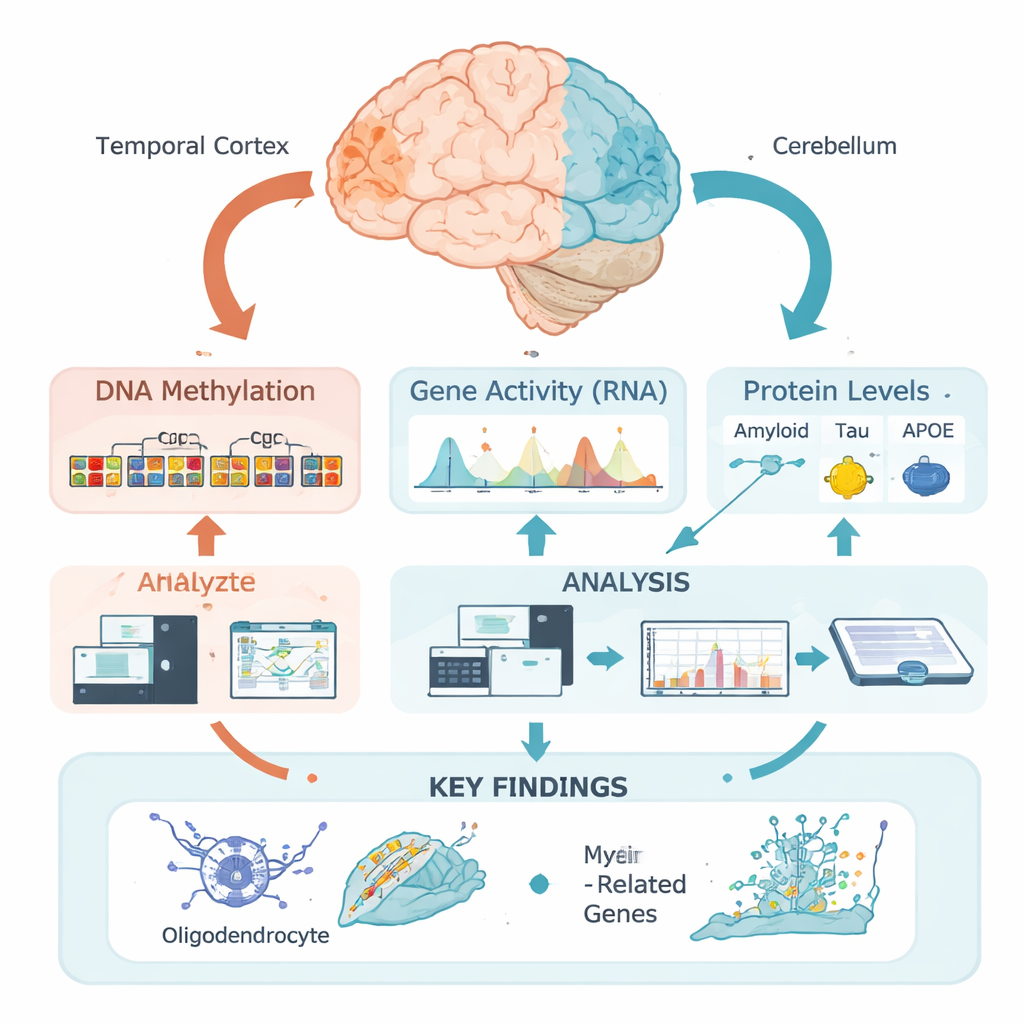
العلامات الكيميائية على الحمض النووي كمفاتيح خفية
يحمل حمضنا النووي التعليمات الأساسية لبناء وتشغيل خلايا الدماغ، لكن تُدار هذه التعليمات بواسطة علامات إبيجينية—علامات كيميائية يمكنها رفع أو خفض نشاط الجينات المجاورة دون تغيير الشيفرة الجينية. واحدة من أهم هذه العلامات هي مثيلة الحمض النووي، حيث تلتصق مجموعات كيميائية صغيرة بمواقع محددة على الحمض النووي. بدلاً من فحص مواقع مفردة بشكل معزول، استخدمت هذه المجموعة نهجاً "إقليمياً" جديداً: جمعت العديد من المواقع القريبة في مناطق وظيفية اعتماداً على كيفية تغليف الحمض النووي في القشرة الصدغية، وهي منطقة تتأثر بشدة في الزهايمر، والمخيخ، الذي يُعد محمى نسبياً. سمح لهم هذا بطرح سؤال أين، بمعنى بيولوجي، تتغير أنماط المثيلة بالنسبة لميزات المرض.
ربط علامات الحمض النووي ببروتينات الزهايمر
حلل الباحثون نسيج دماغي من 472 شخصاً تم تأكيد إصابتهم بالزهايمر بعد الوفاة. لكل عينة من القشرة الصدغية، قاسوا مستويات مفصلة من الأميلويد والتاو وبروتين APOE بأشكال بيوكيميائية مختلفة، بالإضافة إلى الدرجات الميكروسكوبية التقليدية للوح أميلويد وتشابكات تاو. ثم أجروا دراسات ارتباط عبر الإبيجينوم بأكمله، اختبروا فيها ما إذا كانت مستويات المثيلة الإقليمية تتوافق مع هذه القياسات. ولافت للنظر أن تقريباً كل الارتباطات القوية التي وجدواها كانت مرتبطة بالتاو لا بالأميلويد—وخاصة بالتاو القابل للذوبان الكلي والشكل الفسفوري المرتبط بالغشاء (المعدل كيميائياً) الذي يُعتقد أنه سام بشكل خاص.
إشارة قوية في خلايا توصيل الدماغ
كانت العديد من مناطق الحمض النووي المرتبطة بالتاو تقع في أجزاء "نشطة" من الجينوم تؤثر على الجينات المجاورة. من خلال دمج بيانات المثيلة مع قياسات نشاط الجينات من نفس الأدمغة، أظهر الفريق أن هذه المناطق غالباً ما تتحكم في جينات تستخدمها الخلايا قليلة التغصن—الخلايا التي تكسو الألياف العصبية بغلاف المايلين العازل، مما يسمح للإشارات الكهربائية بالسفر بسرعة وموثوقية. ظهرت جينات رئيسية متعلقة بالمايلين مثل MBP وMAG وMYRF، إلى جانب جين الخطر للزهايمر BIN1 وجين مرشح أحدث يُدعى LDB3، ضمن هذه المجموعة. ربطت مستويات أعلى من التاو الفسفوري السام عادةً بزيادة في المثيلة عند هذه المناطق وانخفاض في تعبير الجينات المرتبطة بالخلايا قليلة التغصن والمايلين، بينما أظهر تجمع التاو القابل للذوبان الكلي الأكثر حميدة النمط المعاكس.
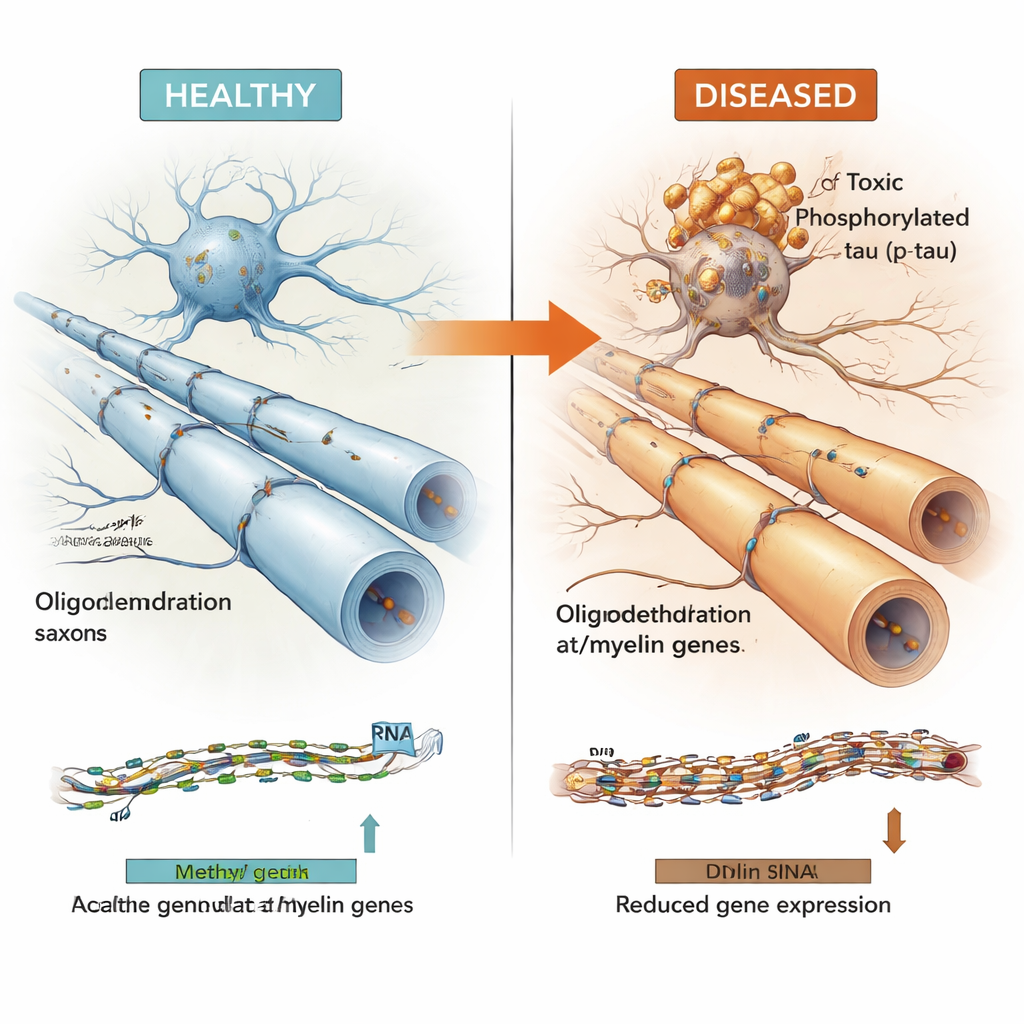
نمط يُرى عبر أمراض دماغية متعددة
لاختبار ما إذا كانت هذه النتائج قوية وعامة، فحص المؤلفون مجموعات بيانات كبيرة ومستقلة من مجموعات أدمغة زهايمر أخرى، ومن أدمغة متأثرة بـ"تاووباتيات" أولية مثل الشلل فوق النووي التقدمي ومرض بيك. على الرغم من أن هذه المجموعات قيسَت باستخدام تقنيات مختلفة وغالباً في مناطق دماغية مختلفة، أظهرت العديد من نفس مناطق الحمض النووي وجينات الخلايا قليلة التغصن سلوكاً متسقاً: مستويات المثيلة فيها ارتبطت بعبء تشابكات التاو، وكان تعبيرها مُنخفضاً في الأدمغة المريضة وفي دراسات الخلية الواحدة التي ركزت تحديداً على الخلايا قليلة التغصن. والأهم أن هذه الأنماط لم تبدُ قابلة للتفسير ببساطة عبر العوامل الوراثية أو بفقدان الخلايا العام، ما يشير إلى تحول إبيجيني حقيقي في كيفية عمل الخلايا قليلة التغصن.
ماذا يعني هذا لفهم الزهايمر
مجتمعة، تدعم النتائج نموذجاً ترى أن مستويات التاو الضارة المتزايدة مرتبطة ارتباطاً وثيقاً بتغييرات إبيجينية في الخلايا قليلة التغصن تُخمد الجينات المتعلقة بالمايلين، مما قد يضعف توصيلات الدماغ ويسهم في التدهور المعرفي. لا يزال غير واضح أيهما يسبق الآخر—تراكم التاو أم اضطراب هذه الجينات المتعلقة بالمايلين—لكن الارتباطات المتكررة والوثيقة عبر آلاف العينات والعديد من الأمراض تشير إلى آلية مشتركة. من خلال رسم هذه المفاتيح على الحمض النووي ودمجها في "أطلس متعدد الأوميات" عام، يبرز هذا العمل الخلايا قليلة التغصن وتنظيمها الإبيجيني كأهداف واعدة للعلاجات المستقبلية الهادفة إلى استقرار دوائر الدماغ، بدلاً من التركيز حصراً على الخلايا العصبية أو لويحات الأميلويد.
الاستشهاد: Oatman, S.R., Reddy, J.S., Atashgaran, A. et al. Integrative epigenomic landscape of Alzheimer’s Disease brains reveals oligodendrocyte molecular perturbations associated with tau. Nat Commun 17, 2116 (2026). https://doi.org/10.1038/s41467-026-68864-9
الكلمات المفتاحية: مرض الزهايمر, بروتين تاو, مثيلة الحمض النووي, الخلايا قليلة التغصن, المايلين