Clear Sky Science · ar
بالميتويلاشن ASCT2 المنظم بواسطة محور JNK1-ZDHHC14 ينظم أيض الجلوتامين وتقدّم سرطان الرئة غير صغير الخلايا
إشعال نار السرطان الرئوي
تعتمد العديد من سرطانات الرئة سريعة النمو على الجلوتامين، وهو حمض أميني شائع يعمل كوقود رئيسي ولبنة بنائية. تكشف هذه الدراسة كيف تضبط الخلايا الورمية بوابة رئيسية لدخول الجلوتامين على سطحها، وكيف أن تعطيل هذا النظام الضابطي قد يبطئ نمو السرطان. فهم هذه الصمام الخفي للوقود يساعد على تفسير سبب صعوبة تجويع بعض الأورام ويشير إلى مجموعات أدوية جديدة قد تقطع إمدادها بالطاقة بفعالية أكبر.
بوابة خلوية للجلوتامين
يدخل الجلوتامين الخلايا أساساً عبر بروتين ناقل يُسمى ASCT2، الموجود في الغشاء الخارجي وينقل الجلوتامين إلى الداخل. يعتمد سرطان الرئة غير صغير الخلايا (NSCLC)، الشكل الأكثر شيوعاً من سرطان الرئة، غالباً على الجلوتامين لدعم الانقسام السريع والبقاء. ترتبط المستويات العالية من ASCT2 في الأورام بمرض عدواني وتوقعات سيئة للمرضى. ومع ذلك، يتم صنع وتعديل وتدمير ASCT2 باستمرار، مما يطرح السؤال: ما الذي يحدّد مقدار هذا الحارس الذي يبقى على سطح الخلية في أي وقت؟
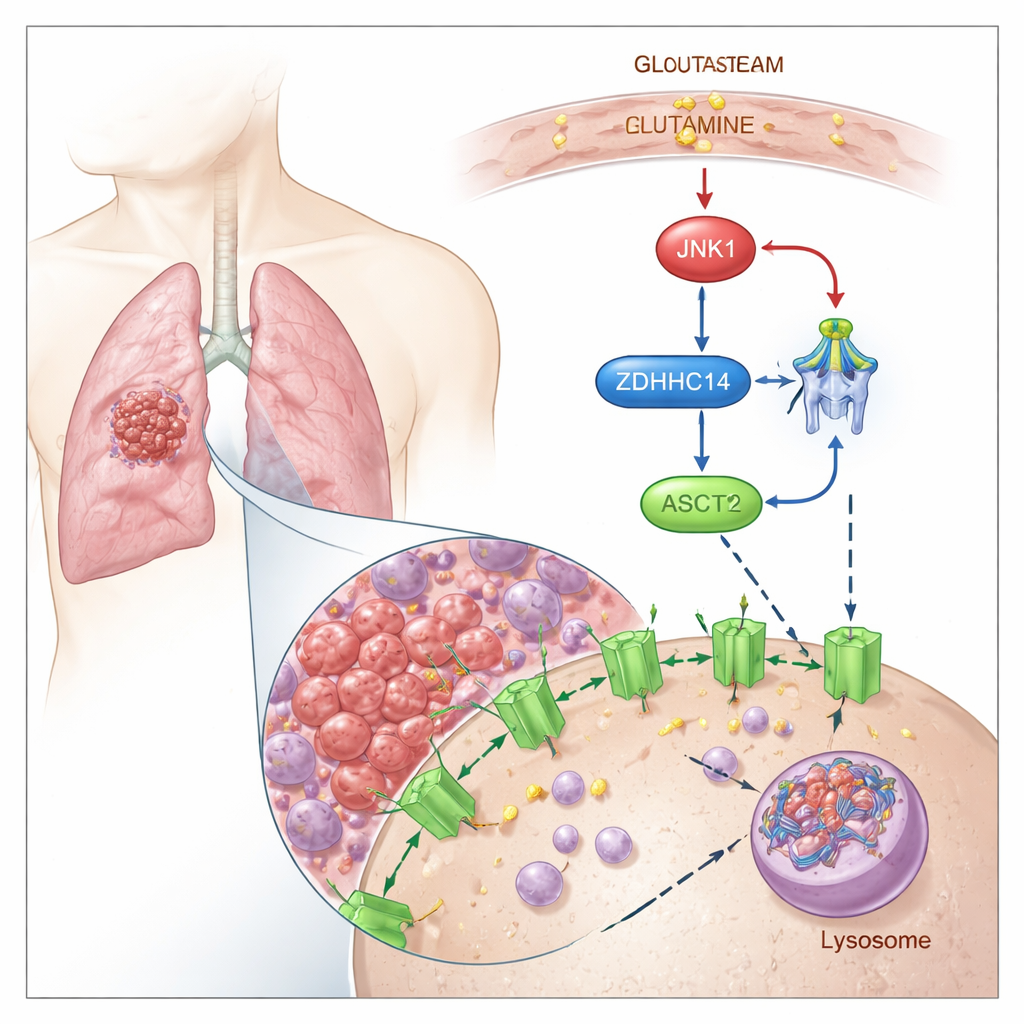
وسم ASCT2 للتفكيك
تُظهر النتائج أن ASCT2 يخضع للتحكم بواسطة وسم كيميائي يُدعى بالميتويلاشن، حيث يُلحق حمض دهني ببقايا سيستين محددة في البروتين. وجد الباحثون أن إنزيمًا يُدعى ZDHHC14 يضيف هذا الوسم الدهني إلى موقعين محفوظين في ASCT2 (Cys39 و Cys48). بعد الوسم، يُعاد توجيه ASCT2 من سطح الخلية إلى مراكز إعادة التدوير الخلوية المسماة الليزوزومات، حيث يُتفكك. يمنع حجب البالميتويلاشن وسم ASCT2 وتكسيره، مما يؤدي إلى مستويات أعلى من بروتين ASCT2 وزيادة في امتصاص الجلوتامين، دون تغيير نشاط الجين الأساسي.
إنزيم معاكس يحمي البوابة
مقابل ZDHHC14 يوجد إنزيم آخر، ABHD17B، يزيل الوسم الدهني عن ASCT2. عندما يكون ABHD17B نشطًا، يقل بالميتويلاشن على ASCT2، ويصبح أكثر استقرارًا وأكثر احتمالاً أن يُعاد تدويره إلى سطح الخلية بدلاً من إرساله إلى الليزوزوم. هذا التأشير وإزالته يشبهان مقبضًا مضبوطًا بدقة على تدفق الجلوتامين: يدفع ZDHHC14 ASCT2 نحو التحلل، بينما ينقذه ABHD17B ويحافظ على نقل الجلوتامين. في خلايا سرطان الرئة، يؤدي تحريك هذا التوازن نحو تقليل البالميتويلاشن إلى زيادة امتصاص الجلوتامين ودعم نمو الورم في الأطباق وفي الفئران.
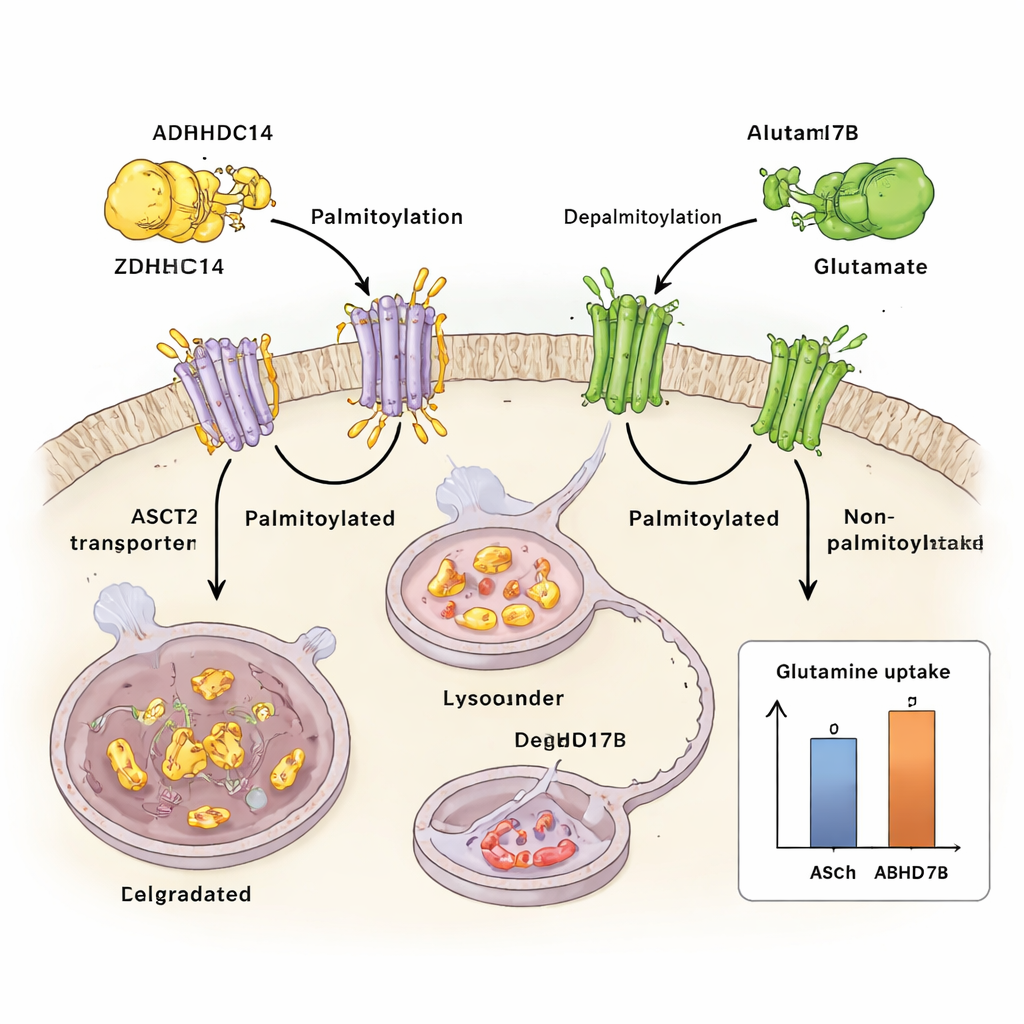
كيف يعيد إجهاد المغذيات برمجة النظام
اختبر الفريق ما يحدث عندما تنفد مخزونات الجلوتامين في الخلايا الورمية. تحت حرمان الجلوتامين، يتنشط بروتين إشارات حساس للإجهاد يُدعى JNK1. يرتبط JNK1 فعليًا بـ ZDHHC14 ويضيف مجموعة فوسفات في موقع محدد (Thr440)، مما يعلّم ZDHHC14 ليُرسل إلى التحلل في الليزوزوم. مع انخفاض مستويات ZDHHC14، يتلقى ASCT2 عددًا أقل من وسوم البالميتويلاشن، يفلت من التفكيك، ويتراكم على سطح الخلية — تمامًا عندما تحتاج الخلية إلى انتشال الجلوتامين النادر. يؤدي تغيير هذا الموقع الواحد الحساس لـ JNK1 إلى تثبيت ZDHHC14، واستعادة وسم ASCT2، وتقليل امتصاص الجلوتامين، مما يؤكد مدى انسداد إجهاد المغذيات في حلقة التحكم هذه.
ترجمة الآلية إلى علاج
بما أن ASCT2 مهم جدًا لأيض الورم، تُستكشف أدوية تحجبه، مثل المركب التجريبي V9302، كعلاجات محتملة للسرطان. تكشف هذه الدراسة أن إشارة JNK1 يمكن أن تعاكس تدمير ASCT2، فعليًا تحمي بوابة الجلوتامين. في نماذج خلوية ونماذج فئران لسرطان الرئة غير صغير الخلايا، أدى دمج مثبط JNK مع V9302 إلى تقليل امتصاص الجلوتامين ونمو الخلايا الورمية وحجم الورم أشد من أي دواء بمفرده. تُظهر عينات المرضى والمجموعات البيانية العامة أيضًا أن انخفاض ZDHHC14 وارتفاع ASCT2 شائعان في NSCLC ويرتبطان ببقاء أسوأ، ما يشير إلى أن هذا النمط الجزيئي قد يساعد في تحديد المرضى الأكثر احتمالاً للانتفاع من استهداف هذا المسار.
ماذا يعني هذا للمرضى
بعبارات بسيطة، تُظهر هذه النتائج أن بعض سرطانات الرئة تتحكم في وقودها المفضل عن طريق ضبط صمام جزيئي على سطحها. تحدد ثلاثيّة عوامل — JNK1 و ZDHHC14 و ABHD17B — ما إذا كان ناقل الجلوتامين ASCT2 سيُوسم للتدمير أم سيُترك مفتوحًا. عندما يكون الجلوتامين نادرًا، يتحول النظام للحفاظ على ASCT2 ومواصلة تدفق الوقود، مما يساعد الأورام على النجاة في ظروف قاسية. من خلال حجب ASCT2 ومسار JNK الذي يحميه معًا، تمكن الباحثون من تجويع الخلايا السرطانية بشكل أكثر فعالية في نماذج مخبرية وحيوانية. ورغم الحاجة لمزيد من الاختبارات، يقدم محور الفسفرة–البالميتويلاشن هذا زاوية واعدة لتطوير علاجات تقطع خطوط حياة المغذيات للأورام الشرهة للجلوتامين.
الاستشهاد: Chen, X., Ke, Z., Wei, S. et al. ASCT2 palmitoylation regulated by JNK1-ZDHHC14 axis orchestrates glutamine metabolism and NSCLC progression. Cell Discov 12, 13 (2026). https://doi.org/10.1038/s41421-026-00870-z
الكلمات المفتاحية: أيض الجلوتامين, سرطان الرئة غير صغير الخلايا, ناقلة ASCT2, بالميتويلاشن البروتين, إشارة JNK