Clear Sky Science · ar
الآليات الجزيئية والآثار العلاجية المحتملة للتفاعل الثنائي بين مثيلة الـDNA وإعادة برمجة الأيض في سرطان الغدة الدرقية
لماذا يهم هذا البحث خارج المختبر
يُعد سرطان الغدة الدرقية من أسرع السرطانات ارتفاعًا عالمياً. وبينما تُعالج العديد من الحالات بشكل جيد، فإن الأنواع الأكثر عدوانية غالبًا ما تتوقف عن الاستجابة لليقينيوم المشع، وهو علاج أساسي، مما يترك المرضى مع خيارات محدودة. تشرح هذه المقالة الاستعراضية كيف يتعاون عاملان غير مرئيين داخل الخلايا — العلامات الكيميائية على الـDNA والتغيرات في كيفية استخدام الخلايا السرطانية للوقود — لدفع نمو سرطان الغدة الدرقية ومقاومته للعلاج. يمكن أن يفتح فهم هذه الشراكة المخفية الباب أمام علاجات أكثر دقة وثباتًا.
كيف تعيد الخلايا السرطانية كتابة دليلها الإرشادي
تحمل كل خلية نفس الـDNA، لكن العلامات الكيميائية المسماة مجموعات ميثيل يمكنها تشغيل أو إيقاف الجينات دون تغيير الشفرة الوراثية نفسها. في سرطان الغدة الدرقية، تكون هذه «العلامات» على الـDNA مشوهة بشكل عميق. تفقد مناطق واسعة من الجينوم علامات الميثيل، مما قد يزعزع استقرار الكروموسومات، بينما تُثقل علامات الميثيل على المكابح الأساسية للنمو ووظيفة الغدة الدرقية وتُسكتها. وتشمل هذه جينات كابحة للأورام وجينات خاصة بالدرقية تساعد عادة الخلايا على امتصاص اليود. النتيجة كتاب إرشادي جيني تُطمس فيه فصول الأمان، مما يشجع على نمو غير منضبط وفقدان الهوية الدرقية الطبيعية.
كيف تعيد الخلايا السرطانية توصيل خطوط الوقود
في الوقت نفسه، تعيد خلايا الورم الدرقي صياغة طرق الحصول على الطاقة واستخدامها. بدلاً من الاعتماد أساسًا على احتراق الوقود بكفاءة في الميتوكوندريا، تتجه بشدة نحو تفكيك السكر السريع لكن المهدِر، مولدة منتجات حمضية تساعدها على التهرب من جهاز المناعة. كما تزيد من تصنيع وحرق الدهون، وتعيد توجيه الأحماض الأمينية مثل السيرين والجلوتامين لدعم الانقسام السريع. هذه التغييرات ليست عشوائية: يقودها إشارات محفزة للسرطان وتُنشئ شبكة أيضية مرنة تسمح للخلايا الورمية بالبقاء في ظروف نقص الأكسجين، ومقاومة الأدوية، والنمو في مواقع جديدة.
حركة ثنائية الاتجاه بين علامات الـDNA والأيض الخلوي
الرسالة المركزية في المقال هي أن وسم الـDNA واستخدام الوقود ليسا قصتين منفصلتين—هما يشكلان حلقة تغذية راجعة تعزز نفسها. من جهة، ينتج أيض الخلايا الورمية جزيئات صغيرة محددة تعمل كمفاتيح للإنزيمات التي تضيف أو تزيل مجموعات الميثيل على الـDNA. عندما تتغير مستويات هذه الجزيئات، يمكن أن تدفع الجينوم نحو مزيد أو أقل من المثيلة في مواقع حساسة. ومن جهة أخرى، يمكن لمثيلة الـDNA أن تسكت مباشرة أو تعزز جينات تتحكم في استخدام السكر والتعامل مع الدهون ونقل الأحماض الأمينية. مع مرور الوقت، تقفل حركة المرور الثنائية هذه حالة ملائمة للسرطان حيث تقوي العلامات غير الطبيعية على الـDNA والأيض المشوه بعضهما بعضًا باستمرار.
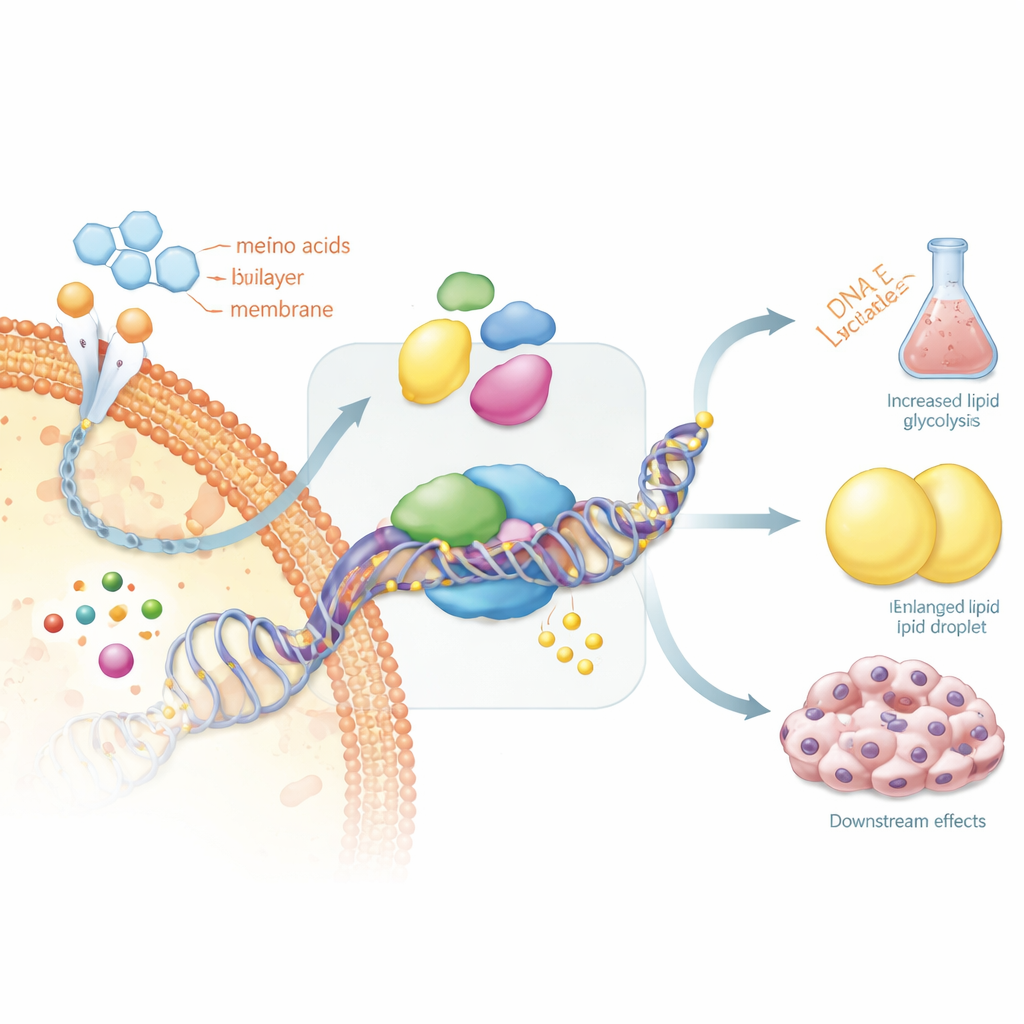
لماذا بعض سرطانات الغدة الدرقية تتوقف عن امتصاص اليود
لهذه الحلقة ردود فعل عملية مهمة للمرضى. يعمل علاج اليود المشع فقط إذا احتفظت خلايا الورم بالآليات الجزيئية اللازمة لسحب اليود إلى الداخل. تبرز المراجعة أن الجينات الدرقية الرئيسية المسؤولة عن ذلك، بما في ذلك مستقبل الهرمون المنشط للغدة الدرقية وناقلة الصوديوم–اليود، غالبًا ما تُغلق بواسطة وسم ميثيل كثيف في مناطق التحكم بها. بمجرد حدوث ذلك، «تنسى» الخلايا السرطانية أنها خلايا درقية ولا تمتص اليود، مما يجعل العلاج القياسي يفشل. يقترح المؤلفون أن قلب هذه العلامات على نحو مدروس، أو حجب المسارات الأيضية التي تدعمها، قد يعيد قابلية امتصاص اليود ويسترجع الحساسية للعلاج.
أفكار علاجية جديدة مبنية على رؤية متكاملة
نظرة إلى سرطان الغدة الدرقية كمرض يعبر محور «مثيلة الـDNA–الأيض» تقود إلى استراتيجيات علاجية جديدة. بدلاً من الاعتماد على دواء واحد، يجادل المؤلفون لصالح نهج تركيبي يستهدف عدة أجزاء من الحلقة في آن واحد—أدوية وصفائية (إيبيجينية) ترفع القيود الضارة على الـDNA، وأدوية أيضية تقطع مسارات الوقود الأساسية، وأدوية مانعة للإشارات تُقلل من المسارات الدافعة للسرطان. قد تضيف العلاجات المناعية الحديثة وأنظمة توصيل الدواء المتقدمة، مثل الجزيئات النانوية الذكية، مزيدًا من التوازن عن طريق إعادة تشكيل بيئة الورم المناعية مع تقليل الآثار الجانبية. تشير بيانات مخبرية وسريرية مبكرة إلى أن مثل هذه الهجمات المنسقة قد تُبطئ المرض، وتستعيد امتصاص اليود المشع لدى بعض المرضى، وتؤخر ظهور المقاومة.
ما الذي يعنيه هذا للرعاية المستقبلية
بالنسبة للقارئ العام، الخلاصة هي أن سرطانات الغدة الدرقية العدوانية قد تُشفى ليس بالبحث عن طلقة سحرية واحدة، بل بفهم وتعطيل الحلقة الخبيثة بين وسم الـDNA وأيض الخلية. من خلال رسم خريطة هذا المحور بتفصيل وتتبع هذه التغيرات في عينات الدم والأورام، قد يتمكن الأطباء يومًا من مضاهاة المرضى بمجموعات علاجية مخصصة تجمع بين العلاجات الإيبيجينية والأيضية والمستهدفة والمناعية. إذا نجح ذلك، فقد تحول هذه المقاربة المتكاملة أكثر أنواع سرطان الغدة الدرقية عنادًا إلى حالات يمكن علاجها مرة أخرى—وربما تمنع تحولها إلى أشكال عدوانية من الأساس.
الاستشهاد: Zhang, T., Han, H., Zhang, Y. et al. The molecular mechanisms and potential therapeutic implications of the crosstalk between DNA methylation and metabolic reprogramming in thyroid cancer. Cell Death Discov. 12, 110 (2026). https://doi.org/10.1038/s41420-026-02981-8
الكلمات المفتاحية: سرطان الغدة الدرقية, مثيلة الـDNA, أيض السرطان, مقاومة اليود المشع, العلاج المستهدف