Clear Sky Science · ar
تثبيط HSP27 ينشط تداخل XBP1s/CerS1، مما يثير البلعمة الميتوكوندرية المدفوعة بـ DRP1، وبالتالي يحمي من موت الخلية ويعزز دورة التكاثر الحياتية لـ KSHV في خلايا الليمفوما الانصبابية الأولية
عندما يصبح إجهاد الخلية سيفًا ذا حدين
تنجو خلايانا من الإهانات اليومية بتشغيل برامج طوارئ تصلح الأضرار وتحافظ على بقائها. لكن الخلايا السرطانية قد تختطف هذه البرامج نفسها لتنمو ولتحمي الفيروسات الكامنة بداخلها. تستعرض هذه المقالة كيف يؤدي حجب بروتين واحد واقٍ من الإجهاد في نوع نادر من الليمفوما ليس فقط إلى دفع الخلايا الورمية نحو الموت، بل يمنح أيضًا فيروسًا مخفيًا بداخلها نافذة للاستيقاظ والتكاثر. فهم هذا التوازن الدقيق قد يساعد في تصميم علاجات تقتل السرطان مع حرمان الفيروس من فرصة الانتشار.
فيروس مخفي في ليمفوما عدوانية
الليمفوما الانصبابية الأولية هي سرطان عدواني للغاية للخلايا البائية، نوع من خلايا الدم البيضاء. تحمل معظم هذه الخلايا الورمية راكبًا خامدًا: فيروس الهربس المرتبط بساركوما كابوزي (KSHV). في حالته الهادئة أو الكامنة، ينتج الفيروس عددًا قليلاً من البروتينات ويختبئ داخل جينوم العائل. بعض أشكال الإجهاد يمكن أن تدفعه إلى طور نشط، أو طليعي، يعيد فيه نسخ نفسه ويُنتج جزيئات فيروسية جديدة، عادةً ما تقتل الخلية المضيفة. تعتمد الخلايا الورمية نفسها على عدة أنظمة استجابة للإجهاد، بما في ذلك ما يسمى ببروتينات الصدمة الحرارية واستجابة البروتين المتعرج، التي تساعدها على التعامل مع البروتينات المطوية بشكل خاطئ واضطراب أيض الدهون، وكذلك الضرر في الميتوكوندريا منتجة الطاقة. 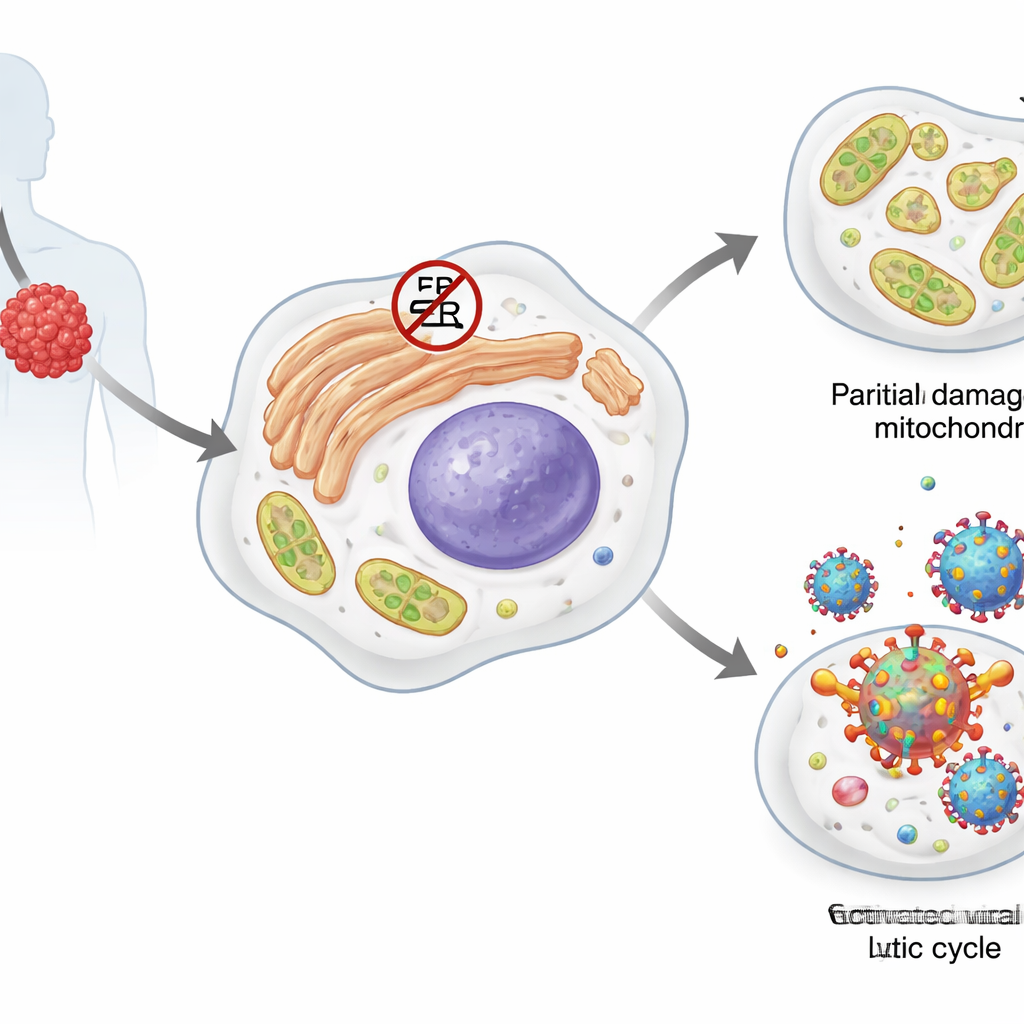
حجب حارس خلوي
ركز الباحثون على HSP27، وهو بروتين صدمة حرارية صغير معروف بحمايته للخلايا من الإجهاد. باستخدام مثبط كيميائي يُدعى J2 أو عن طريق إسكات الجين باستخدام حمض نووي صغير ريبوزي، قللوا من نشاط HSP27 في خلايا الليمفوما المزروعة مخبريًا. جعل ذلك الخلايا أقل قدرة على البقاء وأثار إشارة إجهاد قوية في شبكة غشائية داخلية تُسمى الشبكة الإندوبلازمية. ارتفعت مؤشرات هذه الاستجابة، بما في ذلك عوامل وقائية ومحفزة للموت، وتفعل مفتاح مهم يسمى XBP1s. وفي الوقت نفسه، أظهرت الخلايا علامات متزايدة للموت المبرمج، مما يؤكد أن إزالة HSP27 تدفعها نحو نقطة توازن بين البقاء والانهيار.
حلقة إجهاد تتواصل مع دهون الخلية
يرتبط الإجهاد في الشبكة الإندوبلازمية ارتباطًا وثيقًا بكيفية تعامل الخلايا مع الدهون. وجدت المجموعة أن حجب HSP27 زاد مستويات CerS1، وهو إنزيم يصنع جزيء دهني محدد يسمى سيراميد C18. عندما حجبوا كيميائيًا XBP1s، اختفى ارتفاع CerS1، مما أظهر أن XBP1s يساعد على تشغيل جين CerS1 في هذه الظروف. اللافت أن تثبيط CerS1 بدوره خفَّض XBP1s، كاشفًا عن حلقة تغذية راجعة إيجابية: كل عامل يدعم الآخر. هذه المصافحة الجزيئية لا تعيد تشكيل أيض الدهون فحسب، بل تقوّي أيضًا قدرة الخلية على التكيّف مع إجهاد الشبكة الإندوبلازمية، حتى مع تراكم إشارات الموت.
إعادة تدوير الميتوكوندريا بدلًا من تدميرها
غالبًا ما ينتقل الإجهاد في جزء من الخلية إلى الميتوكوندريا، مصانع الطاقة الصغيرة المنتجة للطاقة. بعد حجب HSP27، أنتجت خلايا الليمفوما المزيد من أنواع الأكسجين التفاعلية، علامة على خلل ميتوكوندري، وزادت مستويات DRP1، وهو بروتين يقطع الميتوكوندريا إلى أجزاء أصغر. أظهر المؤلفون أن حلقة XBP1s–CerS1 كانت مسؤولة عن رفع مستوى DRP1. هذا بدوره أثار البلعمة الميتوكوندرية، عملية رقابة نوعية تُحبس فيها الميتوكوندريا التالفة في أغشية وتُرسل إلى "مراكز إعادة التدوير" الخلوية المسماة الليزوزومات. باستخدام صبغات فلورية وعلامات بروتينية، أكدوا أن الميتوكوندريا كانت تُزال انتقائيًا. عندما عطلوا DRP1 كيميائيًا أو وراثيًا، تقلصت هذه البلعمة الميتوكوندرية وماتت الخلايا بسهولة أكبر، ما يعني أن إعادة تدوير الميتوكوندريا كانت فعلاً تساعد الخلايا الورمية المتعبة على البقاء.
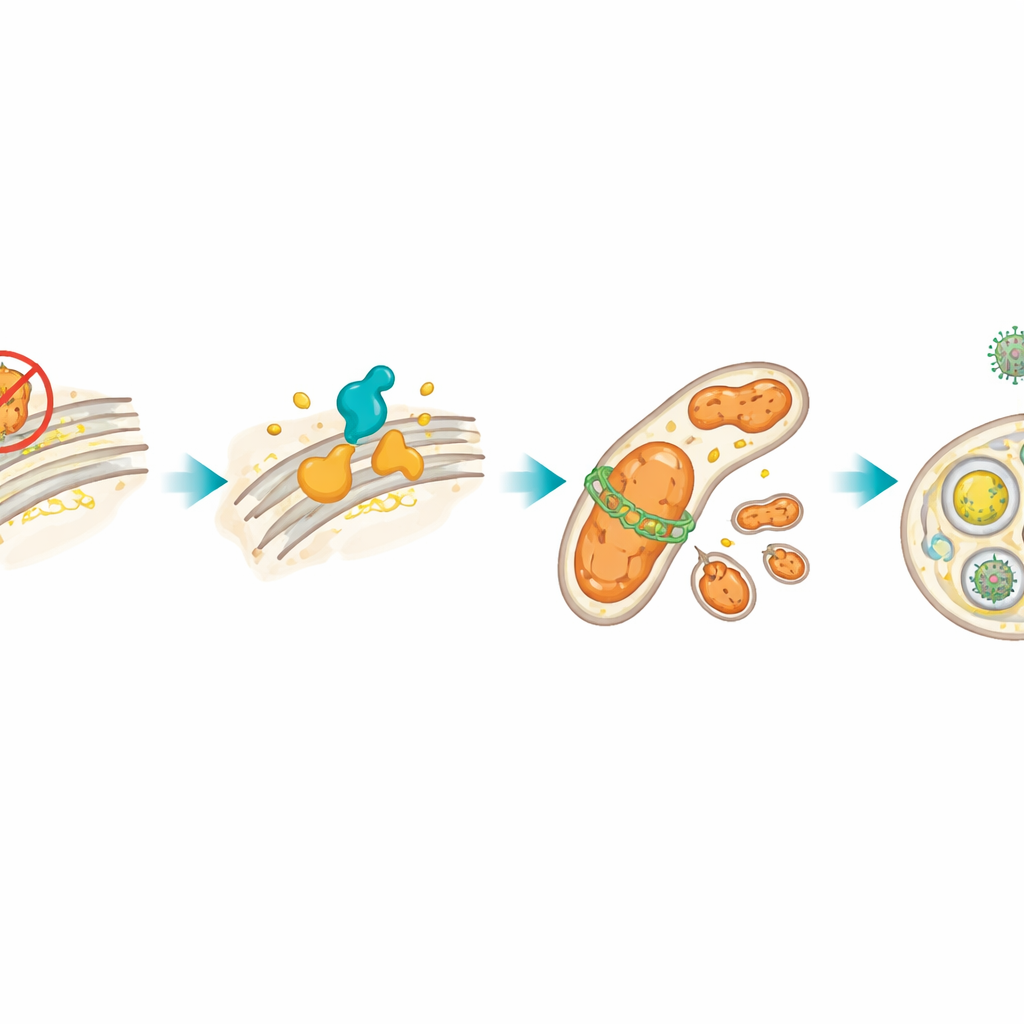
منح الفيروس وقتًا للهروب
البلعمة الميتوكوندرية نفسها التي حمت الخلايا الورمية أفادت أيضًا KSHV. رُبط تنشيط XBP1s وتراكم سيراميد C18 وزيادة انشطار الميتوكوندريا بإعادة إيقاظ هذا الفيروس. هنا، عندما حُجب HSP27، عبرت خلايا أكثر عن بروتينات فيروسية مبكرة ومتأخرة، وهي علامات واضحة للتكاثر الطليعي. أدى حجب DRP1، وبالتالي البلعمة الميتوكوندرية، إلى تقليل هذا إعادة التنشيط الفيروسي. يقترح المؤلفون أن البلعمة الميتوكوندرية، من خلال إطالة بقاء الخلية قليلاً تحت الإجهاد، تمنح KSHV الوقت لإكمال دورة تكاثره ومغادرة الخلية المحتضرة، ما قد يؤدي إلى إصابة أهداف جديدة والمساهمة في تطور السرطان.
ماذا يعني هذا للعلاجات المستقبلية
بالنسبة لغير المتخصص، الرسالة الأساسية هي أن HSP27 يعمل كمراقب مركزي لكيفية تعامل خلايا الليمفوما مع الإجهاد، وكيف يعيدون تدوير الميتوكوندريا التالفة، وكيف يقرر فيروس مرتبط بالسرطان متى يستيقظ. إيقاف HSP27 يطلق سلسلة من الأحداث تُقوّض بقاء الخلية وفي الوقت نفسه تحميها مؤقتًا عبر البلعمة الميتوكوندرية بينما تسمح لـ KSHV بالتكاثر. من الناحية العلاجية، قد يدفع الجمع بين تثبيط HSP27 والأدوية التي تمنع البلعمة الميتوكوندرية المدفوعة بـ DRP1 الخلايا الورمية إلى الموت بسرعة أكبر ويقيد فرصة الفيروس للانتشار، مما يوفر استراتيجية مزدوجة ضد هذه الليمفوما القاتلة.
الاستشهاد: Gonnella, R., Corrado, V., Scaffidi, G.F. et al. Inhibiting HSP27 activates the XBP1s/CerS1 interplay, which triggers DRP1-driven mitophagy, thereby protecting against cell death and promoting the KSHV lytic cycle in primary effusion lymphoma cells. Cell Death Discov. 12, 118 (2026). https://doi.org/10.1038/s41420-026-02979-2
الكلمات المفتاحية: الليمفوما الانصبابية الأولية, فيروس ساركوما كابوزي, استجابة إجهاد الخلية, البلعمة الميتوكوندرية, بروتين الصدمة الحرارية HSP27