Clear Sky Science · ar
محور AdipoR1–AMPK يثبط سرطان الثدي عبر الأنواع الجزيئية من خلال مسارات متعددة لموت الخلايا، بما في ذلك الفرورفوتوس والخلايا المبرمجة
لماذا تهم خلايا الدهون في سرطان الثدي
معظمنا يظن أن دهون الجسم مخزن للطاقة فقط، لكن خلايا الدهون هي مصانع نشطة تُفرِج هرمونات وجزيئات إشارية إلى مجرى الدم. تستكشف هذه الدراسة كيف أن أحد تلك الإشارات المشتقة من الدهون، عبر جزيء يُدعى AdipoR1 على خلايا سرطان الثدي، يمكنه إبطاء نمو الورم. تكمن أهمية العمل في أنه يقترح نهجاً جديداً لعلاج أشكال متعددة من سرطان الثدي من خلال استغلال التواصل بين نسيج الدهون والأورام، مما قد يعزز تأثير الأدوية الحالية.
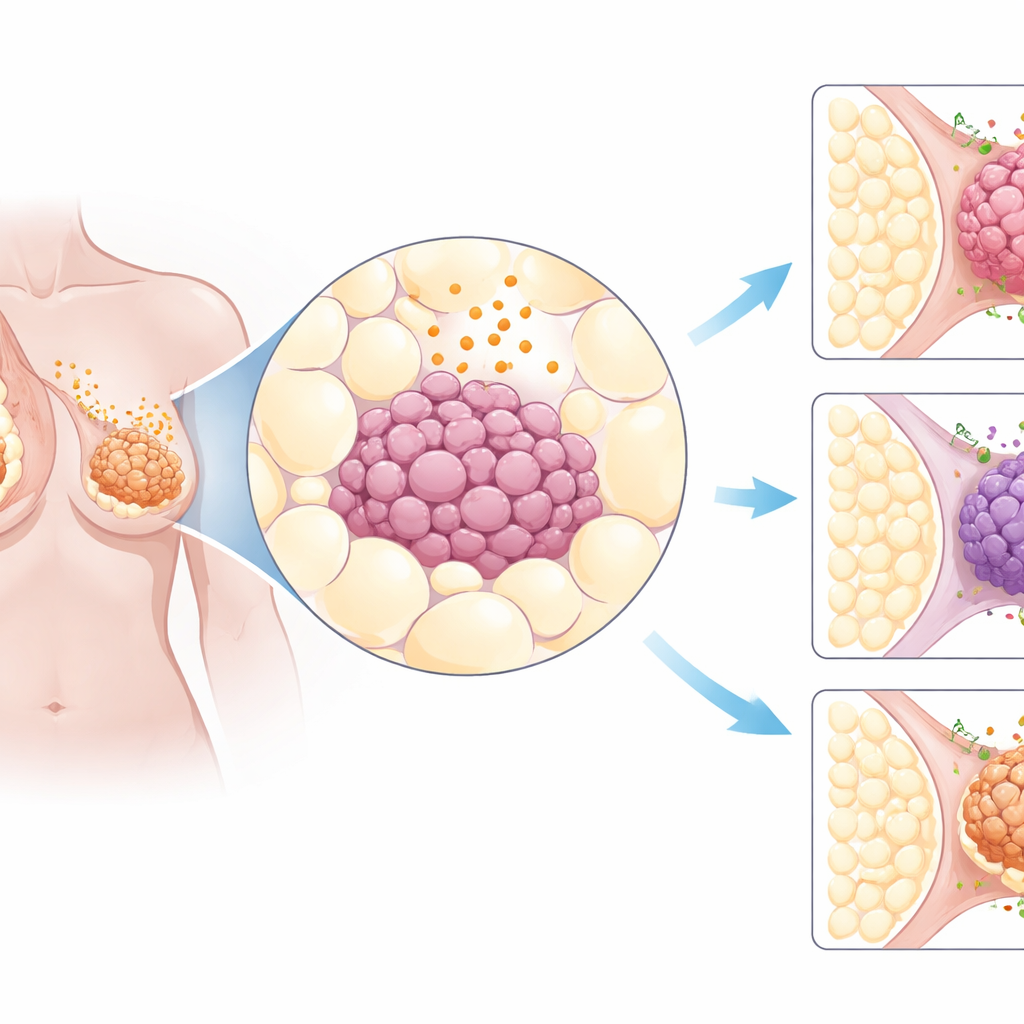
نظرة عبر أنواع عديدة من السرطان
بدأ الباحثون بالتنقيب في قواعد بيانات سرطانية عامة كبيرة تحتوي على معلومات وراثية من آلاف أورام المرضى. ركزوا على نحو ثلاثين جيناً معنيّاً بالإشارات القادمة من نسيج الدهون والهياكل الخلوية التي تستقبل هذه الإشارات. عند مقارنة الأورام من 31 عضوًا مختلفًا بالنسيج السليم، برز نمط واحد بوضوح: أظهر سرطان الثدي تغيرات قوية بشكل خاص في هذه الإشارات المرتبطة بالدهون. وعلى وجه الخصوص، كان مستقبل AdipoR1 متواجداً بمستويات أعلى من المعتاد في أورام الثدي، بغض النظر عما إذا كانت مدفوعة بالهرمونات، أو إيجابية HER2، أو النوع الثلاثي السلبية الأكثر عدوانية. أكدت عينات الأنسجة من أكثر من 600 حالة سرطان ثدي وجود بروتين AdipoR1 على نطاق واسع في خلايا الورم.
اختبار دواء إشارة دهنية على خلايا السرطان
لمعرفة ما يفعله AdipoR1 داخل الأورام فعلياً، لجأ الفريق إلى خطوط خلايا سرطان الثدي المزروعة في المختبر، والتي تمثل عدة أنواع شائعة. عالجوا هذه الخلايا بـ AdipoRon، جزيء صغير يُفعل AdipoR1. سرعان ما حفّز AdipoRon مفتاح استشعار الطاقة المعروف داخل الخلايا المسمى AMPK، مما أظهر أن الإشارة وصلت إلى داخل الخلية. مع زيادة جرعة AdipoRon، انقسمت الخلايا السرطانية بوتيرة أبطأ، وحركتها تقلصت في اختبارات شفاء الجروح، ومرّ كثير منها بعملية انتحار مبرمجة. عندما قلل الباحثون عمدًا من مستويات AdipoR1 في الخلايا، فقد AdipoRon كثيراً من تأثيره، في حين أن تعزيز AdipoR1 جعل الدواء أكثر فعالية، رابطين التأثير مباشرة بهذا المستقبل.
طرق متعددة لدفع خلايا السرطان نحو الموت
من خلال تحليل نشاط الجينات بعد المعالجة، وجد العلماء أن AdipoRon أطلق استجابات إجهاد داخل خلايا سرطان الثدي. فعّل جينات مرتبطة بموت الخلايا المبرمج التقليدي وكذلك تلك المشاركة في شكل أحدث من تدمير الخلايا المعتمد على الحديد يُسمى الفرورفوتوس (ferroptosis). ارتفعت العلامات الرئيسة لهذه العملية على مستوى الحمض النووي الريبوزي والبروتين، لا سيما في خلايا سرطان الثدي الحساسة للهرمونات، ودعمت قراءات كيميائية أضرار شحميات الخلايا هذا الاكتشاف. في الوقت نفسه، خفّض AdipoRon مستويات بروتينات تساعد الخلايا السرطانية عادة على البقاء، بما في ذلك مساعدات إصلاح الحمض النووي (BRCA1 وBRCA2)، ومستقبل الاستروجين الذي يدفع نمو العديد من الأورام، وTROP2، وهو جزيء سطحي مرتبط بالسلوك العدواني.
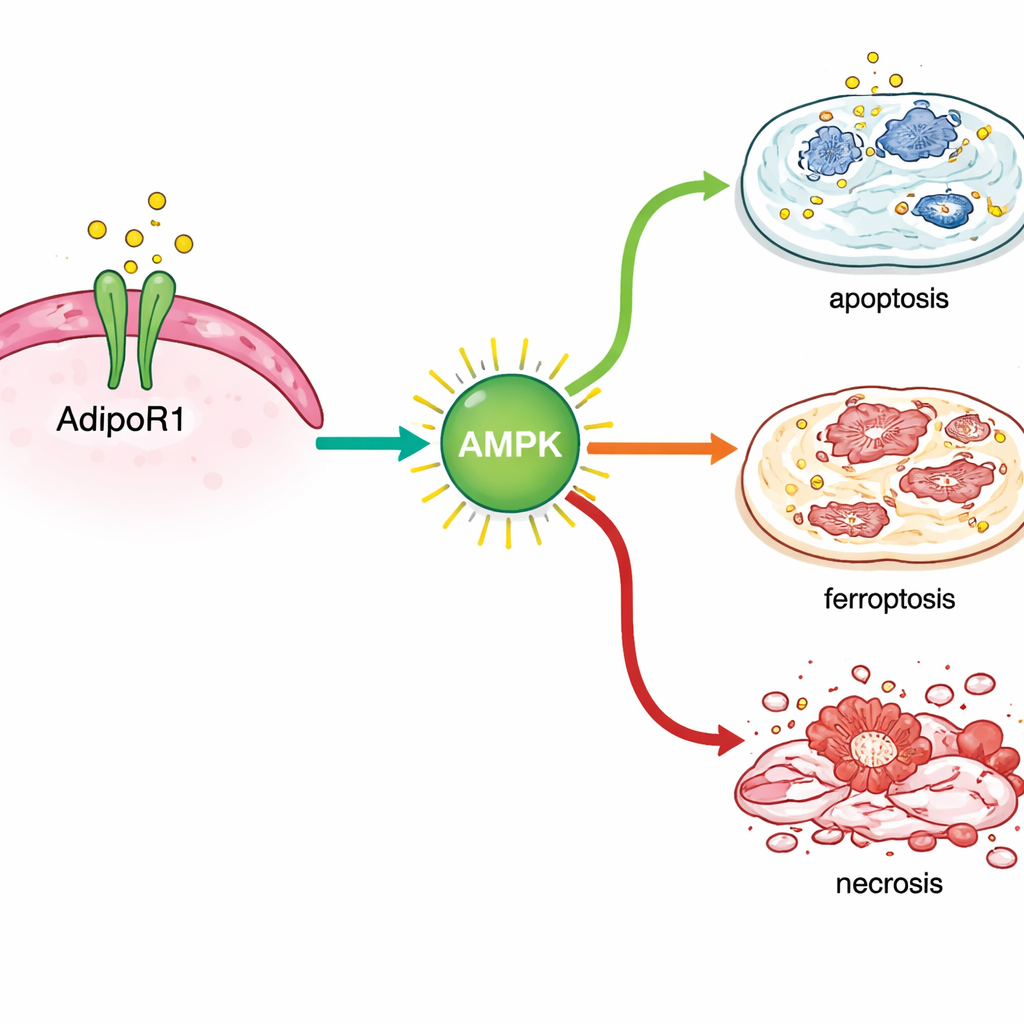
العمل مع العلاجات الحالية لا ضدها
ثم تساءل الفريق عما إذا كان تفعيل AdipoR1 يمكن أن يُكمّل الأدوية القياسية. في خلايا سرطان الثدي الحساسة للهرمونات، أنتج الجمع بين AdipoRon وتاموكسيفين قمعاً للنمو أكبر من أي دواء بمفرده. في خطوط الثلاثية السلبية، عزّز AdipoRon تأثيرات عوامل العلاج الكيميائي الشائعة مثل باكليتاكسيل ودوكسوروبيسين. عند الانتقال إلى الفئران الحاملة لأورام ثدي حساسة للهرمونات، أعطى الباحثون AdipoRon عن طريق الفم. نمت الأورام في الحيوانات المعالجة بوتيرة أبطأ واحتوت على مناطق موت أكبر عند فحصها بالمجهر. والأهم أن الفئران لم تظهر آثاراً جانبية واضحة في السلوك أو الوزن أو صحة الكبد خلال فترة المعالجة.
ماذا قد يعني ذلك للمرضى
تشير النتائج مجتمعة إلى أن تفعيل AdipoR1 في خلايا سرطان الثدي يُشغل عدة طرق متداخلة لموت الخلايا بينما يضعف أنظمة بقاء رئيسية، وأن هذا النهج يعمل عبر أشكال وراثية مختلفة للمرض. بدلاً من استبدال العلاجات الحالية، يمكن أن تعمل أدوية تستهدف AdipoR1 مثل AdipoRon كمكمِّلات تجعل الأورام أكثر عرضة للعلاج الهرموني أو الكيميائي أو للعوامل الموجهة المستقبلية. قبل أن يصل هذا الاستراتيجية إلى العيادة، سيحتاج الباحثون إلى تطوير منشّطات أكثر فاعلية وانتقائية لـ AdipoR1، وتوضيح أي مرضى تعبر أورامهم عن المستقبل بقوة أكبر، وتقييم السلامة بدقة. ومع ذلك، يشير هذا العمل إلى فكرة جذابة: يمكن إعادة توجيه إشارات نسيج الدهون في أجسامنا لمساعدة مكافحة سرطان الثدي بدلاً من تغذيته.
الاستشهاد: Sato, S., Yamanaka, T., Komori, Y. et al. AdipoR1–AMPK axis suppresses breast cancer across molecular subtypes via multimodal cell death pathways, including ferroptosis and apoptosis. Cell Death Dis 17, 384 (2026). https://doi.org/10.1038/s41419-026-08583-7
الكلمات المفتاحية: سرطان الثدي, الهرمونات الدهنية, AdipoR1, مسارات موت الخلايا, استقلاب السرطان