Clear Sky Science · ar
استهداف طفرات p53 السرطانية Y220C وY220N وY220S بمثبّت جزيئي صغير ريزاتابوبت
لماذا يهم هذا لعلاجات السرطان المستقبلية
غالبًا ما يعطل السرطان بروتين p53، الذي يُطلق عليه أحيانًا «حارس» الخلية، عن طريق تحويره بحيث لا يعود قادرًا على ضبط الخلايا الضارة. تغيير واحد محدد في p53، يُعرف باسم Y220C، شائع في الأورام الصلبة وأصبح نموذجًا لاختبار أدوية تهدف إلى إصلاح p53 المعطوب بدلاً من قتل الخلايا مباشرة. هذه الدراسة تطرح سؤالًا عمليًا يركز على المريض: هل يمكن لدواء تجريبي واعد، ريزاتابوبت، وهو قيد التجارب السريرية لطرائق Y220C، أن يفيد أيضًا الأشخاص الذين تحمل أورامهم طفرات قريبة ولكنها أندر في نفس الموضع من p53؟
دواء مصمَّم لسَدّ شقّ في p53
تجعل العديد من طفرات p53 البروتين يتفتح ويفقد شكله الدقيق. في طفرة Y220C، يُنشئ التغيير تجويفًا صغيرًا على سطح البروتين—عيبًا أدرك الكيميائيون أنه يمكن «سدّه» بجزيئات صغيرة مصممة لتثبيت p53. ريزاتابوبت هو أحد هذه الجزيئات، وطُوّر بالاستفادة من سلسلات كيميائية سابقة ترتبط بهذا التجويف وتعمل كدعامة جزيئية. يركز المؤلفون على طفرتين أخريين في نفس موضع الحمض الأميني، Y220S وY220N، اللتين تنحتان جيبًا مشابهًا لكنهما تزعزعان استقرار p53 أكثر من Y220C. إذا أمكن لريزاتابوبت سدّ هذه المتغيرات أيضًا، فقد يوسّع هذا النهج في الطب الدقيق نطاق الفائدة ليشمل آلاف المرضى سنويًا. 
قياس مدى تمسّك ريزاتابوبت وتثبيته لـ p53 المتحوّر
لاختبار ذلك، نقّى الفريق النواة الملتصقة بالحمض النووي من p53 الحاملة لتغيرات Y220C أو Y220S أو Y220N وعرض كلًّا منها لِريزاتابوبت (ولأقارب كيميائية قريبة). باستخدام اختبارات معتمدة على الحرارة، أظهروا أن جميع البروتينات المتحوّرة الثلاثة أصبحت أكثر استقرارًا عند ارتباط الدواء، مع استعادة Y220C وY220S متانة شبيهة بالنمط البري بفعالية. بالمقابل، استعادت Y220N جزءًا فقط من استقرارها المفقود. تكشف تقنية ثانية تقيس الحرارة المنبعثة عند الالتحام عن السبب: يلتصق ريزاتابوبت بقوة كبيرة بـY220C (في نطاق عشرات النانومولار)، وبقوة أقل قليلًا بـY220S، وبقوة أضعف بعد لـY220N، مع بقاء القيم ضمن نطاقات يعتبرها الكيميائيون الدوائيون واعدة.
رؤية الرقعة الجزيئية بتفاصيل ذرية
قدّمت هياكل بلورية بالأشعة السينية عالية الدقة تفسيرًا بصريًا. في جميع الطفرات الثلاث، يستقر ريزاتابوبت داخل الشق الناتج عن الطفرة بوضع محافظ: يلملم الهيكل المركزي التجويف، يصل أحد طرفيه عميقًا إلى الجيب مع مجموعة من ذرات الفلور، ويتفاعل الطرف الآخر مع حلقة بروتينية مجاورة. يشكل الدواء شبكة من الاتصالات، بما في ذلك ذرة فلور موضوعة استراتيجيًا تتفاعل مع العمود الفقري للبروتين. في حالة Y220S، تُحافظ هذه التداخلات مع انزياحات طفيفة فقط، مما يسمح بتثبيت قوي. أما في Y220N، فإن ارتباط الدواء يجبر جانب السلسلة الأسبراجين إلى نواة بروتينية دهنية بطريقة غير ملائمة طاقةً، وتُفقد بعض الاتصالات مع «مرساة» الدواء المفلورة. هذا الملاءمة المشدودة تفسّر كلًا من الارتباط الأضعف وعدم الإنقاذ الكامل للاستقرار. 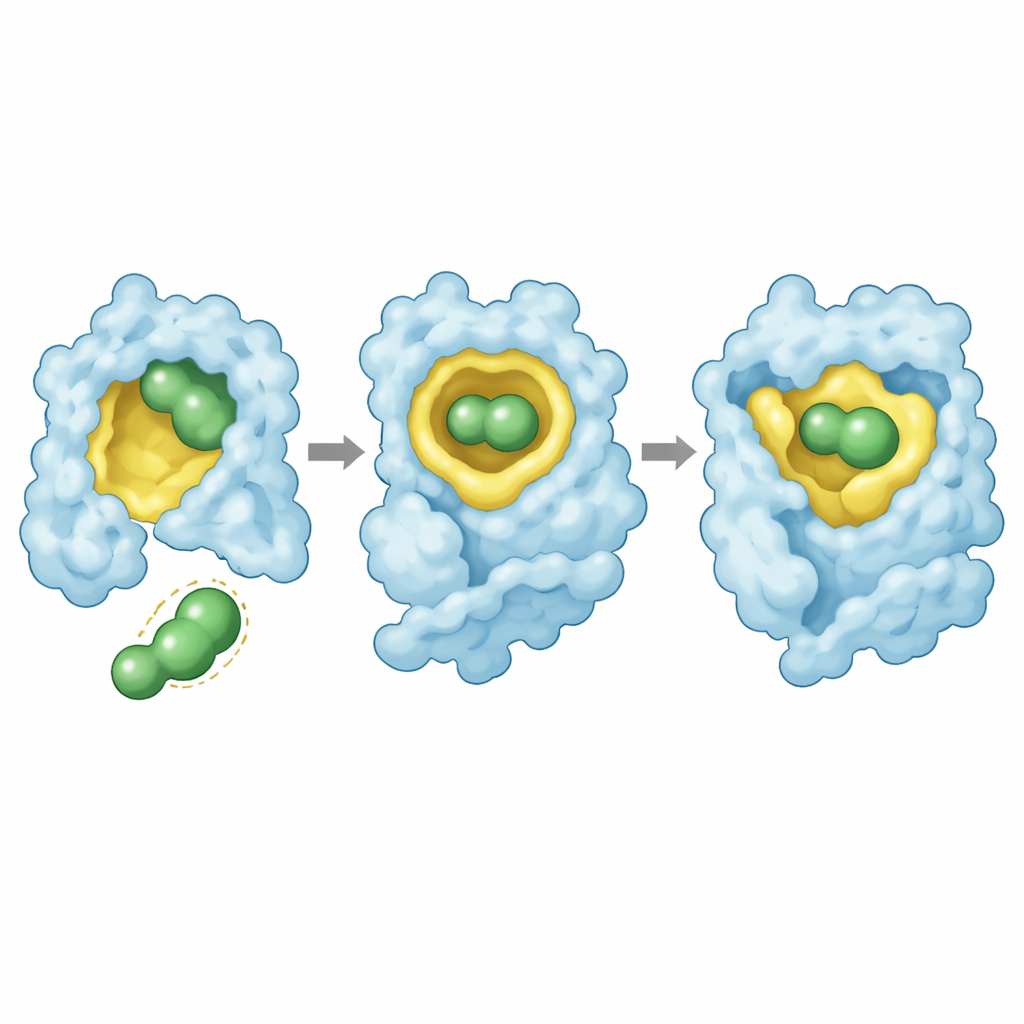
من إصلاح البروتين إلى سلوك الخلية
الاختبار الحاسم هو ما إذا كان مثل هذا التثبيت يعيد دور p53 الحامي داخل الخلايا الحية. مهَّد الباحثون خلايا سرطان الرئة الخالية من p53 الطبيعي لتُعبر إما المتغيرات Y220C أو Y220S أو Y220N أو Y220H. عند المعالجة بريزاتابوبت، أظهرت الخلايا الحاملة لـY220C تفعيلًا قويًا لجينات الهدف الكلاسيكية لـp53 المشاركة في إيقاف دورة الخلية وتحفيز موت الخلية. أظهرت خلايا Y220S نمطًا مشابهًا جدًا—استعادة الشكل المطوي والنشط لـp53، وتفعيل جيني قوي، وتباطؤ التكاثر، وزيادة موت الخلايا—ولكن ذلك فقط عند تراكيز دوائية تزيد بأكثر من عشرة أضعاف تلك اللازمة لـY220C. بالمقارنة، لم تُظهر خلايا Y220N تنشيطًا واضحًا لجينات الهدف عند الجرعات المتحملة وبقيت في الغالب في الحالة غير المطوية، على الرغم من أن آثارًا طفيفة متأخرة على النمو توحي بوجود إنقاذ وظيفي جزئي فقط.
ماذا يعني هذا للمرضى وتصميم الأدوية المستقبلية
بالنسبة للأشخاص الذين تحمل أورامهم طفرة Y220S، تُعد هذه النتائج مشجعة بحذر: يمكن لريزاتابوبت، من حيث المبدأ، أن يستعيد وظائف p53 الواقية، لكن فقط عند جرعات أعلى بكثير قد يصعب تحقيقها بأمان لدى المرضى. بالنسبة إلى Y220N، يبدو أن الدواء الحالي غير كافٍ لإصلاح p53 بالكامل في ظروف واقعية. مع ذلك، ترسم المخططات الهيكلية في هذه الدراسة سبب ضعف أداء التصميم الحالي وكيف يمكن تعديل الجزيئات المستقبلية لتتفاعل مع ثلاث سلاسل جانبية متحوّرة دون إجبارها على أوضاع غير مرغوبة. بعبارة أخرى، يبدو أن إنشاء دواء حقيقي لإصلاح p53 يستهدف جميع متغيرات Y220 تحديًا لكنه قابل للتحقيق، وسيزيد بشكل طفيف عدد المرضى الذين قد يستفيدون من هذه الاستراتيجية الناشئة لإصلاح، بدلاً من استبدال، مثبط الورم الطبيعي في الجسم.
الاستشهاد: Mavridi, D., Funk, J.S., Balourdas, DI. et al. Targeting the p53 cancer mutants Y220C, Y220N, and Y220S with the small-molecule stabilizer rezatapopt. Cell Death Dis 17, 268 (2026). https://doi.org/10.1038/s41419-026-08492-9
الكلمات المفتاحية: إعادة تنشيط p53, ريزاتابوبت, طفرة Y220C, الطب الدقيق للسرطان, تثبيت البروتين