Clear Sky Science · ar
إزالة الإيوبيكويتين بواسطة OTUD4 تُثبّت مستقبل عامل نمو البشرة (EGFR) وتنشّط مسار PI3K/AKT لتعزيز غزو سرطان الثدي الثلاثي السلبي
لماذا يهم هذا البحث لسرطان الثدي
يُعد سرطان الثدي الثلاثي السلبي من أصعب أشكال سرطان الثدي على العلاج لأنه يفتقر إلى العلامات الهرمونية ومؤشرات النمو التي تستهدفها العديد من الأدوية. يكشف هذا البحث عن جزيء «حامٍ» خفي يساعد خلايا السرطان في إبقاء مفصل نمو قوي مُفعّلًا. بفهم هذا النظام الداعم الخفي، قد يجد العلماء طرقًا جديدة لقطع الإشارات التي تدفع نمو وتفشّي الورم.
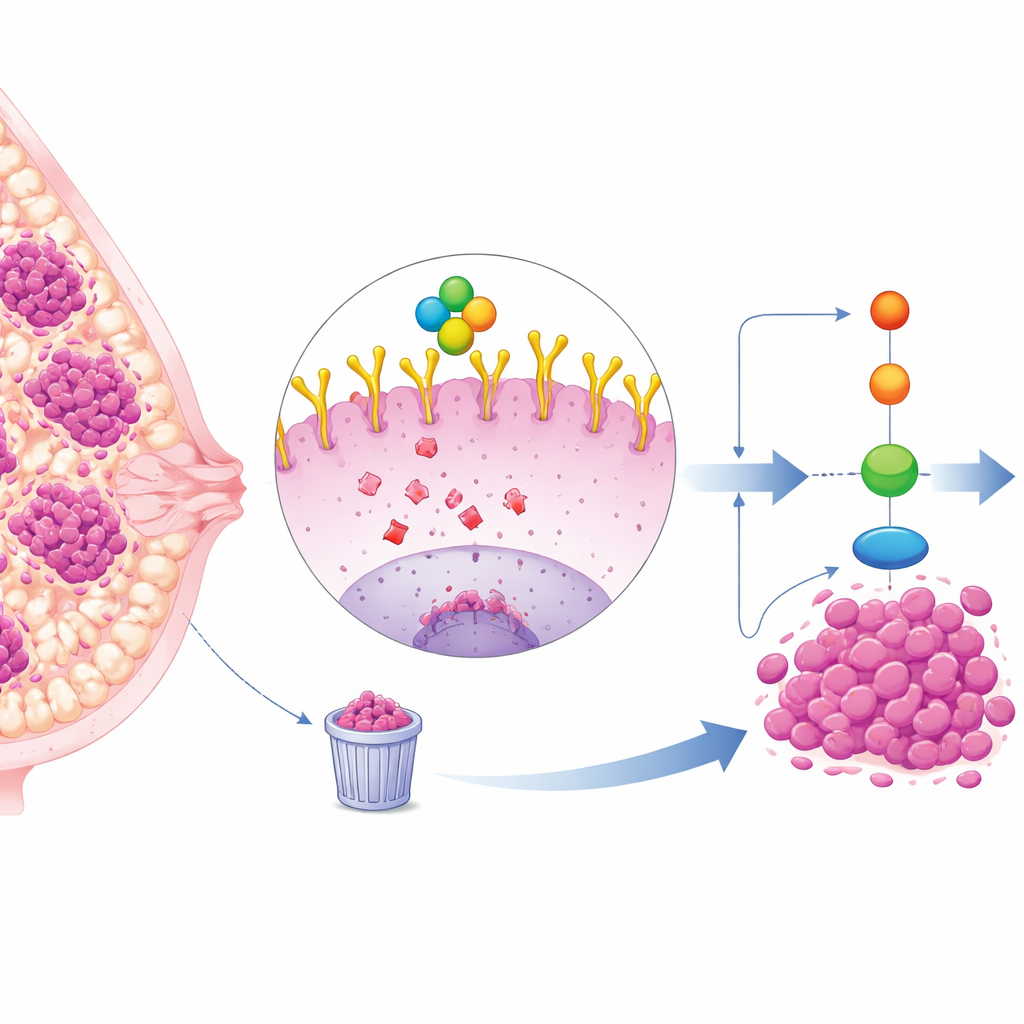
نمط فرعي من سرطان الثدي يصعب علاجه
يشكل سرطان الثدي الثلاثي السلبي (TNBC) نحو ربع حالات سرطان الثدي ويميل إلى النمو والانتشار بشكل أسرع من الأنماط الفرعية الأخرى. وبما أن خلايا TNBC لا تحمل مستقبلات الإستروجين أو البروجيسترون أو HER2، فإن العلاجات المستهدفة القياسية أقل فاعلية، مما يترك العلاج الكيميائي والجراحة كخيارين رئيسيين. ومع ذلك، تظهر كثير من أورام TNBC مستويات عالية من بروتين سطحي خلوي يُسمى EGFR، الذي يعمل كهوائي لاستقبال إشارات النمو والبقاء. ترتبط مستويات EGFR العالية بنتائج سيئة، لكن الأدوية التي تستهدف EGFR مباشرة قدمت نتائج مخيبة في العيادات، مما يشير إلى وجود طبقات أعمق من التنظيم.
اكتشاف مساعد خفي لنمو الورم
ركز الباحثون على OTUD4، وهو إنزيم يزيل وسومًا بروتينية صغيرة تسمى الإيوبيكويتين من بروتينات أخرى. غالبًا ما تعمل هذه الوسوم كإشارات للتخلص، فتضع علامة على البروتينات ليتم تفكيكها، لذا فإن إزالتها يمكن أن تُثبت البروتين المحمَّل بالوسم وتحميه. باستخدام قواعد بيانات سرطانية واسعة وعينات نسيجية من مرضى، أظهر الفريق أن مستويات OTUD4 أعلى في أورام وسلالات خلوية لـ TNBC مقارنةً بالنسيج الثديي الطبيعي. ويميل المرضى الذين تحتوي أورامهم على OTUD4 أكثر إلى البقاء على قيد حياة أقل، ما يوحي بأن OTUD4 يتصرف كجين مُسرطن يساعد على تقدم السرطان.
كيف يجعل OTUD4 خلايا السرطان أكثر عدوانية
لاختبار ما يفعله OTUD4 فعليًا في خلايا TNBC، خفض العلماء مستوياته في اثنتين من سلالات TNBC المدروسة على نطاق واسع. عندما تم قمع OTUD4، نمت الخلايا ببطء أكبر، وكونت مستعمرات أقل، وكانت أقل قدرة على الهجرة في تجارب شفاء الجروح وTranswell، وكلها علامات على تراجع العدوانية. وعندما زادوا مستوى OTUD4، حدث العكس: تكاثرت الخلايا أسرع وتحركت بسهولة أكبر، مما يعزز فكرة أن OTUD4 يدفع السلوك الخبيث. في الفئران، نمت الأورام المكوّنة من خلايا تفتقر إلى OTUD4 ببطء أكبر وأظهرت مؤشرات منخفضة للانقسام وإشارات النمو، مؤكدة هذه التأثيرات في كائن حي.
درع جزيئي يحمي EGFR
بالغوص في الآلية، استخدم الفريق فحوصات تفاعل البروتينات وتجارب بيوكيميائية لتحديد EGFR كشريك ارتباط مباشر لـ OTUD4. وجدوا أن OTUD4 يرتبط بمنطقة محددة من EGFR ويزيل سلاسل إيوبيكويتين مرتبطة بروابط K48، وهو نوع الوسم الذي عادة ما يعلّم الخلايا بتفكيك البروتين عبر نظام إعادة التدوير الخلوي. عندما خُفظ OTUD4، تحلل EGFR بسرعة أكبر، بينما ظلت مستوى نشاط الجين نفسه دون تغيير، مما يبيّن أن عمل OTUD4 يحدث بعد تصنيع EGFR وليس على مستوى الحمض النووي أو الرنا. إعادة تثبيط نظام التخلص من البروتينات أعادت مستويات EGFR، مشددة على أن الخطوة الأساسية هي الحماية من التحلل. بوجود EGFR أكثر استقرارًا على سطح الخلية، يبقى مسار إشارة داخلي رئيسي، وهو PI3K/AKT/mTOR، مفعّلًا، مما يدفع نمو الخلايا وبقائها.
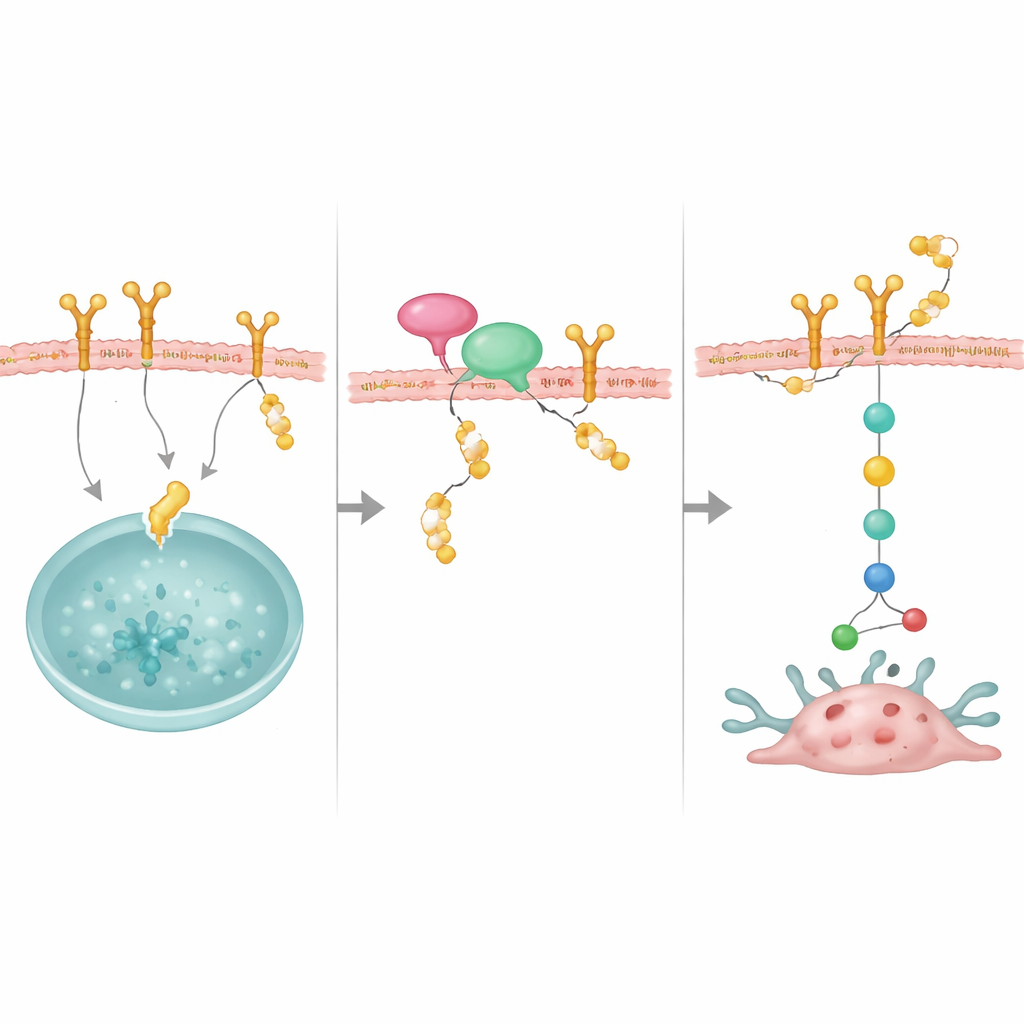
عامل موائم يجلب الحامٍ إلى هدفه
كشفت الدراسة أيضًا عن شريك مهم، NRP1، وهو بروتين غشائي رُبط سابقًا بسرطانات ثدي عدوانية. يرتبط NRP1 بكل من OTUD4 وEGFR ويساعد في وضع OTUD4 في المكان المناسب لإنقاذ EGFR من التحلل. عندما خُفض NRP1، أصبح EGFR أقل استقرارًا وضعفت إشاراته النمائية، على الرغم من أن مستويات OTUD4 لم تتغير. وقد نجحت زيادة إنتاج OTUD4 جزئيًا في التغلب على فقدان NRP1، ما يوحي بأن NRP1 يعمل كمنصة ارتكاز تجند OTUD4 إلى EGFR. معًا تشكل هذه الجزيئات مركبًا مثبتًا يحافظ على وفرة EGFR على سطح الخلية.
ماذا يعني هذا للعلاج المستقبلي
من خلال الكشف عن كيفية تعاون OTUD4 وNRP1 لحماية EGFR من التحلل، يحدد هذا البحث نقطة تحكم جديدة لإشارة نمو رئيسية في سرطان الثدي الثلاثي السلبي. بدلاً من محاولة حظر نشاط EGFR عند موقعه الفعّال، قد تهدف العلاجات المستقبلية إلى تعطيل الأفعال الحامية لـ OTUD4 أو تجنيده عبر NRP1، مما يخفض من مستويات EGFR ويضعف مسار PI3K/AKT الذي يغذي نمو الورم. وبينما ثمة حاجة لمزيد من العمل لإيجاد مثبطات آمنة وفعّالة لـ OTUD4 وفهم طرق الهروب المحتملة التي قد تستخدمها الخلايا السرطانية، تفتح النتائج سبلًا واعدة لعلاجات أكثر دقة ضد هذا النمط الصعب من سرطان الثدي.
الاستشهاد: Ren, Y., Zhou, F., Tan, Z. et al. OTUD4 deubiquitination stabilizes EGFR and activates the PI3K/AKT pathway to promote the invasiveness of triple-negative breast cancer. Cell Death Dis 17, 245 (2026). https://doi.org/10.1038/s41419-026-08482-x
الكلمات المفتاحية: سرطان الثدي الثلاثي السلبي, إشارة EGFR, OTUD4, مسار PI3K AKT, تحلل البروتين