Clear Sky Science · ar
ديهيدروجيناز الأسيل-كوإيه قصير السلسلة يبدأ إزالة ميثلة الحمض النووي الميتوكوندري وتسربه لتغذية المناعة المضادة للأورام في سرطان القولون والمستقيم
لماذا تختبئ خلايانا أحيانًا مناعة الجسم من السرطان
يُعد سرطان القولون والمستقيم أحد أخطر الأورام في العالم، جزئياً لأن دفاعات الجسم المناعية غالبًا ما تفشل في التعرف عليه ومهاجمته. تكشف هذه الدراسة عن صلة غير متوقعة بين طريقة حرق خلايا السرطان للدهون، وكيف تتعامل مصانع الطاقة الصغيرة داخلها (الميتوكوندريا) مع حمضها النووي، وما إذا كانت المنظومة المناعية تُنبه بوجود الورم. من خلال تتبع سلسلة هذه الأحداث، يبرز الباحثون أيضًا مركبًا طبيعيًا قديمًا، الهايبرسين، كطريقة محتملة لإيقاظ الهجوم المناعي في سرطان القولون والمستقيم.
"حارس" ميتوكوندري مفقود في أورام القولون
بدأ الفريق بالبحث في مجموعات بيانات بشرية وفأرية كبيرة عن جينات استقلابية تتغير باستمرار في سرطان القولون والمستقيم. برز إنزيم واحد: ديهيدروجيناز الأسيل-كوإيه قصير السلسلة (ACADS)، الذي يساعد عادة الميتوكوندريا على تكسير الأحماض الدهنية القصيرة. في عينات المرضى وعدة نماذج فأرية، كانت مستويات ACADS أقل بكثير في نسيج الورم مقارنة بالنسيج السليم المجاور في القولون. عندما خفّض العلماء مستوى ACADS في خلايا سرطان القولون الفأرية، نمت الأورام أسرع وبشكل أكثر عدوانية؛ أما رفع مستوى ACADS فأبطأ نمو الورم. كما طوِّعَت فئران تفتقر إلى ACADS تحديدًا في بطانة أمعائها لتطوير أورام أكثر وعددًا وحجمًا في نموذج كيميائي لسرطان مرتبط بالتهاب القولون، مما يدعم الفكرة أن ACADS يعمل كمثبط للأورام في الأمعاء.
كيف تطفئ الأورام إشارات الإنذار المناعي
لا يمكن تفسير هذه التأثيرات على النمو بمجرد سرعة تكاثر الخلايا السرطانية في طبق، والتي تغيّرت قليلًا. بدلاً من ذلك، دفع فقدان ACADS نمو الورم فقط في الحيوانات ذات الأنظمة المناعية السليمة، ما يشير إلى تغيُّرات في محيط الورم الدقيقة. أظهرت تحليلات الخلايا الفردية لأورام القولون والمستقيم البشرية أن الأورام ذات المستويات المنخفضة من ACADS كانت محاطة بمزيد من الخلايا الورمية والخلايا المناعية القامعة—مثل الخلايا القمعية المكونة من النخاع، وبعض الخلايا البلعمية، وخلايا T التنظيمية—وأعدادًا أقل من خلايا T المساعدة وخلايا القاتل الطبيعي. يشير هذا النمط إلى "حي منيع قمعي" يحمي السرطان من الهجوم. 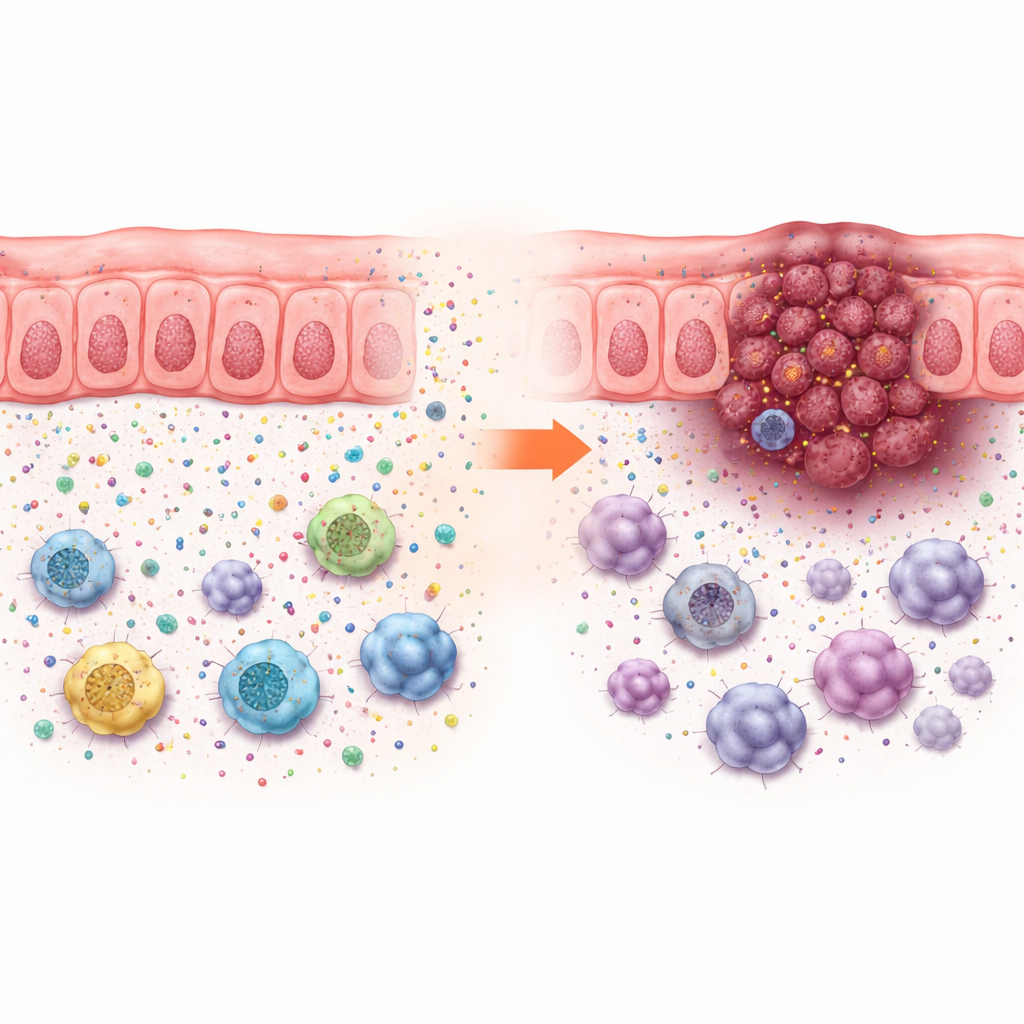
تسرب الحمض النووي الميتوكوندري كزناد مخفي
ما الرابط بين إنزيم حرق الدهون ومستشعر الحمض النووي المناعي؟ الإجابة تكمن في الحمض النووي الميتوكوندري (mtDNA). تحت الضغط، يمكن لقطع من mtDNA أن تتسرب من الميتوكوندريا إلى سائل الخلية المحيط، حيث يكتشفها cGAS كإشارة خطر. أظهر الباحثون أن خلايا السرطان الناقصة ACADS كان لديها كمية أقل من mtDNA في هذا الحيز، رغم أن إجمالي mtDNA لم يتغير. إيقاف تسرب mtDNA في الخلايا ذات ACADS العالية أوقف مسار cGAS–STING، مؤكداً أن هذه القطع الهاربة من الحمض النووي هي الإنذار الحاسم. بشكل مفاجئ، لم تستطع عوامل الإجهاد الميتوكوندري الكلاسيكية مثل أنواع الأكسجين التفاعلية، وارتفاعات الكالسيوم، والتغيرات الكبيرة في شكل الميتوكوندريا تفسير الفرق بالكامل. بدلاً من ذلك، تشير الدراسة إلى "البوابات" في غشاء الميتوكوندريا والأهم من ذلك إلى العلامات الكيميائية على mtDNA نفسه. 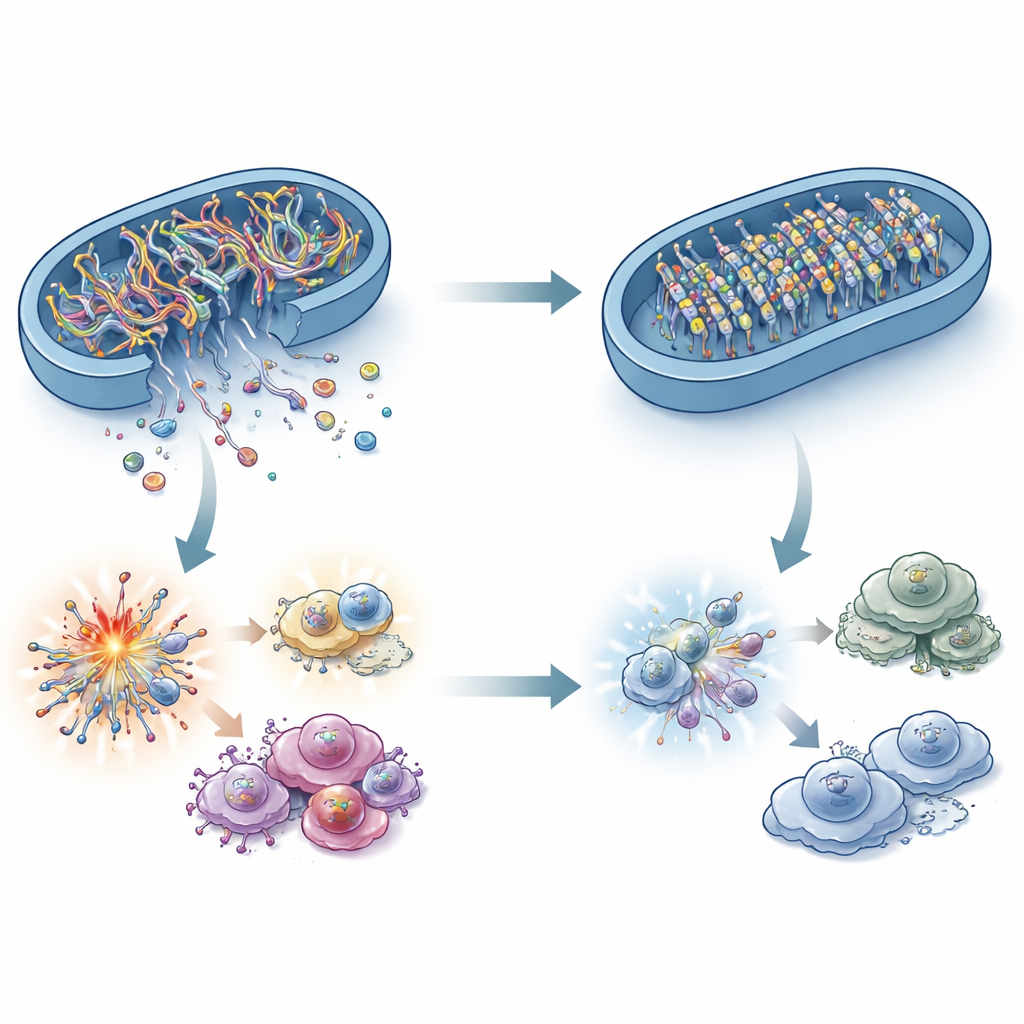
شريك معدل لميثلة الحمض النووي يقفل الإنذار
من خلال شاشات تفاعل البروتينات، وُجد أن ACADS يرتبط بصورة من إنزيم ميثلة الحمض النووي DNMT1 التي تتموضع في الميتوكوندريا. عندما فُقد ACADS، تراكم هذا الشكل الميتوكوندري من DNMT1، مضيفًا مجموعات ميثيل إضافية إلى mtDNA. تجعل هذه العلامات mtDNA أكثر استقرارًا وأقل عرضة للانكسار والتسرب. أدى تحميل الخلايا بكمية زائدة من DNMT1 الميتوكوندري إلى تقليل هروب mtDNA، وكبح إشارة cGAS–STING، وتسريع نمو الورم، بينما أعاد حجب DNMT1 بالعقار ديستابين تسرب mtDNA وأبطأ الأورام الناقصة ACADS. عكست عينات المرضى هذه النتائج: ربطت المستويات المنخفضة من ACADS بوجود DNMT1 ميتوكوندري عالي، وضعف إشارة STING، وقلة خلايا T الفاعلة، وزيادة الخلايا المناعية القامعة، وتوقعات أسوأ للاستجابة لمثبطات نقاط التفتيش المناعية.
إيقاظ الدفاعات المناعية بمركب قديم
للاختبار ما إذا كان يمكن استغلال هذا المسار علاجيًا، استخدم الباحثون فحصًا حاسوبيًا للبحث عن جزيئات ترتبط بـ ACADS. وجدوا الهايبرسين، صبغًا طبيعيًا جُرِّب سابقًا كعلاج منشط بالضوء لبعض ليمفوما الجلد. في خلايا سرطان القولون والمستقيم، زاد الهايبرسين مستويات ACADS، وخفض DNMT1 الميتوكوندري، وعزز تسرب mtDNA، وأعاد تفعيل إشارة cGAS–STING—تغييرات كانت تعتمد على وجود ACADS. في نماذج أورام فأرية وفي زروعات قصيرة الأمد لأورام بشرية من القولون والمستقيم، قلص علاج الهايبرسين حجم الأورام أو حوّل الخلايا المناعية نحو حالة أكثر نشاطًا وغنى بخلايا T. على الرغم من أن هناك حاجة لمزيد من العمل قبل الاستخدام السريري، تشير هذه النتائج إلى أن إعادة "تشغيل" ACADS دوائيًا قد تساعد في تحويل ورم بارد ومثبط مناعيًا إلى ورم يستجيب بشكل أفضل للعلاج المناعي.
ماذا يعني هذا للمرضى والعلاجات المستقبلية
بشكل مبسط، تُظهر هذه الدراسة أن بعض سرطانات القولون والمستقيم تنمو جزئيًا لأنها تطفئ إنزيمًا ميتوكوندريًا كان يساعد عادةً على تسرب مقاطع صغيرة من الحمض النووي إلى داخل الخلية، حيث تعمل كأشعة تحذيرية لاستدعاء الجهاز المناعي. عن طريق السماح لشريك ميثل الحمض النووي أن يقفل ذلك الحمض الميتوكوندري في مكانه، تحافظ الأورام الناقصة ACADS على إخفاء تلك الإشارات وتتجنب اكتشاف الجهاز المناعي. قد يعيد استعادة نشاط ACADS، مثلًا بواسطة أدوية شبيهة بالهايبرسين، فتح نظام الإنذار الميتوكوندري هذا، وتقوية المناعة المضادة للأورام، وتحسين الاستجابة للعلاجات المناعية الحالية. لذلك قد تكون ACADS وDNMT1 الميتوكوندري ونشاط مسار STING بمثابة مؤشرات حيوية مفيدة وأهداف في السعي لعلاجات أكثر فاعلية لسرطان القولون والمستقيم.
الاستشهاد: Yang, F., Wang, M., Hu, S. et al. Short-chain acyl-CoA dehydrogenase initiates mtDNA demethylation and leakage to fuel antitumor immunity in colorectal cancer. Sig Transduct Target Ther 11, 113 (2026). https://doi.org/10.1038/s41392-026-02675-8
الكلمات المفتاحية: سرطان القولون والمستقيم, مناعة الورم, الحمض النووي الميتوكوندري, استقلاب الدهون, مسار cGAS-STING