Clear Sky Science · ar
استهداف البروتين المندمج في الساركوما (FUS): استراتيجية مضادة للاستطالة جديدة لعلاج التليف الرئوي مجهول السبب
لماذا يهم تندب الرئتين
التليف الرئوي مجهول السبب (IPF) هو مرض رئوي متقدم تتحول فيه الحويصلات الهوائية الرقيقة تدريجياً إلى نسيج ندبي جامد، ما يجعل كل نفس أكثر صعوبة. الأدوية المتاحة اليوم قد تبطئ هذا التندب لكنها لا تستطيع إيقافه أو عكسه. تستكشف هذه الدراسة هدفًا جديدًا يُدعى FUS، وهو بروتين يساعد الخلايا على التعامل مع رسائلها الجينية، وتختبر ما إذا كان إيقافه بواسطة شريط مصمم من مادة شبيهة بالحمض النووي يمكن أن يهدئ عملية التندب ويساعد الرئتين المتضررتين على الإصلاح.
موزع حركة خلوية يخطئ المسار
عادةً ما يعيش بروتين FUS في نواة الخلية، حيث يساعد في تنظيم كيفية معالجة الحمض الريبي النووي (RNA) — النسخة العاملة من جيناتنا — واستخدامها. في أمراض الدماغ مثل التصلب الجانبي الضموري (ALS)، قد يعمل FUS بشكل خاطئ فيغادر النواة ويتجمع في مناطق الخلية الخارجية، مما يعيق الوظائف الخلوية الطبيعية. تساءل المؤلفون عما إذا كان سلوك مماثل قد يدفع التندب في IPF. درسوا الأرومات الليفية الرئوية — خلايا النسيج الضام التي تفرز مواد الندبة — من مرضى IPF ومن مانحين أصحاء. في خلايا IPF، كانت مستويات FUS أعلى عموماً، والجانب الحاسم هو أن كمية أكبر بكثير من FUS وُجدت في السيتوبلازم مقارنة بالخلايا الصحية. باستخدام المجهر الإلكتروني عالي الدقة، أكدوا أن هذا البروتين كان وفيرًا بشكل غير طبيعي خارج النواة، مما يوحي بأن سيطرته المعتادة على الـRNA قد تكون مشوهة في الرئات المتليفّة. 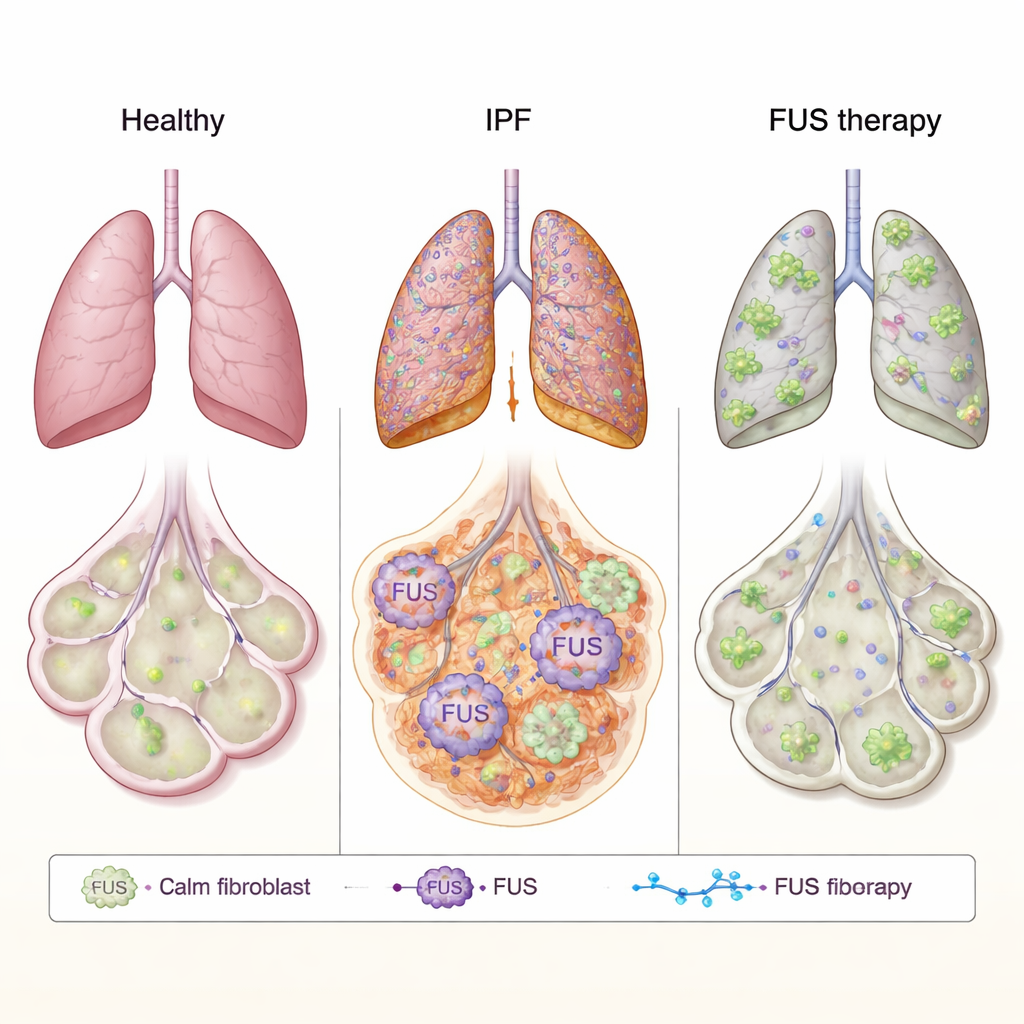
كيف يغذي FUS خلايا التندب
للفهم العملي لهذا البروتين الخارج عن السيطرة، عزَّز الباحثون وجود FUS في الأرومات الليفية السليمة وخفضوه في خلايا IPF. أدى وجود FUS الزائد إلى دفع الخلايا السليمة للانقسام بسرعة أكبر، بينما أدى تقليل FUS في خلايا IPF إلى إبطاء نموها وحركتها — سلوكان مركزيان لتكوين الندبة. استخدم الفريق بعد ذلك تقنية «تجمِّد» شراكات البروتين–RNA وقراءة أي RNAs ترتبط بـFUS. في أرومات IPF، وُجد FUS مرتبطًا بالعديد من الرسائل الجينية التي تعزز التليف، بما في ذلك تلك التي تشفر الكولاجين وعوامل النمو مثل TGF‑β والإشارات الالتهابية. بعبارة أخرى، كان FUS يعمل كمحور يربط شبكة كاملة من الرسائل الداعمة للتندب.
إسكات الإشارة بدواء دقيق
اختبرت الدراسة أوليغونوكليوتيدًا مضادًا للمسار يُدعى ION363 — شريطًا قصيرًا مُعدَّلًا كيميائيًا مصممًا ليرتبط بـRNA الخاص بـFUS ويحفز تكسيره. عندما عولجت أرومات IPF بـION363، انخفضت مستويات FUS، وتباطأت الخلايا في التكاثر والهجرة، وخفتت التعبيرات الجينية الأساسية لبناء الندبة. من المهم أن هذا التأثير لم يكن نتيجة لقتل الخلايا أو إدخالها في الشيخوخة القسرية؛ بل بدا أنه يعيد ضبط سلوكها. عند تطبيق العلاج نفسه على مقاطع رئوية رقيقة من مرضى IPF محفوظة حية في المختبر، هبطت مجموعات كبيرة من الجينات المرتبطة بالمادة البينية خارج الخلوية والالتهاب والبطانة الظهارية الشاذة، بينما ارتفعت الجينات المرتبطة بإنتاج السورفكتانت الصحي ووظيفة الحويصلات الهوائية. كما خفف العلاج من صبغة الكولاجين وزاد من مؤشرات خلايا سطح الرئة الوظيفية، ما يشير إلى تحول من التندب نحو الإصلاح.
مساعدة الحويصلات الهوائية المتضررة على النمو مجدداً
نظرًا لأن خلايا البطانة المبطنة للحويصلات الهوائية الصغيرة، المعروفة بخلايا الحويصلة من النوع الثاني، حاسمة لإصلاح الرئة، بنى الباحثون «ألويلوسفيرات» ثلاثية الأبعاد من خلايا المرضى لمحاكاة وحدات رئوية مصغرة. في المزارع الخلوية من مرضى IPF، هذه البنى عادة ما تعاني من ضعف البقاء. مع علاج ION363 تكوَّنت ألويلوسفيرات أكثر، ونمت أكبر، وأظهرت نشاطًا ليسوزوميًا أكبر — سمة مميزة للتجدد النشط. أظهر التلوين التفصيلي مزيدًا من الخلايا الحاملة لمؤشرات خلايا متخصصة في تبادل الغازات، مما يشير إلى أن إسكات FUS لم يهدئ الأرومات الليفية فحسب، بل شجع أيضًا الظهارة المتضررة على إعادة بناء سطح صحي. 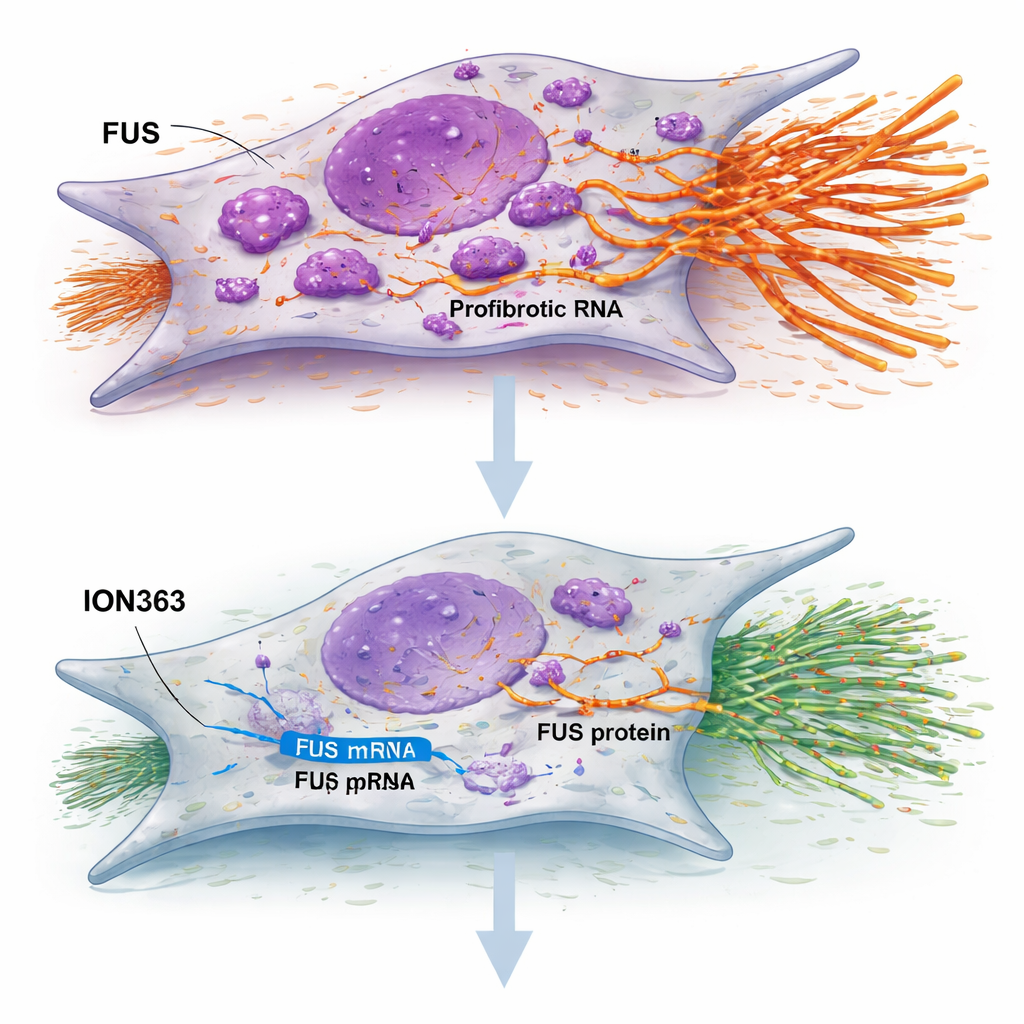
ماذا قد يعني هذا للمرضى
مجمل النتائج تصوّر FUS كمفتاح رئيسي في IPF يربط الأرومات الليفية المفرطة النشاط والمشكلة مع فشل إصلاح الحويصلات الهوائية الرقيقة. بخفض نشاط FUS بواسطة دواء مضاد للمسار موجه، استطاع الباحثون تقليل برامج الجينات المروِّجة للتليف، وتخفيف تراكم الكولاجين، وتعزيز التجدد في نماذج رئوية مشتقة من مرضى بشر. رغم أن هذه المقاربة لا تزال على مستوى المختبر وستتطلب اختبارات دقيقة في نماذج حيوانية وتجارب سريرية، فإنها توحي بأن IPF قد يُعالج يومًا ما ليس فقط بإبطاء التندب، بل بإعادة موازنة البرامج الخلوية التي تتحكم في إصابة الرئة وإصلاحها.
الاستشهاد: Katariya, B.B., Chillappagari, S., Arnold, L. et al. Targeting fused in sarcoma (FUS): a novel antisense strategy for treating idiopathic pulmonary fibrosis. Sig Transduct Target Ther 11, 70 (2026). https://doi.org/10.1038/s41392-026-02585-9
الكلمات المفتاحية: التليف الرئوي مجهول السبب, أوليغونوكليوتيد مضاد للمسار, بروتين FUS, تليف الرئة, إصلاح الحويصلات الهوائية