Clear Sky Science · zh
使用纳米柱光子晶体生物传感器实现超灵敏阿尔茨海默病生物标志物检测
为什么一种简单的记忆力丧失血检很重要
随着能够减缓阿尔茨海默病进展的新药问世,医生迫切需要能够在症状明显出现前很久就识别出风险人群的简单检测方法。如今,确认阿尔茨海默病通常需要昂贵的脑部影像或腰穿检查,而常规护理中很少有人接受这些检查。本研究描述了一种基于光学的微型传感器,能够在一滴血液中以临床相关的水平识别出与阿尔茨海默病相关的关键分子,有望为可在日常诊所甚至床边使用的快速、低成本检测铺平道路。
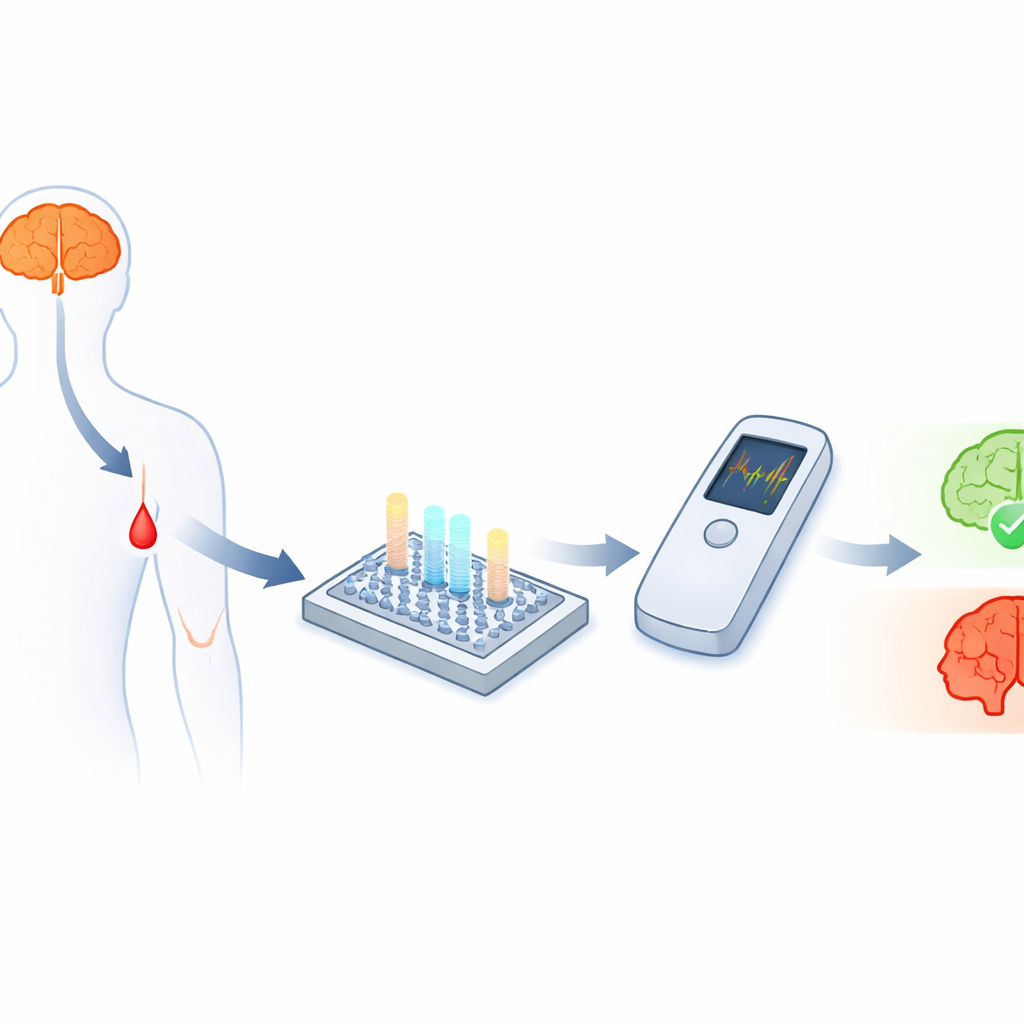
在血液中寻找线索
阿尔茨海默病与一种叫做淀粉样‑β的小蛋白片段密切相关,尤其是两种形式Aβ40和Aβ42。它们的含量,尤其是二者的比值,携带着关于疾病是否存在及其进展情况的重要线索。挑战在于这些片段非常微小,在血液中以极低浓度循环——每毫升只有万亿分之一克量级——在专门实验室外很难准确测量。尽管电化学传感器原则上可以检测到如此低的浓度,但要将其开发成能够同时追踪多个生物标志物、同时又坚固耐用且价格可承受的现场检测设备却很困难。
通过微小柱状结构引导光
研究团队利用纳米光子学来应对这一挑战——这是一类能在比光波长还小的尺度上控制光的结构。他们在玻璃芯片上制造了一阵规则排列、成对的细如发丝的硅柱。当光照射到这种有图案的表面时,光会被束缚在一种特殊的谐振模式中,这种模式对柱顶附近的微小变化极为敏感,类似于调音叉若附着了物质时音色会发生变化。通过精细调整每对柱子之间的间距,研究者们在三项关键性质之间达成了平衡:光学谐振的清晰度、其对周围环境变化的响应强度,以及产生信号的幅度。这样的“最佳点”设计使芯片特别适合检测微量物质。
让肉眼看不见的分子可见
即便采用了这种优化设计,阿尔茨海默病标志物本身对光的扰动仍然微乎其微。为放大这种效应,研究者使用了一种夹心式策略并辅以金纳米颗粒。首先,他们在传感器表面涂覆了几层粘附性化学层,能使特异性抗体正确定向,使其结合位点朝向液体侧。这些抗体从样本中捕获Aβ40或Aβ42。随后,带有第二种识别同一淀粉样片段不同端位抗体的金纳米颗粒被流过芯片。当存在淀粉样片段时,它会在表面和金颗粒之间形成桥接,从而“标记”其存在。由于金属对局部光学环境有强烈扰动作用,每个被捕获的片段在传感器谐振上产生的位移远大于肽本身,从而将灵敏度提升约一到两个数量级,同时仍保持清晰的光学信号。
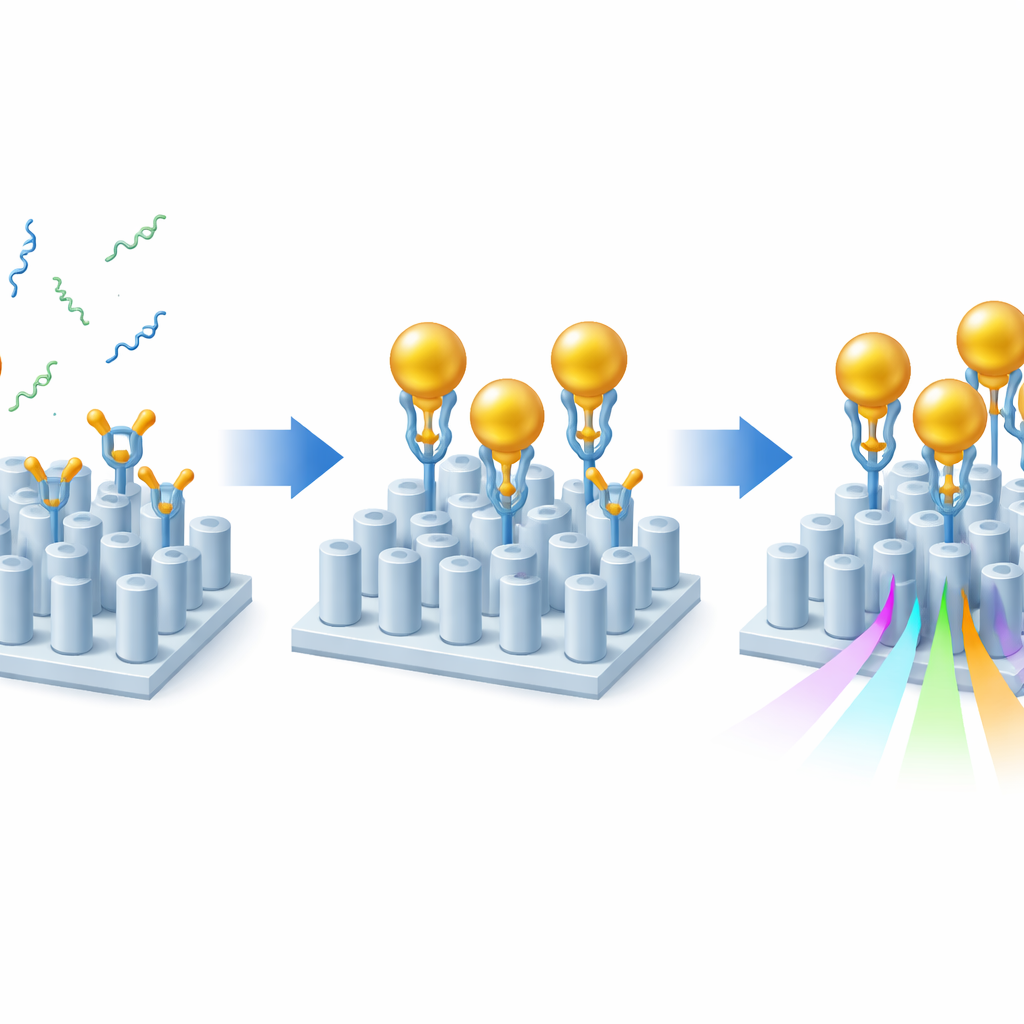
检测更接近真实的样本
为证明该方法在简单实验缓冲液之外也能奏效,团队用人血清对其传感器进行了测试。他们将血清稀释以便与微流控操作兼容,同时仍保持淀粉样蛋白水平与患者体内相当。重要的是,他们能在这种稀释血清中检测到0.2皮克克/毫升(pg/mL)的Aβ40和Aβ42——相当于全血中临床相关的20皮克克/毫升的水平。通过在同一芯片的不同区域点置不同的捕获抗体,他们在单一微小通道内同时测量了两种淀粉样形式,这是从同一小样本评估二者比值的关键一步。信号能够清晰地区分被额外添加淀粉样蛋白的样本与仅含自然背景水平(即便在健康人中也存在)的样本。
这对未来护理可能意味着什么
综上所述,这些进展表明,一种小型的光学传感器结合金纳米颗粒的放大作用,能够达到有意义的阿尔茨海默病血液检测所需的灵敏度,同时可以同时处理多个生物标志物。尽管还需更多工作将其转化为稳健的商业化设备,并加入如不同形式的tau蛋白等其他标志物,但该基础技术由可扩展的材料构建,可与简单的手持光学设备配对。如果完全开发成熟,它可使临床医生仅凭一小份血样就监测脑部健康,从而大大简化阿尔茨海默病的早期发现并追踪治疗效果随时间的变化。
引用: Guilherme S. Arruda, Katie Morris, Augusto Martins, Yue Wang, Sian Sloan-Dennison, Duncan Graham, Steven D. Quinn, Emiliano R. Martins, and Thomas F. Krauss, "Ultrasensitive Alzheimer’s disease biomarker detection with nanopillar photonic crystal biosensors," Optica 12, 1587-1596 (2025). https://doi.org/10.1364/OPTICA.566672
关键词: 阿尔茨海默氏症血液检测, 纳米光子生物传感器, 淀粉样β蛋白, 金纳米颗粒, 早期诊断