Clear Sky Science · zh
共振胶原蛋白的飞秒激光选择性肿瘤消融
将光转化为靶向的抗癌工具
胰腺癌是最致命的癌症之一,部分原因在于很难在不损伤周围脆弱器官的情况下切除肿瘤。本研究探索了一种使用不可见的超快近红外脉冲更精确烧灼胰腺肿瘤的新方法,方法是瞄准肿瘤中过量存在的一种结构成分。该工作暗示了未来可能的治疗方式,能够在更好保护健康组织的同时强力打击癌细胞。
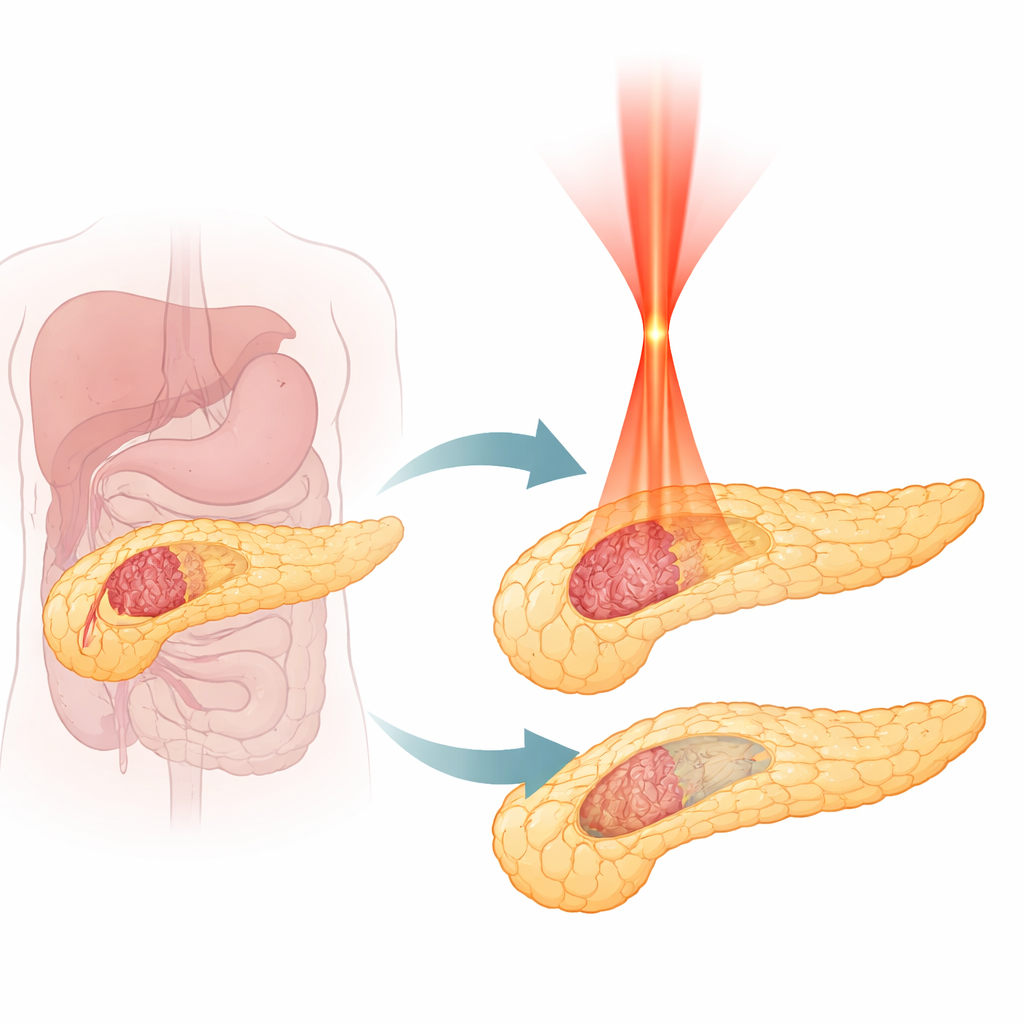
为什么胰腺肿瘤如此难以治疗
胰腺导管腺癌是胰腺癌最常见的形式,生长迅速且常在晚期才被发现。只有极少数患者适合手术,即使是现代化疗和放疗也效果有限。通过热破坏组织的治疗方法,比如射频、微波或传统激光消融,可以缩小肿瘤,但它们往往会烧毁路径上的一切。由于胰腺靠近重要血管和脆弱的消化结构,扩大治疗范围会带来严重并发症风险。因此医生需要一种在破坏过程中能够区分肿瘤与正常胰腺的方法,而不是简单地加热一大片区域。
在肿瘤组织中发现隐蔽弱点
作者关注了胰腺肿瘤与健康胰腺之间的一个关键物理差异:肿瘤中充斥着富含胶原蛋白的坚硬纤维物质,而正常组织则更柔软、结构更松散。通过对手术样本进行常规组织染色和电子显微镜观察,他们证明了癌组织中存在致密的胶原纤维束,而邻近的健康胰腺纤维明显较少。随后他们用红外光谱测量这些组织对不同中红外波长的吸收强度。两种组织在类似波段都有吸收,但肿瘤在约6.1微米处表现出明显更强的峰值,这对应于胶原的振动模式。这提示将激光精确调谐到该波长,可能比对正常胰腺更有效地加热并破坏肿瘤组织。
构建一台能“听见”胶原的激光器
为验证这一想法,团队构建了一台强功率中红外激光,发射中心波长为6.1微米的超短脉冲——脉冲持续时间仅为几百飞秒(十的负十五次方的几十至数百倍),这些“飞秒”脉冲能够限制不必要的热扩散,有点像一系列受控的小型闪电。该系统通过特殊晶体将高功率工业激光转换为所需波长,平均输出功率可超过一瓦;这已足以实现实际组织消融。研究人员还研发了一种玻璃制的中空光纤,可将该波长光沿柔性路径引导——这是把激光通过细针送入体内、实现微创操作的重要一步。
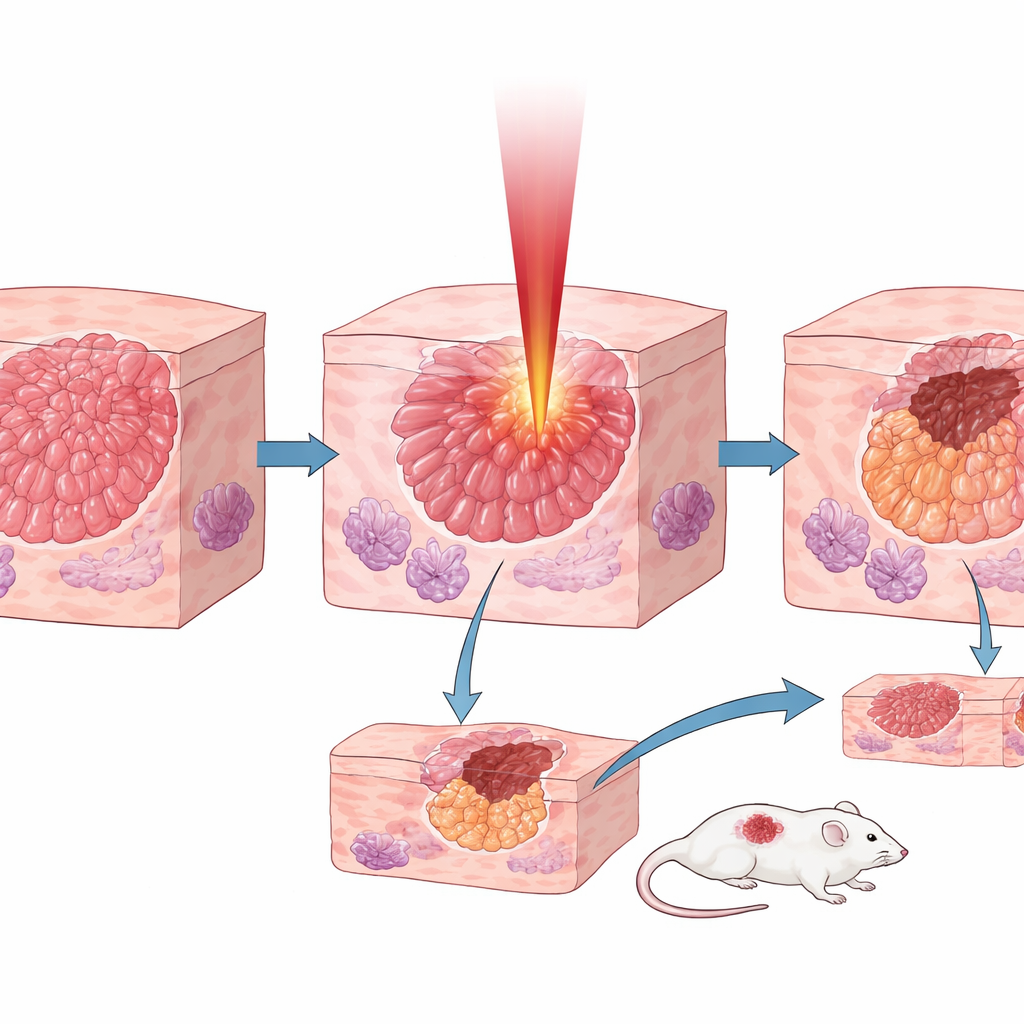
在细胞、鼠类和人体组织中的选择性测试
在两种胰腺癌细胞系的细胞培养中,6.1微米激光比1微米或3微米激光致死性高得多,暴露数秒到数分钟内细胞存活率显著下降。在皮下移植胰腺肿瘤的小鼠模型中,比较了三种不同波长。尽管1微米光束功率远高于6.1微米,但它只能去除表浅的肿瘤层。以胶原共振为目标的6.1微米激光实现了5到10倍更深的消融深度,并显著减缓肿瘤生长,使处理组肿瘤体积最终约为未处理组的八分之一。最重要的是,当团队将6.1微米激光用于人体肿瘤样本及相邻正常胰腺时,在相同条件下肿瘤切口比健康组织深2到3倍,显示出真正的选择性。相反,当他们测试另一种不积累额外胶原的肝脏肿瘤类型时,这种优势大多消失,进一步强调了胶原在其中的核心作用。最后,他们还展示了中空光纤能够传递相同的选择性效果,支持未来基于针状器械的治疗方案。
这对未来癌症护理可能意味着什么
研究表明,精确调谐的中红外短脉冲可以利用肿瘤与健康组织之间的材料差异,实现更有选择性的破坏。通过靶向富含胶原的区域,6.1微米飞秒激光能更深地切入胰腺癌,同时保留更多周围器官组织。尽管该工作仍处于实验阶段,需要在更现实的模型和临床环境中进行更多测试,但它指向了一类基于影像引导、光纤传输的微创手术方式,未来可能以更高精度和更少副作用治疗胰腺肿瘤以及其他富含胶原的癌症。
引用: Dunxiang Zhang, Xing Huang, Xuemei Yang, Ning Xia, Kan Tian, Jinmiao Guo, Maoxing Xiang, Linzhen He, Zhizhuo Fu, Ang Deng, Han Wu, Yuxi Wang, Wonkeun Chang, Bole Tian, Junjie Xiong, Qi Jie Wang, Anderson S. L. Gomes, and Houkun Liang, "Selective tumor ablation via femtosecond laser resonant with collagen," Optica 12, 1578-1586 (2025). https://doi.org/10.1364/OPTICA.561337
关键词: 胰腺癌, 激光消融, 胶原蛋白, 中红外, 微创手术