Clear Sky Science · zh
动力蛋白优化蛋白-膜相互作用以促使裂解
细胞如何巧妙地从自身膜上捏下小块
你的细胞每秒都在忙着捏下微小的膜泡以运输货物、重塑内部隔间并抵御病毒。这看似简单的将狭窄膜管切成两段的动作,从物理学角度看却出乎意料地难。本文提出了一个看似基础但不容小觑的问题:一种称为动力蛋白(dynamin)的蛋白如何使膜的切割既可行又可靠,哪些蛋白特性对完成这项工作是真正必要的?
正在工作的细胞“捏合器”
动力蛋白是一种分子机器,会在细小的膜管周围形成围圈并像绞索一样收紧以帮助其断裂。这类裂解事件支撑着内吞作用等过程,细胞借此将物质拉入内部,以及线粒体等内部结构的分裂。如果不借助外力,膜管强烈抵抗断裂,因为它必须先被压缩到几乎与膜厚相当并通过一个不稳定的中间态。这个能量障碍远高于细胞内随机热扰动所能提供的能量,因此像动力蛋白这样的专门裂解蛋白是必需的。
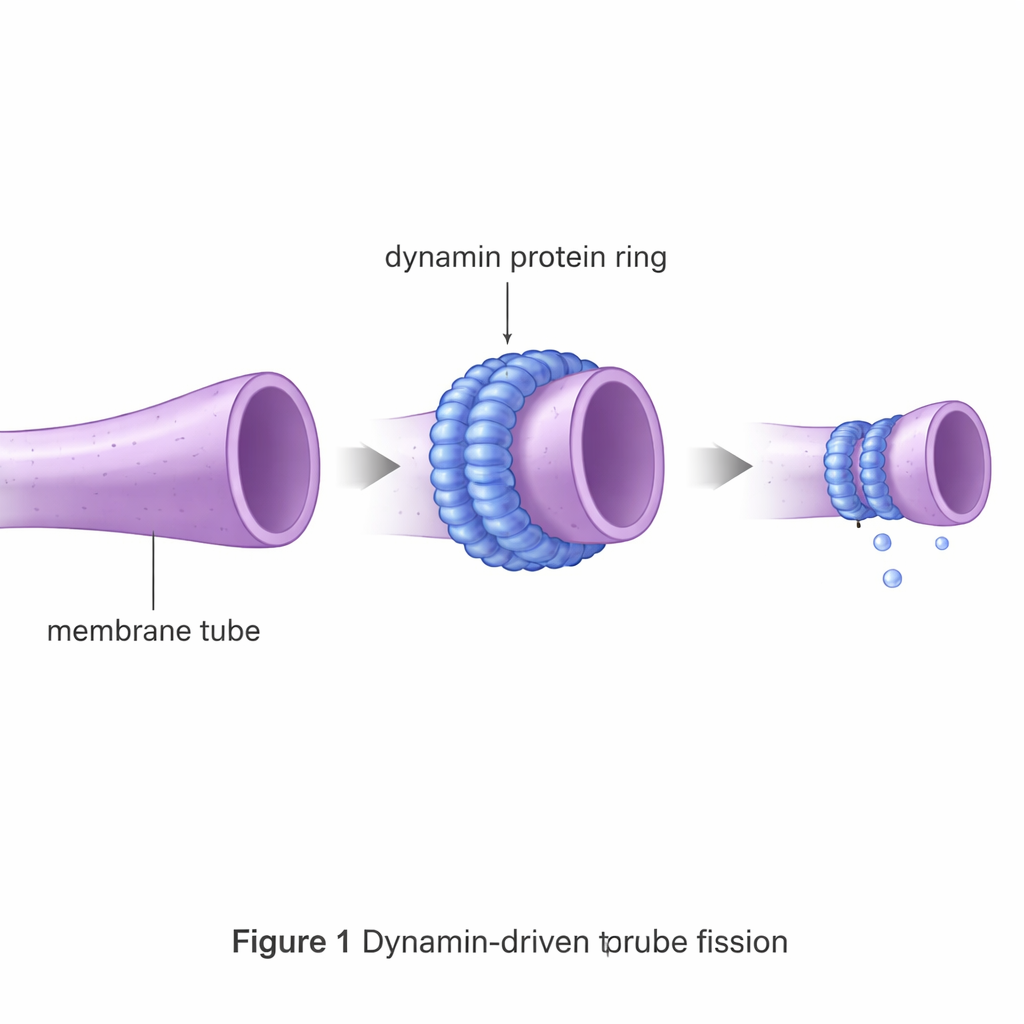
用虚拟膜测试蛋白设计
直接观察管子断裂的关键瞬间在实验中非常困难:快速成像缺乏分子细节,而高分辨率方法又需要将系统固定在时间点上。为弥合这一差距,作者使用了一种强大的理论工具——自洽场理论。他们不追踪每个原子,而是将脂质和溶剂描述为在平滑场中运动的柔性链。蛋白不是以完整的原子结构引入,而是作为环状外部势场,表现为简单排斥空间、粘附在膜表面或插入外层。利用该框架,他们能计算出膜的形状以及从完整管到裂解中间态所需的完整自由能代价。
什么样的抓握有助于管子断裂?
研究团队系统地改变类似动力蛋白的模型与膜的相互作用。有些模型蛋白只是在人群拥挤般覆盖表面,表现为刚性袖环;有些对外层头基有轻度或强烈的黏附;还有些模仿真实动力蛋白的PH结构域,通过将疏水部分插入外层并把头基“撑开”。对于每种情况,他们考察三项关联量:蛋白对未收缩管的黏附强度、结合时诱导的曲率与收缩程度,以及管子进入半裂解(hemifission)——内层已合并的中间态时仍需跨越的能量障碍。他们发现,仅靠简单挤压可以降低障碍,但不足以解释高效裂解;而强烈的表面黏附反而可能阻碍断裂,因为膜必须先从蛋白上剥离才能完成塌陷。
为什么浅层插入胜过简单挤压
最有效的设计是蛋白部分插入脂质头基之间并向上拉动脂肪链,在膜上产生局部的倒V形(人字形)弯曲。这种“撑开”使管子的最窄点略微偏离蛋白环的正下方而位于一侧。结果,膜可以在不与蛋白脱离的情况下完成向半裂解中间态的关键塌陷,总体能量障碍相比裸膜管降低了一个数量级以上。当作者允许蛋白参数自动调整以最小化该障碍时,最优解与动力蛋白PH结构域的尺寸与作用极为接近:一个中等宽度、浅层插入的疏水片段,而非会从溶液中剥离脂质的宽大且过于粘性的表面。
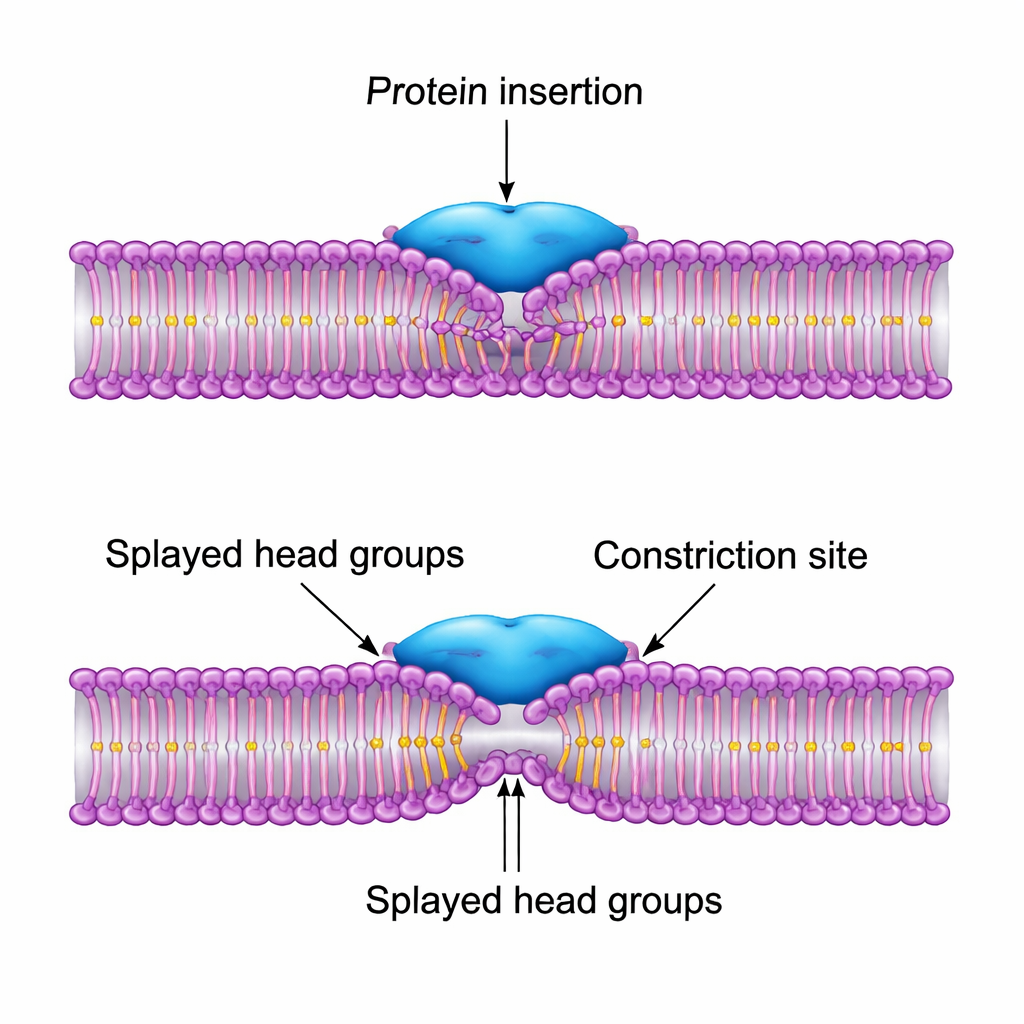
给自然与纳米技术的设计规则
对非专业读者而言,关键信息是:动力蛋白的作用不仅仅是像系紧皮带那样收紧膜,而是通过精确调节它如何以及在何处抓握外层来发挥作用。一个能撑开外层脂质并将曲率聚焦在蛋白旁侧的浅楔,比粗暴收缩或强粘附更为有效。这些结果有助于解释为何进化偏好了动力蛋白的特定结构,并为需要可控切割或重塑膜的合成蛋白或药物在医学与纳米技术中的设计提供了原则性指导。
引用: Spencer, R.K.W., Müller, M. Dynamin optimizes protein-membrane interactions for fission. npj Soft Matter 2, 6 (2026). https://doi.org/10.1038/s44431-026-00018-9
关键词: 膜裂解, 动力蛋白, 蛋白–膜相互作用, 膜曲率, 自洽场理论