Clear Sky Science · zh
APP E590D 突变增加 Aβ 和 Aη 肽的产生并加剧 tau 病变
为何这个罕见突变很重要
通常认为阿尔茨海默病是两种有害蛋白——淀粉样蛋白和 tau——在脑内缓慢积累的过程。大多数人患病没有单一明确原因,但有少数家庭携带罕见的基因改变,会显著改变这种平衡。本文研究了淀粉样前体蛋白(APP)基因中的一个罕见变体,展示了它如何大幅提升有毒蛋白片段的产生并加重称为 tau 病变的大脑纠缠过程。理解这一罕见个例能提供线索,或可广泛适用于阿尔茨海默病如何启动并加速的发展机制。
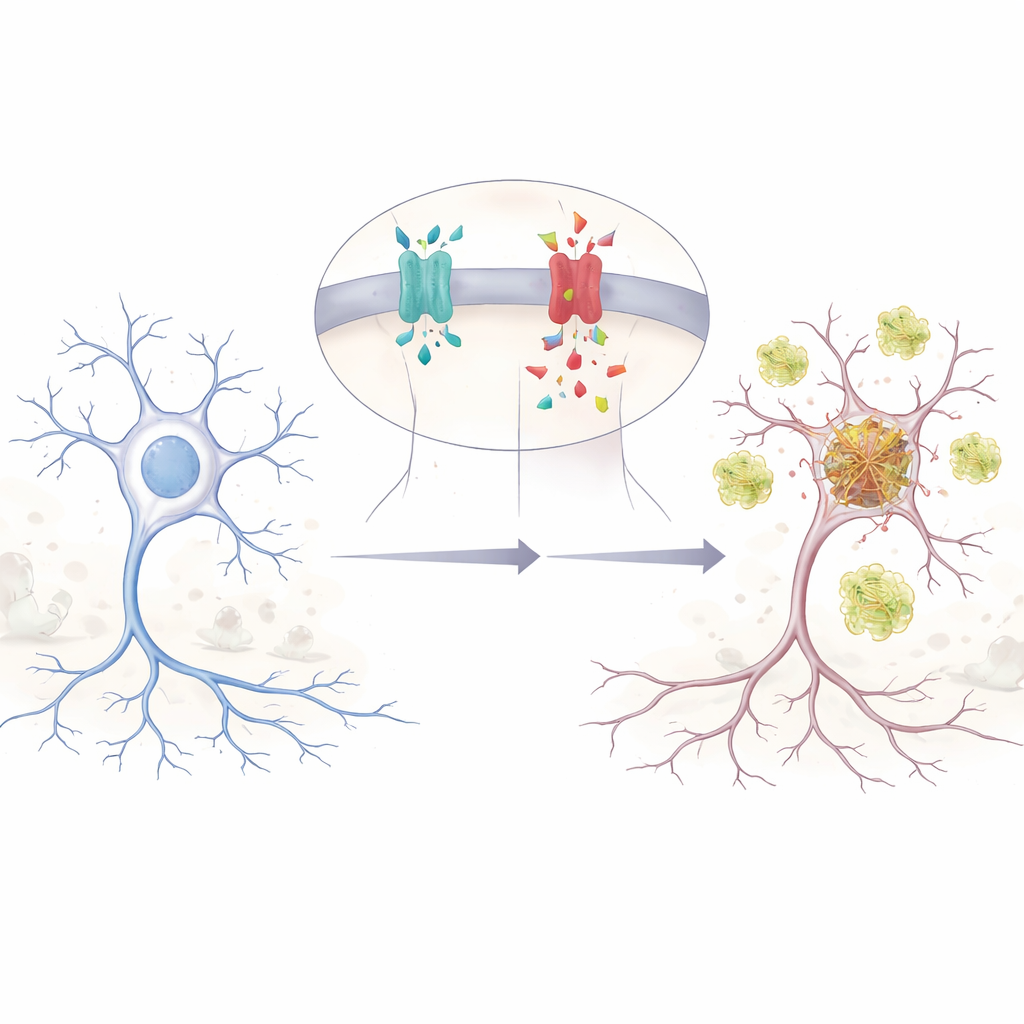
一个小小基因变化带来的大影响
作者关注的是 APP 基因中的一个单个氨基酸替换,在主要脑型 APP 中记为 E590D。此前仅在两名患者中报告过该突变,这两人均在相对年轻时确诊为阿尔茨海默病,且出现不寻常的、非常早发的记忆和行为问题。由于极为罕见,科学界不确定它是真正致病还是无关的并存变异。为弄清楚,研究团队在人体细胞和小鼠神经元中重建了该突变,并追踪 APP 被切割成各类片段的过程。他们发现,与正常 APP 在相当条件下比较时,突变型 APP 产生的淀粉样β(Aβ)肽显著增多——Aβ 长期以来被认为与阿尔茨海默病密切相关。
不是一种而是两种有毒肽
APP 可以在不同位置被切割,有点像把原木在不同点切片。经典的阿尔茨海默病通路会产生 Aβ,但另一种切割会产生较少为人知的片段 Aη。早期研究表明 Aη 会损害神经细胞之间的连接并削弱大脑巩固记忆的能力。在他们的实验中,研究者发现 E590D 突变不仅提高了 Aβ 的产生;它还强烈增加了 Aη 以及一个位于上游、可通往两条通路的前体片段。这表明该突变使 APP 的处理朝向对大脑产生双重打击的有害肽,可能在经典淀粉样斑块出现之前就扰乱脑回路。
突变如何加快细胞内运输
为了解为何产生更多有毒片段,团队研究了 APP 在细胞表面的定位与移动。生成 Aβ 的许多切割只会在 APP 被内吞入细胞后发生。通过使用标记细胞表面蛋白并追踪其内化的成像和生化方法,科学家们显示突变型 APP 在细胞外表面含量较低且被更快地内吞到细胞内室。进入早期内体后,APP 会遇到产生 Aβ 的酶,改变后的运输路径似乎给这些酶提供了更多作用机会。同时,在细胞表面的 η 位点的切割也增加,这解释了 Aη 增加的现象。
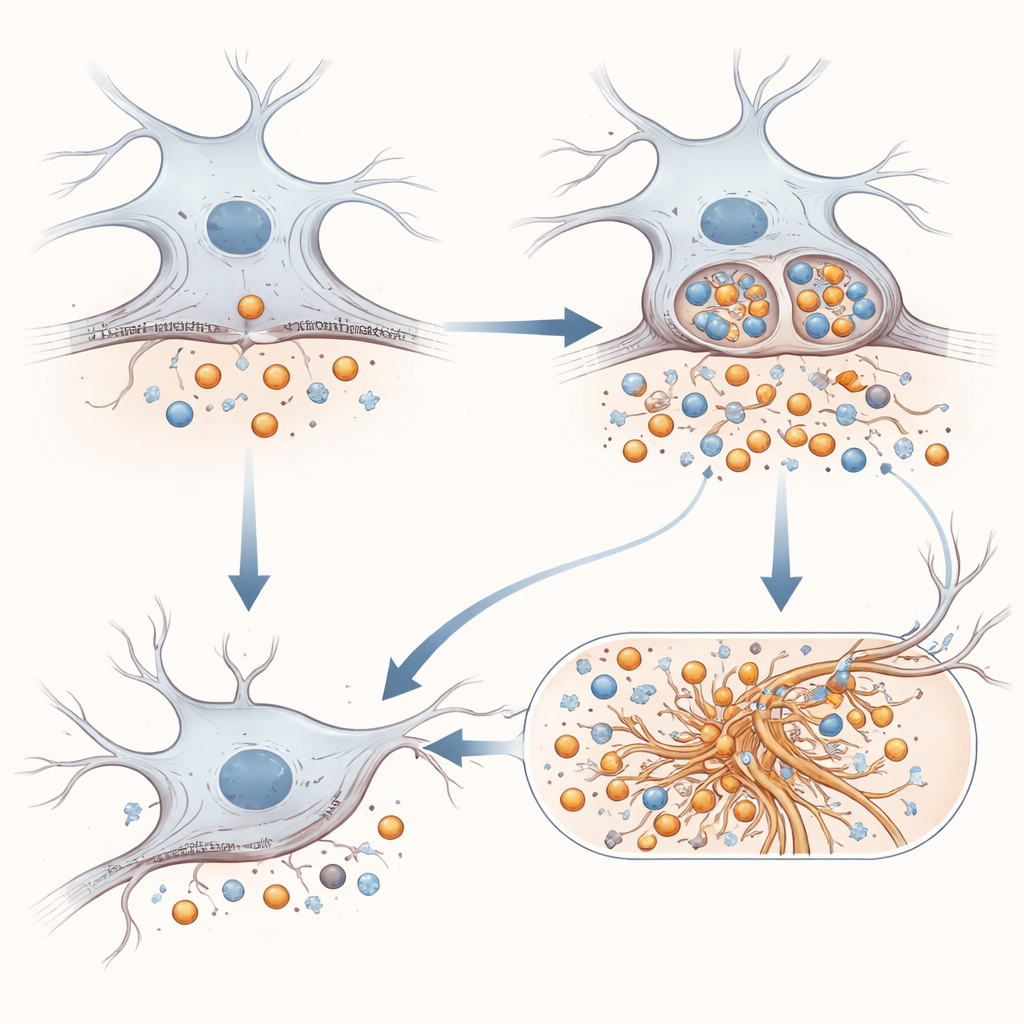
从蛋白片段到 tau 纠结与脑炎症
故事并不止于与淀粉样相关的片段。研究者检验了突变型 APP 是否会影响结构蛋白 tau,后者在多种痴呆中形成扭曲的纤维。在一种当 tau 种子促使新 tau 团块形成时会发光的细胞模型中,存在 E590D APP 会导致比正常 APP 或无 APP 时更强的聚集。在一个已易发生 tau 问题的小鼠模型中,将表达突变 APP 的病毒注入海马,使 tau 纠结加重,并引发星形胶质细胞和小胶质细胞——大脑的支持与免疫细胞——更强烈的活化。有趣的是,这些小鼠脑中常规可溶性淀粉样片段难以检测到,但一种独特的 APP 衍生片段仅在存在该突变时出现,提示活体组织中的处理方式发生了改变。
这对理解阿尔茨海默病意味着什么
综合来看,结果表明这一罕见 APP 突变并非良性。它促使 APP 产生不止一种有毒肽,加速有利于有害切割的内化步骤,并放大了大脑中的 tau 纠结与炎症反应。对非专业读者来说,核心信息是阿尔茨海默病生物学并非由单一“罪魁祸首”驱动,而是由相互作用的蛋白片段和细胞反应网络所支配。研究此类强效但罕见的基因变体可放大观察该网络的视角。本例提示,疗法可能需要同时考虑 Aβ 与诸如 Aη 的替代 APP 衍生肽及其对 tau 的综合影响,而不是孤立地靶向单一路径。
引用: Liu, T., Wetzel, L., Roy, D. et al. APP E590D mutation increases generation of Aβ and Aη peptides and exacerbates tauopathy. npj Dement. 2, 21 (2026). https://doi.org/10.1038/s44400-026-00069-9
关键词: 阿尔茨海默病, 淀粉样前体蛋白, tau 纠结, 神经炎症, 遗传突变