Clear Sky Science · zh
一种高通量、定量平台:使用2D解离的人类大脑类器官模拟阿尔茨海默病中的神经炎症
为什么感染可能与记忆丧失相关
阿尔茨海默病通常被描述为大脑中黏性蛋白的缓慢堆积,但越来越多的证据表明感染可能促使这一过程启动。本研究使用体外培养的微型人类大脑模型探讨这一想法,提出一个简单的问题:一种常见的口唇疱疹病毒能否在人体脑细胞中触发类似阿尔茨海默的变化?抗病毒药物能否将这些变化逆转或抑制?
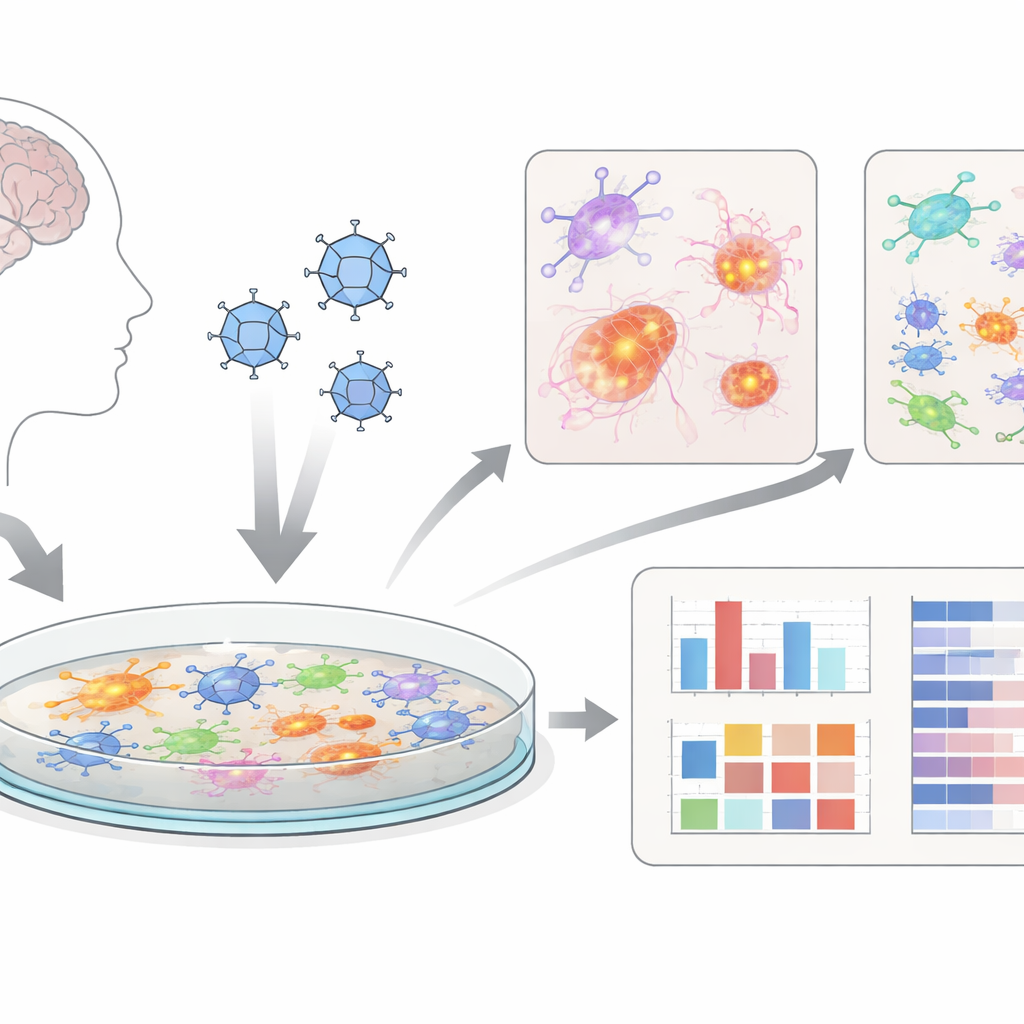
培养在平板上的迷你大脑
研究者没有仅限于动物模型,而是使用“脑类器官”——由人类干细胞生长出的类脑细胞簇。随后他们将这些三维类器官温和解离,制成含有多种脑细胞的平面混合层,包括神经元、被称为星形胶质细胞的支持细胞以及类似免疫细胞的小胶质细胞。他们称这种二维培养为dcOrgs,这类培养更容易实现均匀感染并便于高通量检测,能够同时在许多培养皿和药物条件下进行筛选。因此该系统很适合用于新疗法的筛查。
以口唇疱疹病毒作为触发因素
团队用单纯疱疹病毒1型(HSV-1)感染dcOrgs,该病毒是大多数口唇疱疹的致病因子,长期以来有人怀疑它可能在某些人群中促成痴呆。他们将受感染的培养与假处理对照、给予抗病毒药(阿昔洛韦)的培养、感染另一种病毒(甲型流感)以及经紫外线灭活的病毒进行比较。通过自动化细胞分析和单细胞测序,他们确认HSV-1能强烈感染培养皿中的多种细胞类型,而被灭活的病毒和流感病毒则产生了非常不同且较温和的变化模式。
细胞内及细胞间的阿尔茨海默样变化
在HSV-1感染的dcOrgs中,许多细胞累积了与阿尔茨海默大脑中相同形式的高含量蛋白:细胞内聚集的β-淀粉样蛋白以及多种“磷酸化”形式的tau蛋白,这些都是疾病的关键标志。这些堆积与携带病毒蛋白的细胞紧密相关,并在濒死细胞中尤为明显。同时,与较短片段相比,较长的β-淀粉样片段(Aβ42)释放到周围液体中的量减少,这种变化类似于在阿尔茨海默患者脑脊液中测得的模式。细胞群体也发生了改变:神经元数量减少,而星形胶质细胞和小胶质细胞增多,呼应了患者脑组织中观察到的神经元丧失与反应性炎症。
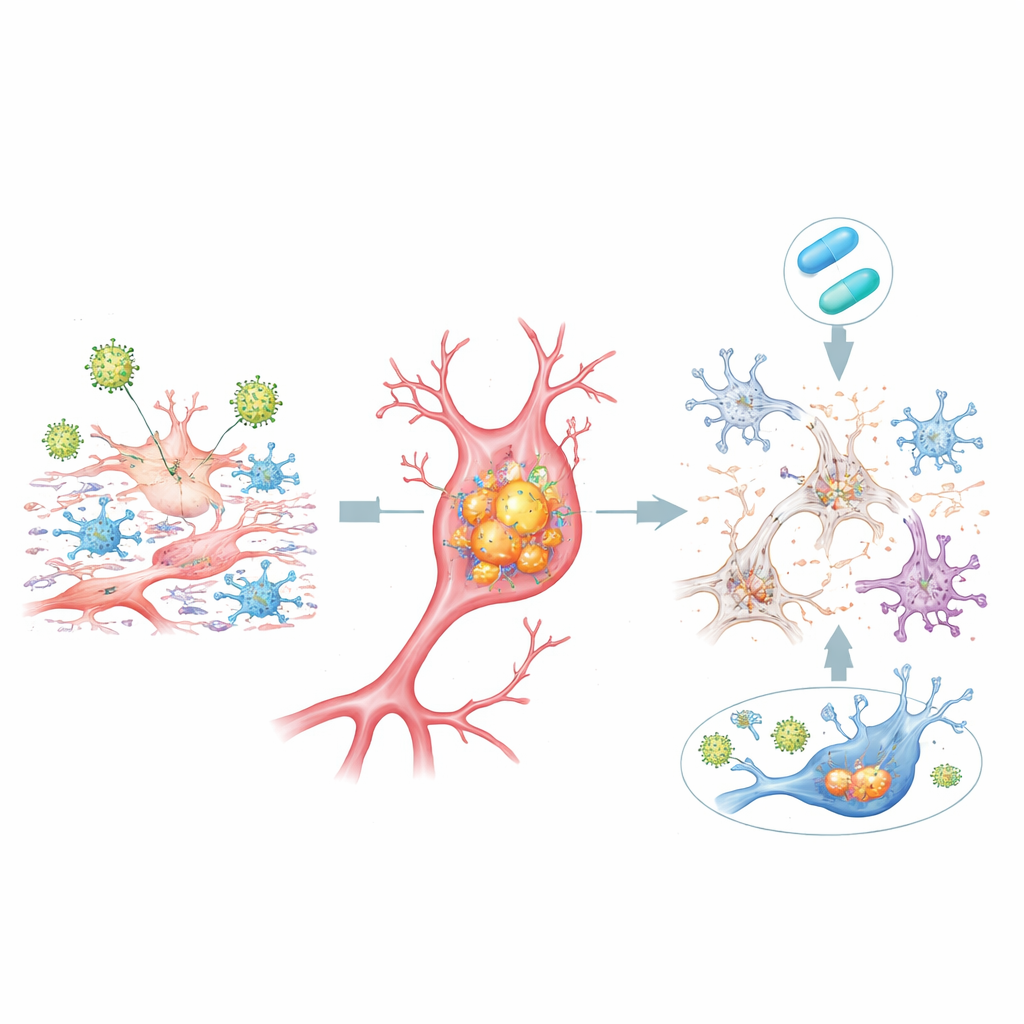
基因活性将该模型与人类阿尔茨海默联系起来
当研究者检查全基因组的基因活动时,发现HSV-1在dcOrgs中使许多先前在人类大规模遗传学研究中与阿尔茨海默风险相关的基因发生开启或关闭。这些变化在更简单的干细胞培养或流感感染的dcOrgs中并未出现,提示HSV-1与混合类脑环境之间存在特异性相互作用。单细胞测序显示,一些与阿尔茨海默相关的基因变化来自那些接触过病毒但本身几乎不含病毒遗传物质的细胞,这暗示受感染细胞释放的信号可向邻近细胞传播有害的炎症程序。
抗病毒治疗能做什么、不能做什么
在HSV-1暴露后不久加入抗病毒药物阿昔洛韦,可降低病毒基因表达、减弱多种炎症反应、降低细胞内有毒β-淀粉样蛋白和tau的堆积,并部分恢复不同细胞类型之间的平衡。相当一部分与阿尔茨海默相关基因的活性水平朝着正常方向回调。然而,并非所有变化都可逆:一大类人类基因在治疗后要么保持不变,要么甚至更受扰动,尤其是在药物对晚期病毒基因抑制效果较差时。这强调了尽管阻断病毒复制可能有益,但一旦生物学级联反应开始,单靠抑制复制未必能完全逆转。
这对理解阿尔茨海默意味着什么
对非专业读者来说,结论是:一种人类口唇疱疹病毒,在一个真实混合的人类脑细胞环境中,能够迅速产生许多阿尔茨海默病的特征——从蛋白质聚集和神经元死亡到在患者中已观测到的基因模式。这里开发的基于平面类器官的系统快速、定量且可扩展,是测试抗病毒药物及其他旨在缓解脑部炎症疗法的有力平台。尽管这并不能证明疱疹病毒在每位患者中都是阿尔茨海默的病因,但它加强了这样一个观点:对某部分人群而言,慢性或复发的病毒感染可能是病因之一的重要环节——也是潜在的预防目标。
引用: Olson, M.N., Barton, N.J., Feng, L. et al. A high-throughput, quantitative platform using 2D dissociated human cerebral organoids to model neuroinflammation in Alzheimer’s disease. npj Dement. 2, 20 (2026). https://doi.org/10.1038/s44400-026-00066-y
关键词: 阿尔茨海默病, 单纯疱疹病毒, 脑类器官, 神经炎症, 抗病毒疗法