Clear Sky Science · zh
唐氏综合征整个生命周期的白质衰老:发育起源、阿尔茨海默病进展及治疗意义
这对家庭和照护者为何重要
唐氏综合征患者的寿命比以往更长,这一令人欢迎的进步却带来了在相对年轻时阿尔茨海默病显著增加的问题。本文综述解释了被称为白质的大脑“线路”系统如何从出生前到成年晚期在唐氏综合征中发生变化,以及这些变化如何推动记忆丧失和认知问题。理解这段“线路”演变为更早的诊断和更有针对性的治疗开辟了新途径。
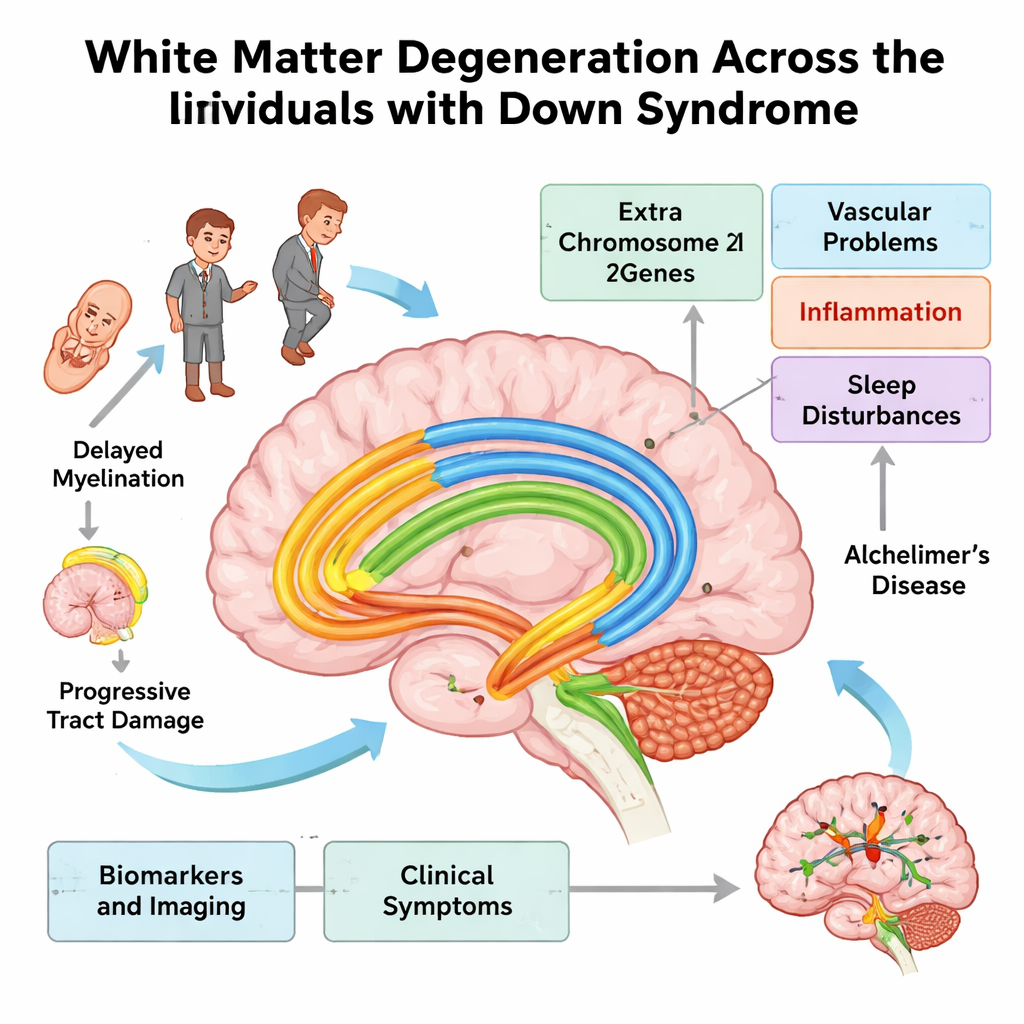
大脑的“布线”以及它如何影响思维
接近一半的人类大脑由白质构成——这些成束、绝缘的神经纤维将远距离的区域相互连接,类似于高速互联网电缆。这些纤维被一种称为髓鞘的脂质包膜包裹,由称为少突胶质细胞的支持细胞制造,使信号能够快速高效地传导。当髓鞘或其基础纤维受损时,信号传播变慢,网络失去同步,大脑需要付出更大代价。作者认为在唐氏综合征中,这种“布线”在整个生命周期内都容易受损,导致处理速度变慢、学习困难,并在晚年出现痴呆。
早期存在且未能完全弥补的布线差异
来自脑组织和儿童脑影像的证据表明,唐氏综合征的白质从一开始就以不同方式发育。对胎儿、婴儿和儿童的研究显示髓鞘形成延迟且减少,尤其在与记忆相关的区域如海马以及前后侧长程连接中。先进的磁共振成像技术证实,学龄儿童的长程联合通路已表现出较弱布线的迹象,而一些连通两脑半球的横向通路则显得异常紧凑且不成熟。这些早期的布线差异并非简单反映后期的损伤;它们代表一种内在的发育脆弱性,会随个体进入成年期持续存在。
随年龄增长与阿尔茨海默病的加速磨损
随着唐氏综合征成人的年纪增长,几乎所有人在中年前后都会出现阿尔茨海默疾病的脑部改变——淀粉样斑块和tau缠结。综述显示白质并非均匀退化;相反,特定的纤维束受到的冲击最大,尤其是那些在生命后期成熟的通路。这些包括支撑记忆和语言的长程联合纤维、连接两半球的胼胝体,以及协调运动的投射和小脑通路。MRI测量显示这些通路的纤维组织性下降、含水量增加,而在扫描上被称为白质高信号的亮点——常与小血管病和低血流相关——从30多岁中期开始迅速扩大。这些影像学变化与淀粉样蛋白堆积、反映神经损伤和炎症的血液标志物,以及认知从正常到轻度受损再到痴呆的逐步恶化紧密相关。
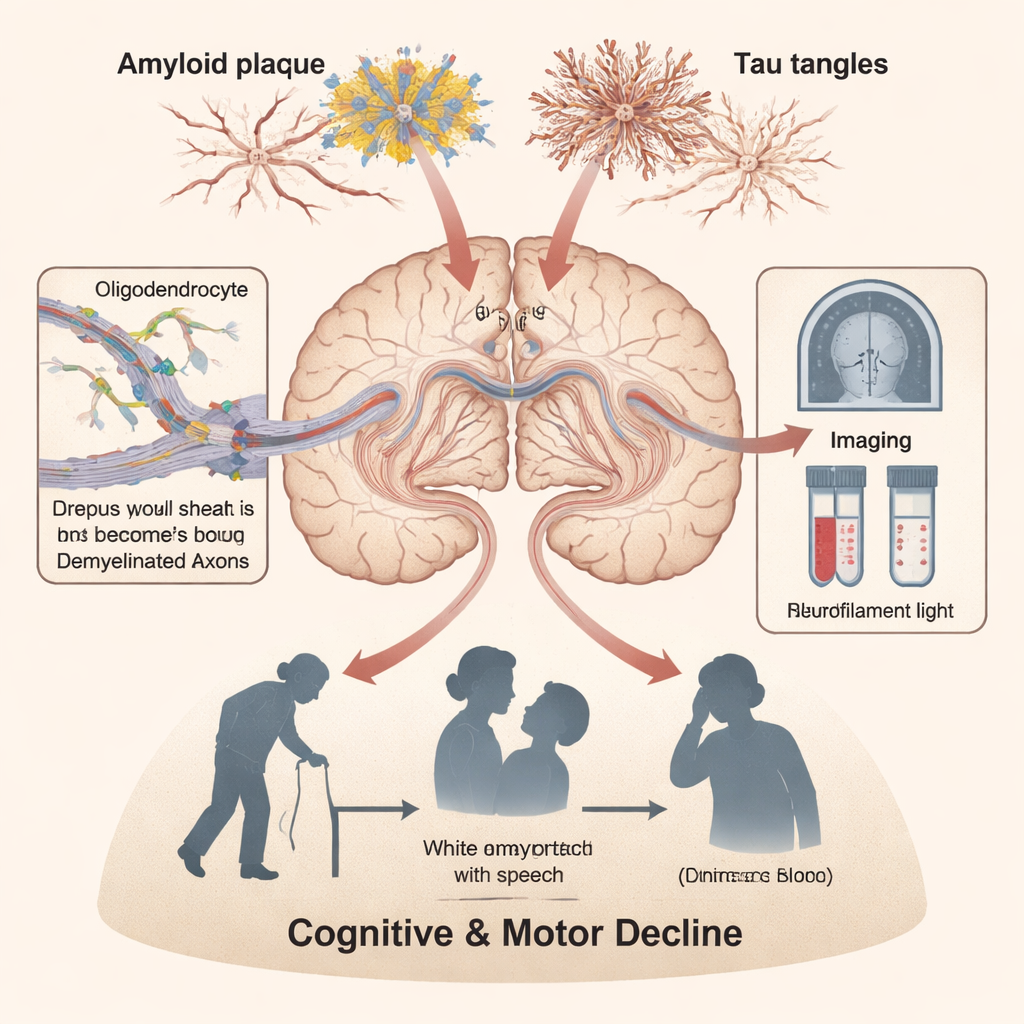
指向白质损伤的细胞、血液与生活方式线索
在细胞层面,作者描述了染色体21的额外拷贝如何改变指导少突胶质细胞发育和髓鞘形成的关键基因。在脑组织和小鼠模型中,髓鞘变薄,较少轴突被正确包裹,本应更新髓鞘系统的前体细胞显示过早老化和炎性应激的迹象。血液和脑脊液检测显示,神经丝轻链(neurofilament light)水平升高——这一在长神经纤维受损时释放的蛋白——与MRI上白质损伤高度一致。其他反映淀粉样蛋白、tau及胶质细胞活化的标志物也随白质高信号的增长而升高。诸如睡眠呼吸暂停等常见问题似乎会加重这种布线损伤,尤其影响那些支持思维与注意力的长程通路。
对治疗与早期检测的意义
作者得出结论:白质退化既是一个敏感的预警信号,也是唐氏综合征相关阿尔茨海默病中一个有前景的治疗靶点。由于布线变化在明显记忆丧失前就出现,将脑影像与如神经丝轻链等血液检测结合,可能帮助识别高风险个体并监测疾病进展速度。同时,少突胶质细胞、生物炎症、血管健康与睡眠相关的生物学机制为干预提供了多种切入点——从促进髓鞘修复或清除衰老细胞的药物,到积极治疗睡眠呼吸障碍。通过保护大脑的“布线”,有可能延缓或减轻唐氏综合征患者的痴呆,并获得对一般人群阿尔茨海默病更广泛的见解。
引用: Silva, J.A., Liou, JJ., Parikh, S. et al. White matter aging across the lifespan in Down syndrome: developmental origins, Alzheimer's disease progression, and therapeutic implications. npj Dement. 2, 16 (2026). https://doi.org/10.1038/s44400-026-00062-2
关键词: 唐氏综合征, 白质, 阿尔茨海默病, 髓鞘, 大脑衰老