Clear Sky Science · zh
在图中对功能性边进行编码以模拟肿瘤微环境中随空间变化的相互关系
为什么绘制癌症“邻里”很重要
癌症不会孤立生长。肿瘤细胞生活在一个繁忙的社区中,周围布满免疫细胞、支持细胞、血管和化学信号,这些成分在空间上紧密相邻。邻居的排列方式以及它们相互影响的强度,可能决定癌症是否扩散、对治疗是否敏感或被控制。本文介绍了SPIFEE——一种将显微图像和肿瘤的分子图谱转化为网络的新型人工智能框架,帮助研究者识别哪些细胞与通路间的相互作用与疾病类型和患者结局最相关。
将组织转成网络地图
现代癌症研究能测量的远不止显微镜下的形态。有些方法在单个细胞上标记数十种蛋白,另一些提供组织结构的详细彩色切片,而更新的工具则记录在肿瘤切片上成千上万个位置的基因活性。SPIFEE将这些视为同一“邻里”的不同视角。它把每个样本表示成一个图:节点代表肿瘤微环境中的关键实体——例如细胞类型、视觉组织模式或分子通路——而边则捕捉这些实体在空间上的相互作用。关键在于,SPIFEE并不把相互作用简化为像“距离”这样的单一数值;相反,每条边储存一条小曲线,描述两个实体在一定距离范围内如何相互混合或排斥,从而保留更丰富的空间细节。
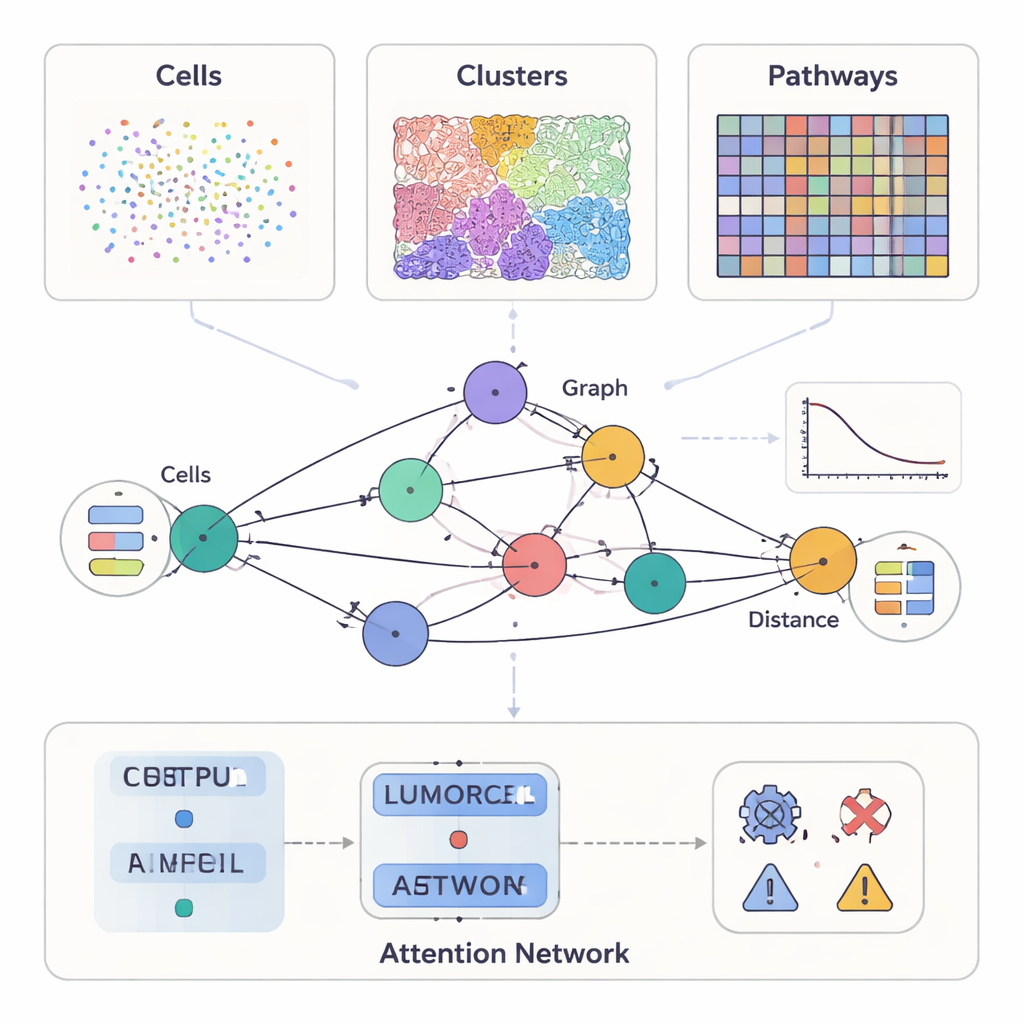
一种能适配多类癌症数据的灵活视角
作者在多个大型独立的癌症数据集上测试了SPIFEE,涵盖不同技术和尺度。在用多重免疫荧光标记的胰腺病变样本中,图中的每个节点代表一种细胞类型,节点特征来自单细胞RNA测序,概括了这些细胞常见的通信方式。在用常规苏木精-伊红(H&E)染色的肺癌切片中,节点代表由自监督学习系统自动发现的反复出现的视觉组织模式。在第三种情形中,常规肺癌切片被深度学习工具转化为虚拟的空间转录组学,SPIFEE的节点代表诸如缺氧、雌激素或JAK–STAT信号等分子通路,其特征来自基因活性。在所有这些设置中,相同的框架都能接纳不同类型的节点并构建可比较的空间图。
找到区分健康结局的相互作用
一旦SPIFEE构建了图,就将其输入图注意力网络(一种神经网络),该网络不仅学习预测结局——例如癌症亚型、存活风险或疾病与非癌症性炎症的区分——还能够突出显示对预测最重要的边。在胰腺组织中,SPIFEE以比早期基于图的方法更高的准确率区分慢性胰腺炎与胰腺导管腺癌。模型持续关注涉及上皮(类肿瘤)细胞与调节性T细胞、抗原呈递细胞以及辅助性T细胞的相互作用,指向在癌症中比在炎症中更突出的免疫抑制性邻里。在肺腺癌切片中,SPIFEE识别出某些基质-肿瘤模式,其相互作用与更好或更差的生存相关,提示肿瘤与支持组织之间的“边界带”携带重要的预后线索,常规分析可能会遗漏这些信息。
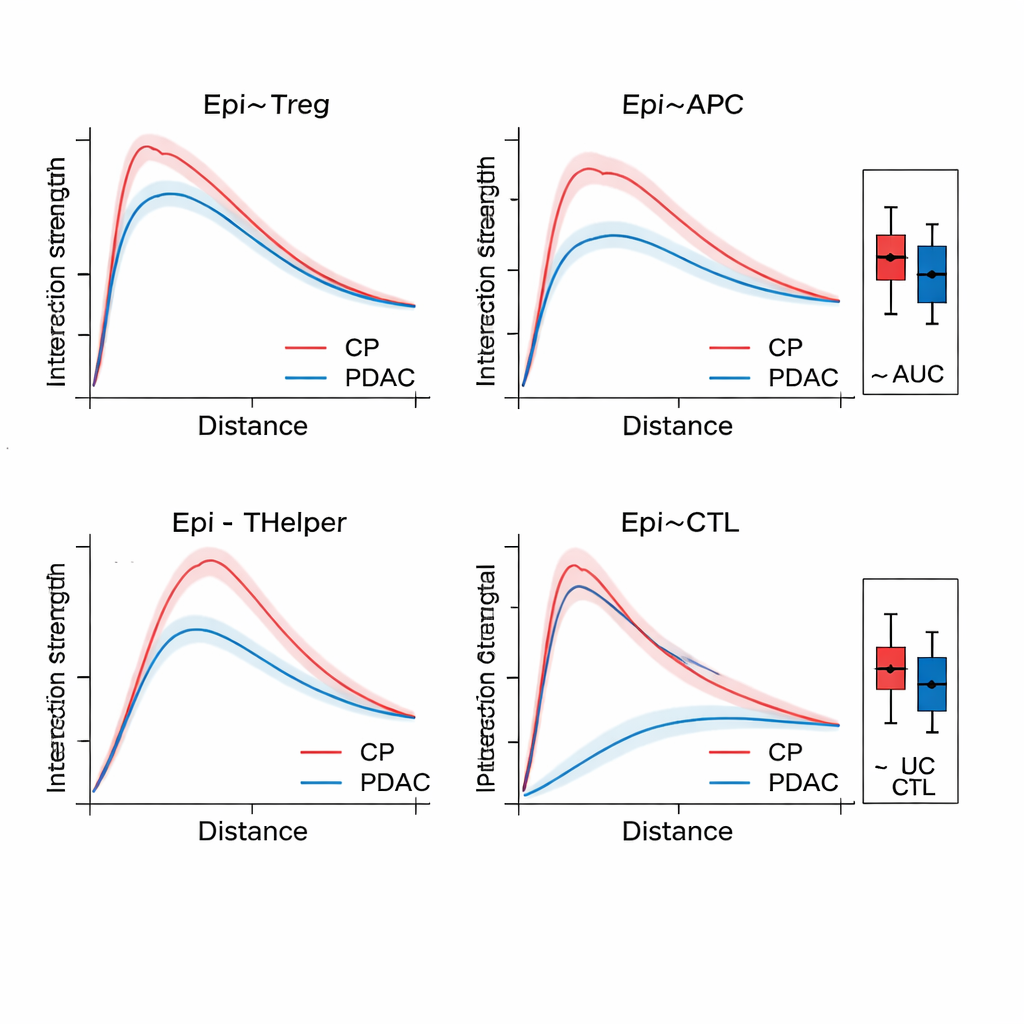
从常规切片读取分子间的串扰
也许最引人注目的是,一旦将常规病理图像转化为预测的基因活性图,SPIFEE便能推断出有意义的通路相互作用。通过将通路视为节点并将其空间共现性作为功能性边,这种方法突出显示了诸如缺氧与EGFR、JAK–STAT与PI3K等配对——这些组合已知在肺癌中驱动免疫逃逸和耐药。它还提升了肺腺癌中的雌激素相关通路以及鳞状癌中的某些免疫和应激通路的相关性,这些发现与总体RNA测序以及独立的真实空间转录组数据集中的模式一致。这表明,即便分子测量是近似的,常规切片中的空间模式仍包含可恢复的关于关键通路如何在活肿瘤中相互作用的信号。
这对未来癌症护理意味着什么
对非专业读者来说,核心信息是SPIFEE提供了一种从图像和分子图谱中直接解读癌细胞“社交生活”的新方法。通过对关系随距离变化的方式进行编码,而不是将其压缩为单一分数,并使用基于注意力的神经网络对重要相互作用进行排序,该框架能够发现区分癌症类型并预测生存的细胞、组织模式和通路组合。尽管这些发现仍需生物学和临床层面的验证,但像SPIFEE这样的做法指向了一个未来:常规肿瘤样本不仅能提供静态快照,还能产生交互热点的动态地图,帮助指导诊断、风险分层,并最终支持个性化治疗选择。
引用: Tsang, A.P., Krishnan, S.N., Kulkarni, R. et al. Encoding functional edges in graphs to model spatially varying relationships in the tumor microenvironment. npj Artif. Intell. 2, 27 (2026). https://doi.org/10.1038/s44387-026-00075-5
关键词: 肿瘤微环境, 空间转录组学, 图神经网络, 癌症病理学, 细胞-细胞相互作用