Clear Sky Science · zh
使用扩散模型进行受相互作用约束的三维分子生成,促进基于结构的药效团建模以支持药物设计
为什么设计更好的药物如此困难
现代药物发现往往依赖于让小分子像钥匙般嵌入蛋白质的锁孔。但钥匙不仅要契合:还必须形成一系列正确的微小吸引力——例如微弱的电性吸引和疏水区的相互排斥——从而使药物能够既强烈又特异性地结合。化学空间极为庞大,远超当今数据库所包含的范围,因此研究者在寻找更聪明的方法以从头发明新钥匙,同时保持这些关键接触模式。
教会计算机什么才是真正重要的
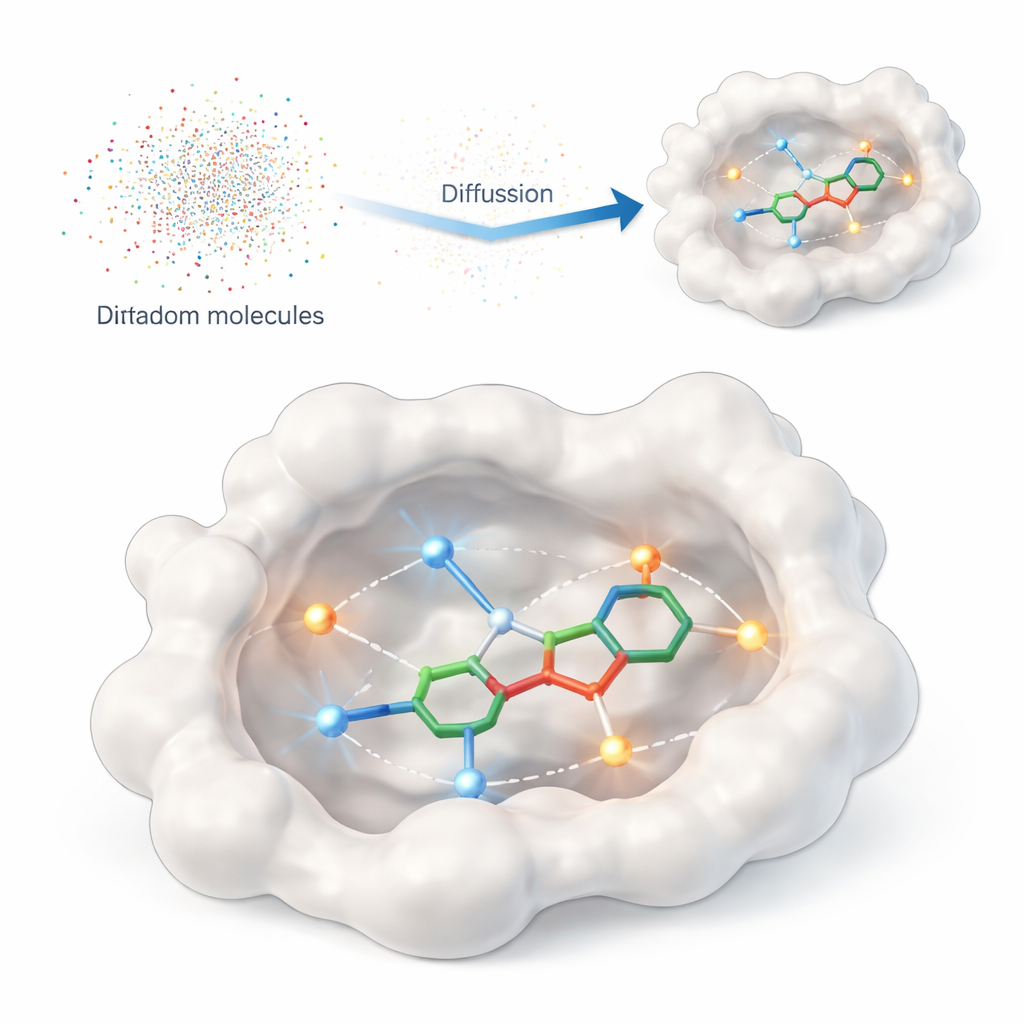
这项研究提出了 DiffPharma,一种在蛋白结合位点内直接生成三维类药小分子的计算框架。DiffPharma 不再要求算法在巨量现有化合物目录中检索,而是逐原子创建新分子,生成过程由它们与蛋白质应当形成的相互作用来引导。该方法建立在一种现代生成模型——扩散模型之上,这类模型从随机噪声开始,逐步“去噪”形成有结构的对象——在本例中,即嵌入蛋白口袋的三维分子。
编码蛋白质的“握手”
为了告知模型蛋白表面上哪些事项重要,作者将关键接触表示为沿蛋白质与参考分子之间路径散布的小型“相互作用粒子”。强调了两类常见的相互作用:氢键,像定向磁体般连接特定原子;以及疏水接触,指油性区域聚集并避开水环境。独立的神经网络学习每种相互作用类型的几何与化学特征,以及结合口袋的整体形状,然后一种特殊的融合架构将这些视角合并为单一的、连贯的指导图景,从而引导分子生成。
它在多大程度上模拟真实的结合模式?
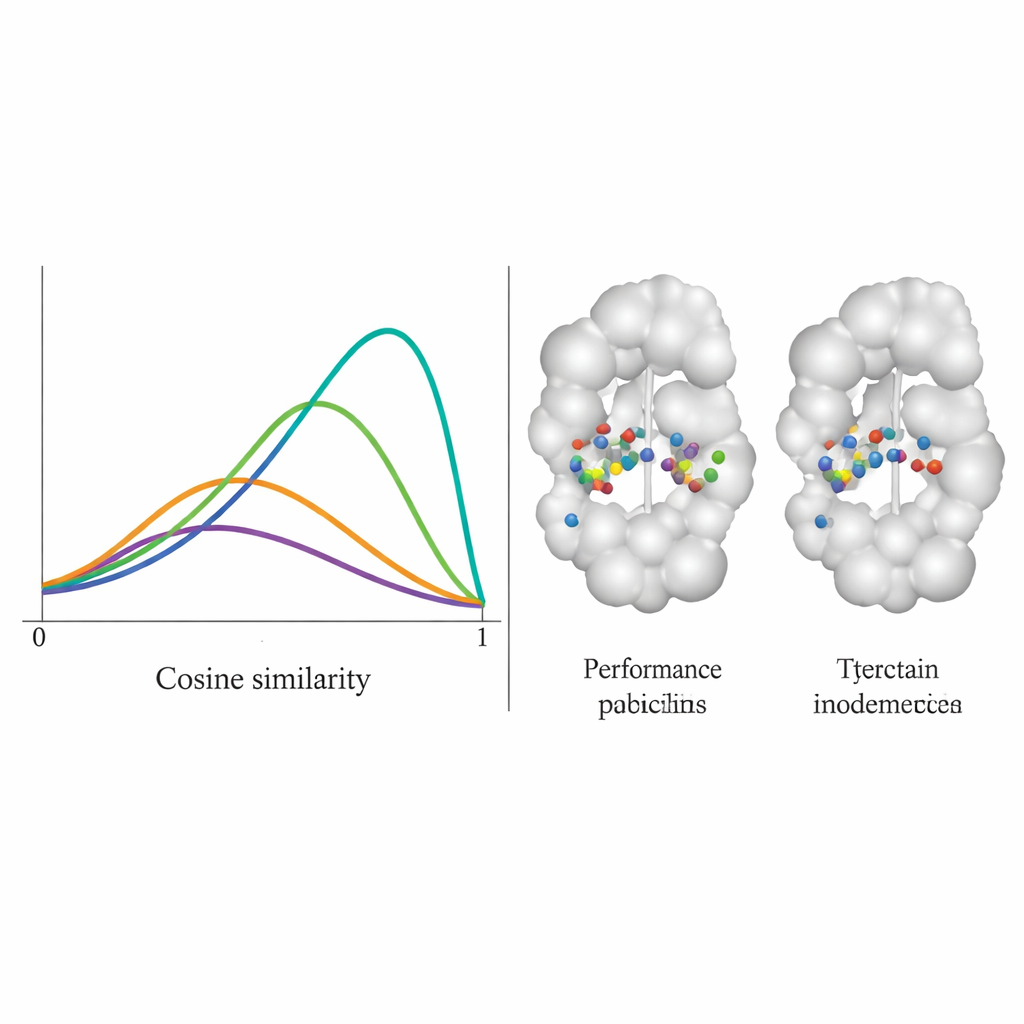
团队在 100 对不同的蛋白-分子复合体上测试了 DiffPharma,评估新生成分子在残基逐一层面上复制原始接触模式的忠实度。他们使用 0 到 1 的余弦相似度得分来衡量,1 表示完全一致。DiffPharma 的得分分布在约 0.9 附近达到峰值,意味着平均来看,相同的蛋白残基形成了与参考结构中相同类型的关键相互作用——显著优于六种竞争方法。值得注意的是,模型在实现此结果的同时仍产生了多样的分子形状,且生成化合物保留了与真实稳定分子相匹配的合理键长、键角和整体三维几何。
从理论走向可行的药物先导
在基准测试之外,作者还考察了 DiffPharma 是否能为实际靶点设计出可信的候选药物。针对两种研究透彻的酶——AKT 激酶和与抗生素抗性相关的 β-内酰胺酶——该方法生成了保留已知配体关键相互作用模式但常常采用不同化学骨架的分子,这是一种在药物化学中受欢迎的“骨架跳跃”。在对 SARS-CoV-2 主蛋白酶的更高要求的案例研究中,DiffPharma 在特定相互作用约束下生成分子,并使用分子动力学模拟和结合能估算进行评估。在更严格的相互作用约束下生成的分子形成了更稳定的复合体,有时其预测的结合能优于已知的参考抑制剂。值得注意的是,系统甚至在训练集中从未出现过该参考化合物时,单凭蛋白结构和相互作用指令就重新发现了该参考分子。
这对未来药物意味着什么
对非专业人士而言,DiffPharma 可以被视为一种智能且具三维感知能力的药物分子设计工具:给定蛋白口袋的形状和期望的“握手”模式,它提出化学上合理、契合且以正确方式相互作用的钥匙。尽管它尚未同时优化药物所需的所有性质,例如溶解性或代谢特性,该方法能可靠地保留蛋白表面的关键接触图并探索超出现有目录的新化学空间。这种以相互作用为指导的方法可能帮助研究者更快地从与疾病相关蛋白的结构数据出发,得到多样且现实的实验药物开发起点。
引用: Sako, M., Yasuo, N. & Sekijima, M. Interaction-constrained 3D molecular generation using a diffusion model enables structure-based pharmacophore modeling for drug design. npj Drug Discov. 3, 8 (2026). https://doi.org/10.1038/s44386-026-00040-x
关键词: 基于结构的药物设计, 分子生成模型, 药效团建模, 蛋白-配体相互作用, SARS-CoV-2 主蛋白酶