Clear Sky Science · zh
用于虚拟筛选和化合物效能预测的 AI 指导竞争对接
更聪明的新药搜索
寻找新药有点像在由数百万种分子构成的干草堆里找针。该研究展示了人工智能的最新进展如何通过帮助科学家预测哪些分子最有可能附着在与疾病相关的蛋白上并实际成为药物,使这类搜索更快、更便宜。作者并不是在实验室里逐一测试化合物,而是使用 AI 模型在分子之间进行虚拟竞赛,让胜出者脱颖而出。
AI 如何学会看分子的锁与钥匙契合
许多现代药物通过嵌入蛋白上的微小口袋起作用,就像钥匙嵌入锁中一样。传统上,计算程序试图用物理方程估算原子之间的相互力来预测这种契合。然而在过去几年里,称为基于扩散的共同折叠模型(例如 AlphaFold3 和 Boltz)的新型 AI 系统从大量已知的蛋白–分子结构中学习。即使没有实验结构,这些系统现在也能“想象”蛋白与潜在药物如何在三维中共同折叠。作者要解决的核心问题是,这些 AI 工具能否不仅仅画出看似合理的图像——还能否把好药与坏药区分开来?
真实结合者与伪装者
研究团队首先测试了 16 种研究充分的蛋白,以及一种更复杂的细菌酶—— DNA 回旋酶。对每种蛋白,他们要求 AI 模型将已知的活性抑制剂和一组无关的“非靶向”分子放入相同的结合位点。与其只信任单次预测,他们考察了 AI 在多次运行中对每个分子的放置是否一致。真正的抑制剂倾向于反复回到相同的位置和方向,聚集在彼此之间仅几万亿分之一米的范围内。无活性的分子则游走更广,常常距离口袋更远。这个简单的想法——构象收敛——被证明是化合物确实适配其蛋白靶点的强有力信号。
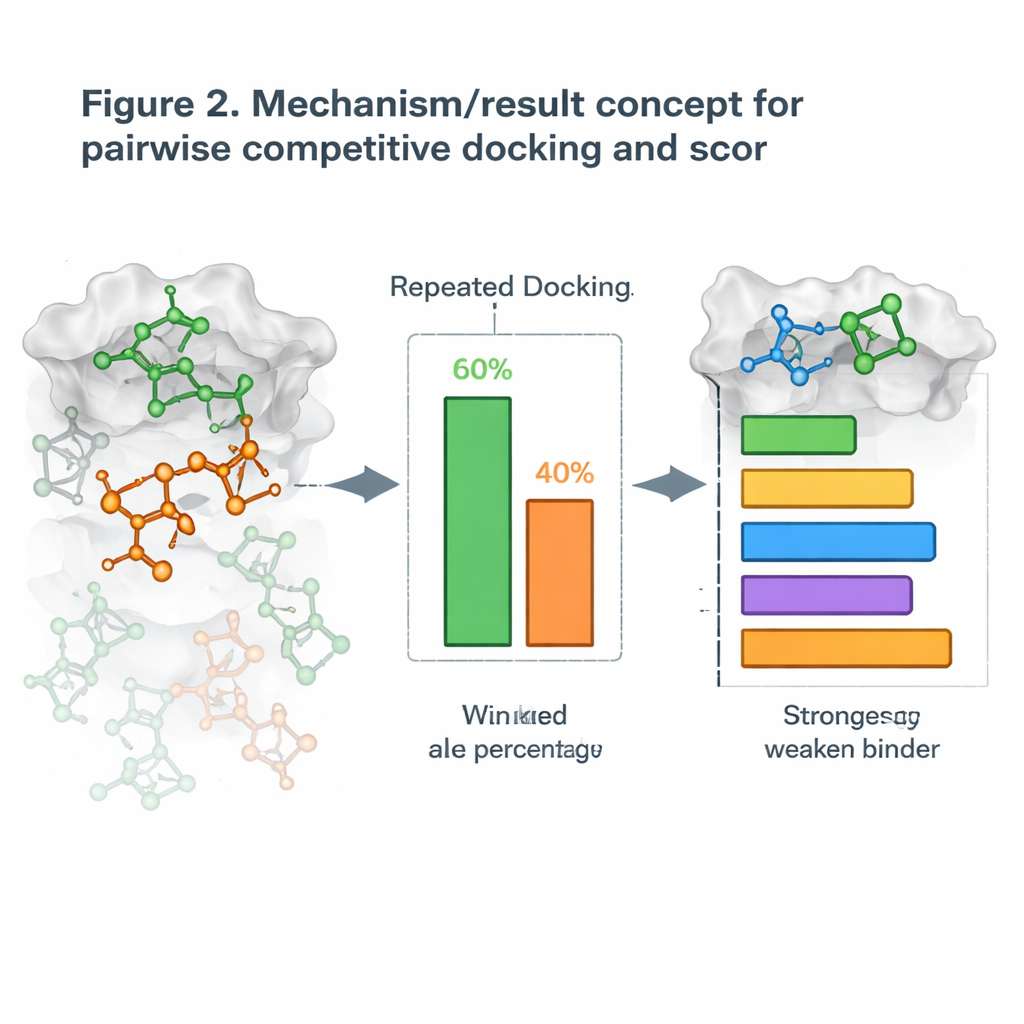
将对接变成一对一的正面交锋
在此基础上,作者引入了一种称为成对竞争对接的新策略。他们不是一次对接一个分子,而是将两个候选分子与蛋白一起对接,让它们在相同的口袋中“竞争”。经过多次重复运行,占据该位点更频繁的分子被判为该回合的胜者。通过对所有可能的配对运行,他们构建出胜负表并为每个分子计算竞争对接得分,就像在循环赛中对选手排名一样。当这些得分与分子抑制其靶标强度的实测数据比较时,排名常常吻合,有些蛋白体系甚至显示出近乎完美的一致性。
从虚拟筛选到更好抗生素的设计
作为详细案例,作者选择了对细菌至关重要的酶 DNA 回旋酶。该蛋白具有多个被不同类别抗生素靶向的药物口袋,包括广泛使用的氟喹诺酮类。AI 模型通常能够将每类药物放入其正确的口袋,竞争对接得分大致反映了它们的实测效力。随后,作者将规模扩大到对 3000 多种获批药物的虚拟筛选,询问哪些分子最能在氟喹诺酮位点上竞争。他们的两步策略——先用“同时竞争”挑选可能的胜出者,再按分子在口袋中聚集的紧密程度筛选——大大富集了真正的氟喹诺酮类并剔除了较弱的候选物。最后,他们使用 AI 驱动的分子生成器提出新的类似氟喹诺酮的结构,并用竞争对接找出少数预测结合更好且具有可接受药物样特性的候选。
承诺、局限与对病患的意义
该研究表明,现代 AI 模型不仅能绘制出合理的蛋白–药物结构:在竞争框架下运行时,它们还能帮助以常与实验数据相呼应的方式对化合物进行排序。这并不能替代实验室工作——性能仍然高度依赖特定蛋白,有些口袋会被错误预测,AI 模型对非常大或非典型分子也可能失败。但随着这些模型及其训练数据的改进,像成对竞争对接这样的策略可能会使早期药物发现更加高效。对患者而言,这最终可能意味着更快地开发出有针对性的药物,包括能跟上耐药性细菌发展的新抗生素。
引用: Mirgaux, M., Barcelli, V., Chua, A.C.Y. et al. AI-guided competitive docking for virtual screening and compound efficacy prediction. npj Drug Discov. 3, 6 (2026). https://doi.org/10.1038/s44386-026-00039-4
关键词: AI 药物发现, 虚拟筛选, 分子对接, 蛋白-配体结合, 抗生素设计