Clear Sky Science · zh
偏重刺激 HER4 可保留脑源性促生长因子诱导的心肌功能改善
为衰竭心脏带来新希望
心力衰竭影响全球数百万人,即便在现有最优药物治疗下病情也常常持续恶化。本研究探索了一种新型生物药物 JK07,旨在帮助心脏自我修复,同时回避一个严重顾虑:意外促进潜在癌症的生长。研究者通过调整心脏中的天然修复信号并将其引导远离与癌症相关的通路,力图把有益效果送达而把风险排除在外。
心脏自身修复信号如何工作
工作重点是神经调节素‑1(NRG‑1),这是一种体内产生的蛋白,帮助心肌细胞生长、生存并从损伤中恢复。NRG‑1 通过细胞上的对接位点 HER3 和 HER4 传递指令。当 NRG‑1 与这些受体结合时,它们与名为 HER2 的伙伴配对并启动细胞内的生存与修复信号。先前在动物和人体的研究中,用重组 NRG‑1 可显著增强心脏的泵血功能,但也伴随消化不适和肝脏问题等副作用。更令人担忧的是,HER3 已知驱动多种癌症的生长,这引发对长期 NRG‑1 治疗可能唤醒隐匿肿瘤的担忧。
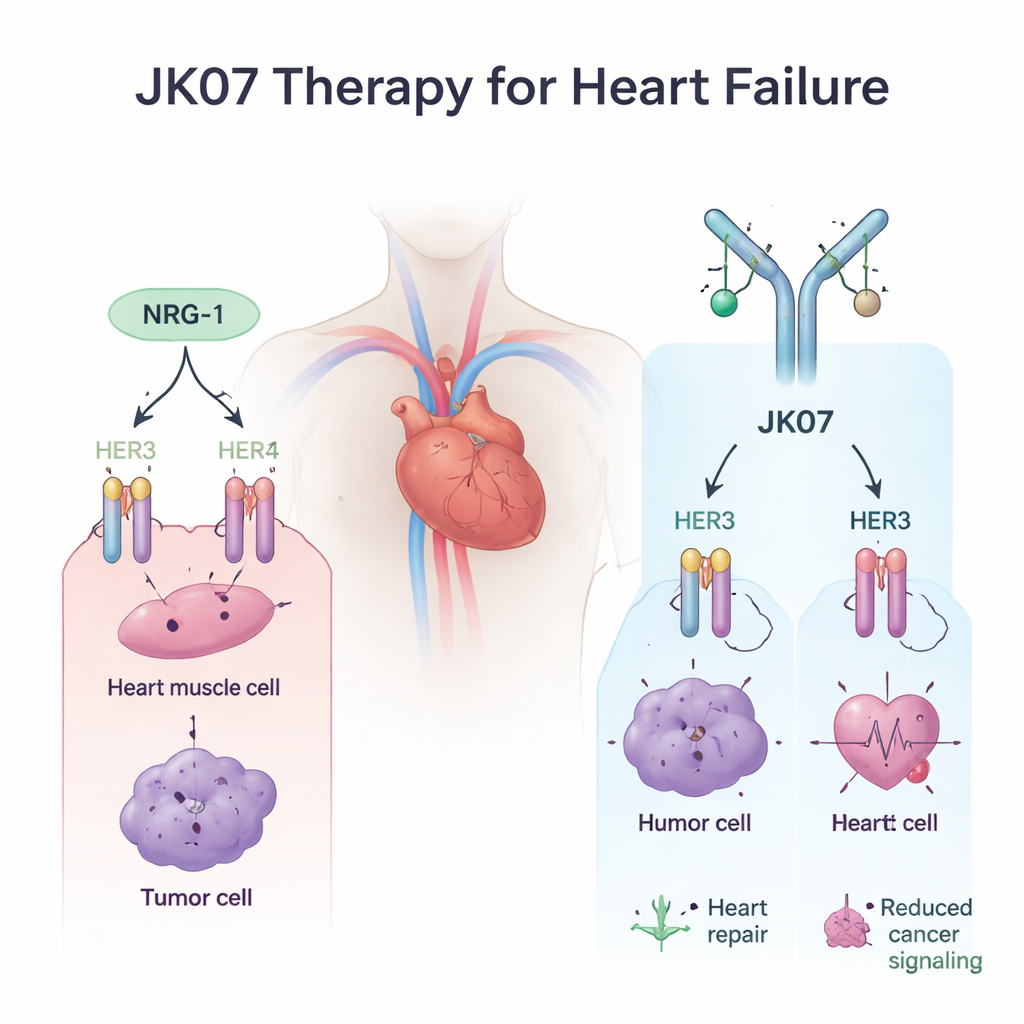
带有安全锁的设计分子
为了解决这一问题,研究人员设计了 JK07,这是一种由两个经过精心挑选部分融合而成的分子。一端是完全人源化的抗体,用来阻断与癌症相关的受体 HER3;另一端是 NRG‑1 的活性片段,作为双份连接,以便仍能作用于心脏细胞。在体外实验中,JK07 能牢固结合 HER3,同时保持 NRG‑1 片段的正确折叠和活性。在依赖 HER3 的癌细胞体系中,JK07 显著抑制了需 HER3 的信号传导,使细胞生长较纯 NRG‑1 处理时更为缓慢;在携带 HER3 驱动肿瘤的小鼠中,其对肿瘤有剂量依赖性的缩小作用。这些发现表明,抗体部分确实对 HER3 起到了安全锁的作用。
保留对心脏有利的信号
更为关键的是,JK07 仍需保留与心脏修复主要相关的受体 HER4 的益处。利用专门的细胞系和由人类干细胞分化得到的心肌细胞,研究团队显示 JK07 可促使 HER4 与 HER2 配对并激活心肌细胞内一个关键的保护性通路——AKT,其强度与未经改造的 NRG‑1 相当。大鼠心肌细胞也呈现相同反应。换言之,JK07 并未削弱心脏的救援信号;它只是将该信号从 HER3 重定向到 HER4。
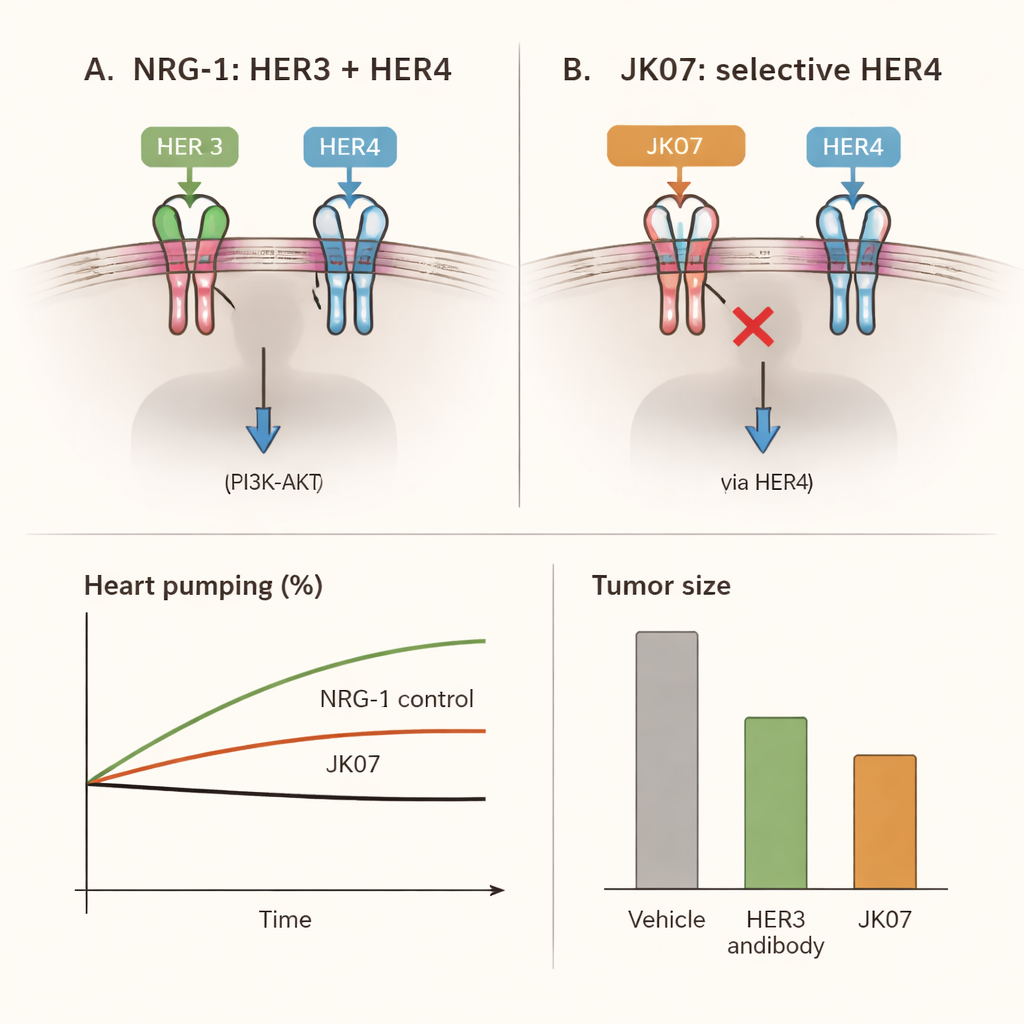
从啮齿动物到猴子:JK07 对心脏的作用
随后研究人员探问这种选择性信号是否真的能拯救衰竭心脏。在经手术诱导心肌梗死的大鼠中,心脏泵血能力下降约三分之一,近似模拟人类的心力衰竭。接受为期四周、多次 JK07 治疗的动物表现出明显恢复:射血分数(衡量每次心跳心脏排出血量的标准指标)相比治疗前提高了最多约三分之一。扩大了的心腔回缩至接近正常,受损区域的瘢痕相关胶原减少,心肌的显微结构更为有序与健康。这些改善与一种不阻断 HER3 的对照 NRG‑1 基药物所见相当,表明仅刺激 HER4 就足以带来心脏益处。
更接近临床:猴子心力衰竭中的结果
为在更贴近人类疾病的动物模型中检验 JK07,团队研究了自然发生长期心力衰竭的中年恒河猴(猕猴),包括射血分数降低型(HFrEF)和舒张功能受限型(HFpEF)。在抽搐泵功能减弱的猴子中,两项独立研究显示每周一次的 JK07 输注使大多数动物的射血分数至少提高 5 个百分点,有些动物接近 20 个百分点的绝对改善——与使用已上市药物沙库巴曲/缬沙坦的动物相似。在主要问题为心室充盈与松弛功能障碍的猴子中,JK07 在大多数动物中改善了舒张功能分级,而沙库巴曲/缬沙坦仅偶尔见效。总体来看,在所测试剂量下未出现重大安全性问题。
这对患者意味着什么
对非专业读者来说,关键信息是:这项研究表明可能以更有针对性且更安全的方式利用心脏自身的修复系统。JK07 的设计是刺激支持心脏修复的“良性”受体(HER4),同时阻断与癌症相关的“风险”受体(HER3)。在啮齿动物和猴子中,这一选择性策略改善了心脏泵血功能、减少了结构性损伤和瘢痕,并在癌症模型中显示了抗肿瘤活性。尽管仍需通过人体试验来确认其疗效和长期安全性,JK07 指向了一个可能使心力衰竭治疗既更有效又更少促癌风险的未来。
引用: Murphy, S.L., Tang, W.H.W., Zhuang, X. et al. Preferential HER4 stimulation preserves neuregulin-induced improvement of myocardial function. npj Drug Discov. 3, 10 (2026). https://doi.org/10.1038/s44386-026-00038-5
关键词: 心力衰竭, 神经调节素‑1, HER4, 生物治疗, 心脏重塑