Clear Sky Science · zh
通过受逻辑约束的基因-通路异质知识图从组织病理图像推断信号通路异常
在癌症切片中看见隐匿的细胞信号
当医生在显微镜下检查癌症时,主要看到的是形状和颜色,而非细胞内正在进行的复杂分子“对话”。然而,这些基因与通路之间看不见的信号“对话”往往决定了肿瘤如何生长以及对治疗的反应。本研究提出了一种新的人工智能系统,它读取常规病理图像并推断哪些细胞通信通路(即通路)出现异常——提供了一种在不做额外实验室检测的情况下窥见分子行为的方法。
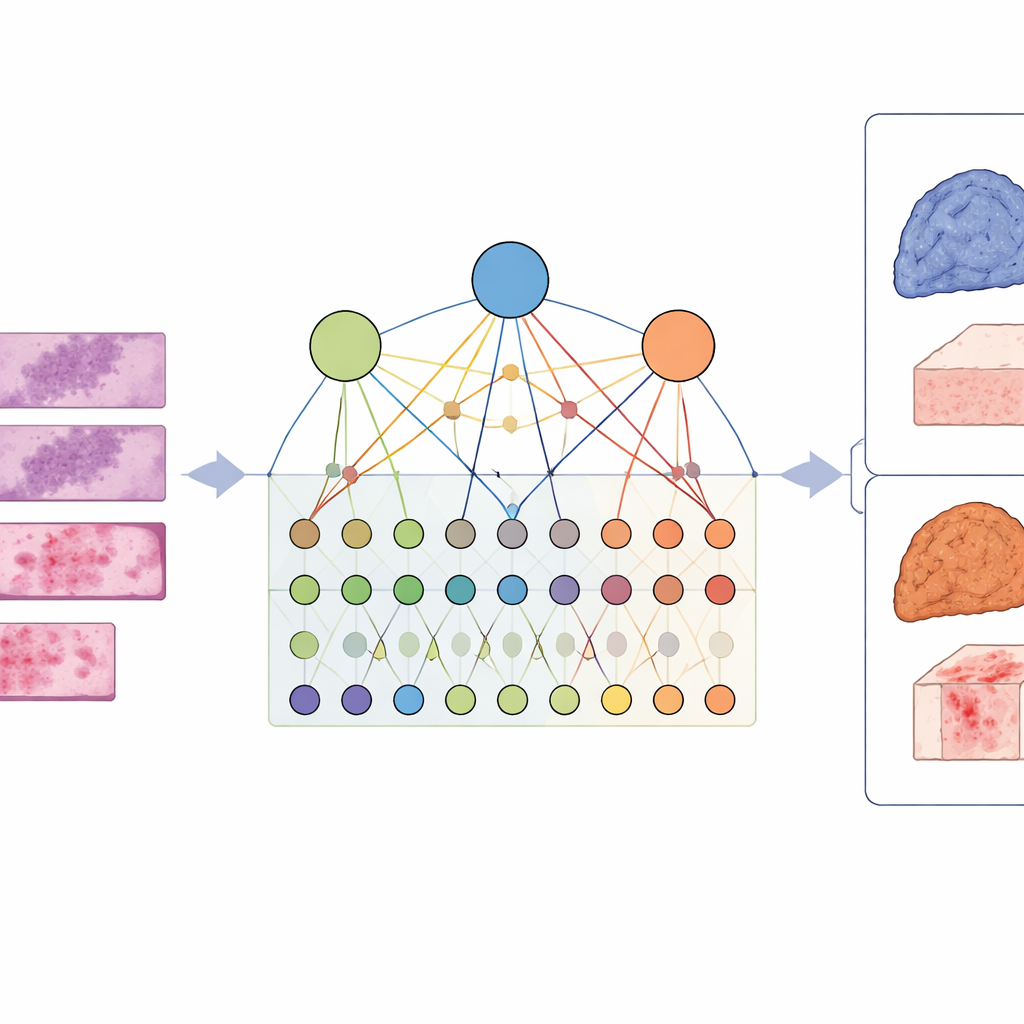
从单基因线索到更宏观的图景
传统方法试图从组织图像预测单个基因的状态:某个特定基因是否发生突变?这固然有用,但癌症很少仅依赖单一异常基因。相反,基因群体协同作用,扰乱控制生长、生存和免疫的整条信号通路。作者认为,专注于单一基因会忽略这种协作行为,无法解释肿瘤在显微镜下的形态与行为。
在图像、基因与通路之间构建映射
为捕捉这种复杂性,研究者设计了一个称为 LCG-HGNN 的框架,将三层信息连接起来。首先,他们将每张肺腺癌整片图像切成许多小补丁,并将这些补丁表示为图,其中相邻或外观相似的区域相互连接。其次,他们利用已有的生物数据库将基因标记与信号通路连接,构建第二个图以编码哪些基因属于哪些通路。最后,他们让 AI 模型在这个组合图上传播信息,使图像模式、基因和通路相互影响,而不是各自为政。
把已知生物学教给系统
一个关键创新是模型不允许完全自由学习而无约束。作者将源自数十年癌症研究的明确、类规则性陈述嵌入模型中。例如,有些突变几乎不会在同一肿瘤中共存,某些通路处于其他通路的上游或下游。他们将这些规则编码为逻辑约束,温和地引导 AI 的内部连接与预测。如果模型提出与已知生物学或病人切片间相似性冲突的基因与通路组合,这些规则会促使其向更现实的备选方案修正。
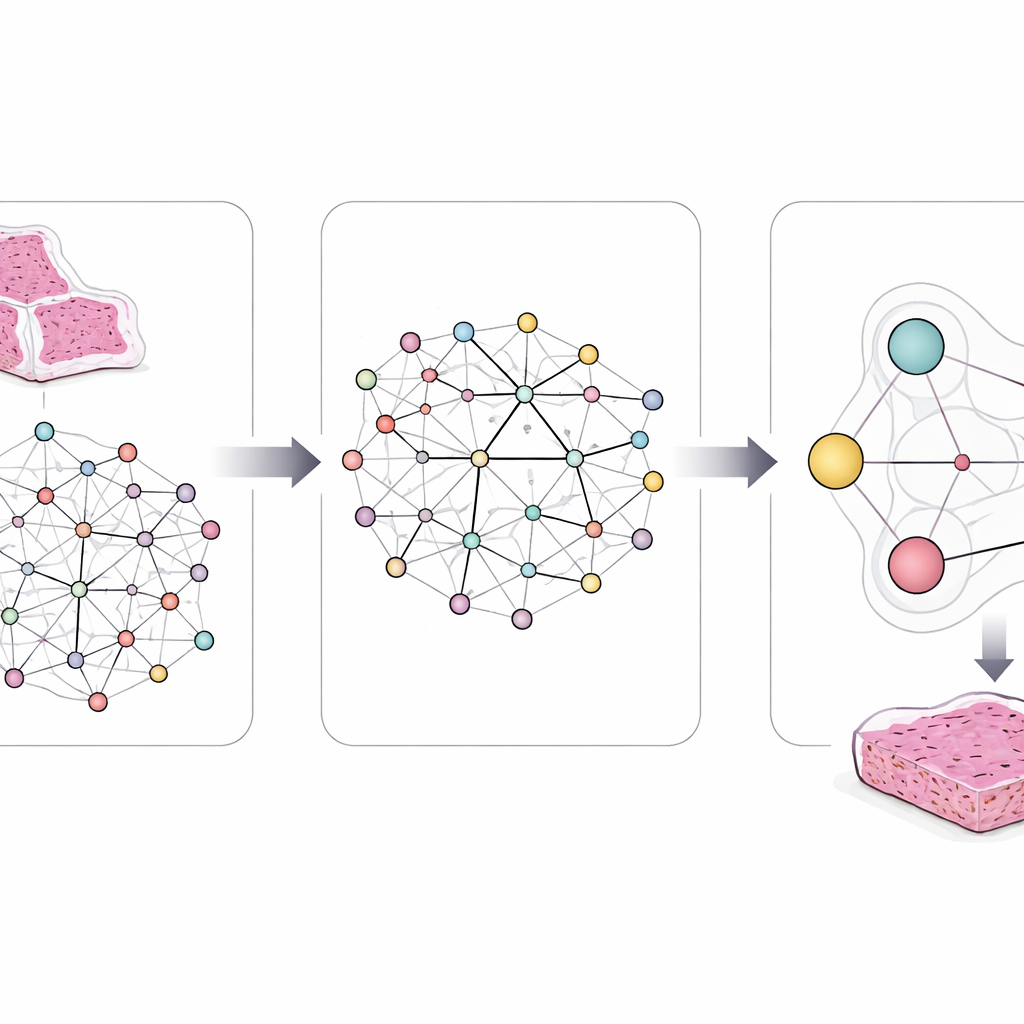
与现有方法的准确性比较
该团队在超过1600张与基因数据相关联的肺癌切片上评估了他们的系统。他们将其与侧重单基因的标准深度学习模型以及处理多基因但忽略通路结构的更高级方法进行了比较。在若干重要通路上——包括涉及细胞生长信号和组织支架的通路——新模型对基因组群变化和通路异常的预测更为准确。它还生成了外观与已知与特定突变相关的临床实例密切匹配的图像补丁,表明模型关注的是有意义的显微学模式,而非无关的图像噪声。
这对患者意味着什么
对非专业人士而言,最重要的结果是这种方法将一张常规病理切片转变为丰富的分子信息来源。医生未来可能无需为每个可能的靶点单独下昂贵的基因检测,而是直接利用此类模型从已有图像中筛查被破坏的通路。尽管该方法仍需更大规模、真实世界的验证且尚不能取代基因组检测,但它指向了这样一个未来:显微镜视野同时成为窥见肿瘤内在连线的窗口——帮助指导更精确、基于生物学的癌症治疗。
引用: Yu, Y., Shi, W., Chen, X. et al. Inferring signaling pathway abnormalities from histopathological images via logic-constrained gene-pathway heterogeneous knowledge graph. npj Biomed. Innov. 3, 23 (2026). https://doi.org/10.1038/s44385-026-00078-6
关键词: 癌症通路, 组织病理学人工智能, 图神经网络, 肺腺癌, 数字病理学