Clear Sky Science · zh
为癌症免疫疗法改造巨噬细胞:新兴见解与治疗潜力
把身体的清道夫变成抗癌战士
我们的身体里遍布巨噬细胞——这些漫游的“清道夫”吞噬病原体和死亡组织。本文综述探讨了科学家如何重新定向这些细胞以对抗癌症。由于巨噬细胞在肿瘤内丰度很高,包括那些对当前主流免疫疗法耐受的肿瘤,理解并工程化它们有望为难治性癌症患者开辟新的治疗选择。
单一细胞类型的多种面貌
巨噬细胞并非一种固定的细胞类型;它们是变形者。它们既可以来自血液,也可以常驻于组织,定植后会响应局部信号。在肿瘤中,这些肿瘤相关巨噬细胞既可能帮助杀死癌细胞,也可能令人困惑地促进肿瘤生长和转移。早期研究者试图将其分为两个类别——“M1”(攻击模式)和“M2”(修复或支持模式)。新的基因和空间绘图工具现在显示出更加丰富的状态谱系,存在多个亚群,其行为因肿瘤类型和具体部位而异。即便曾被认为坚定“促瘤”的细胞,在某些情境下也能动员T细胞并支持抗癌免疫。
感知环境并吞噬癌细胞
巨噬细胞不仅听从化学信号;它们也能感知周围的物理世界。当它们在肿瘤那稠密的蛋白网格中爬行、挤过细胞间隙并承受流体力时,会通过诸如Piezo1之类的专用受体感知刚性和应变。这些机械线索与经典免疫信号共同影响巨噬细胞朝炎性或抑制性角色倾斜。从功能上讲,巨噬细胞可以吞噬癌细胞,随后把它们分解并将片段(抗原)呈递给T细胞,从而连接先天免疫与适应性免疫。癌细胞会通过发送“别吃我”信号进行反击,典型的是表面分子CD47,它与巨噬细胞上的抑制受体结合。阻断该相互作用的药物正在多个临床试验中测试,可增强癌细胞清除,但需要谨慎调控以避免损伤健康细胞。
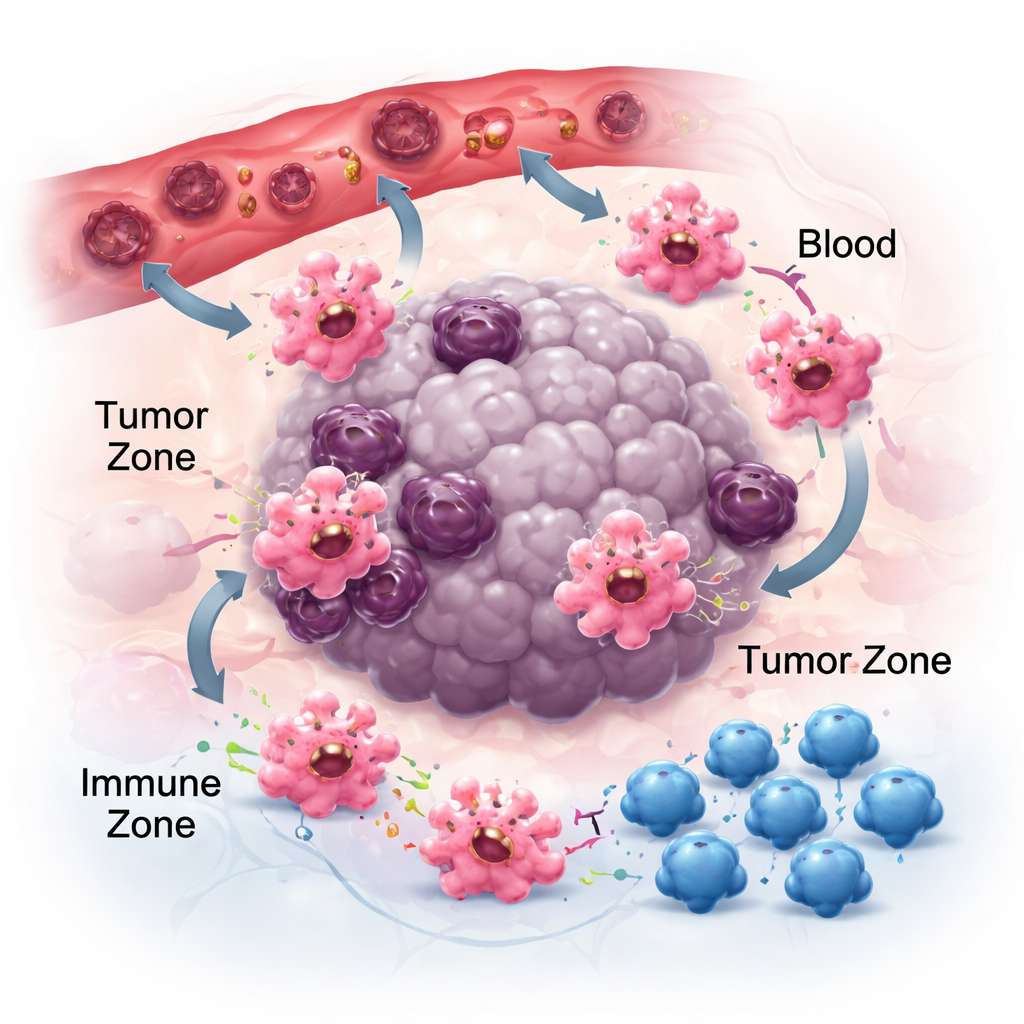
在肿瘤邻里中的移动、黏附与交流
要在癌症中发挥作用,巨噬细胞首先必须到达肿瘤并定位于合适的利基。它们追随由癌细胞和周围细胞释放的化学足迹——趋化因子和生长因子。像CCR2–CCL2这样的配对帮助将它们吸引到肿瘤,阻断这些信号的药物可以减少巨噬细胞的积累,尽管并不能完全阻止,这提示还有诸如CSF-1和VEGF等其他吸引因子。到位后,巨噬细胞与局部基质的黏附方式也会塑造其行为。它们的黏附受体——整合素,不仅仅起粘合作用;它们可以放大炎症信号并推动细胞朝更具抗肿瘤性的状态转变。与此同时,巨噬细胞还会释放被称为细胞外囊泡的小囊,携带RNA和蛋白质到邻近细胞。根据肿瘤类型,这些囊泡要么削弱免疫并促进转移,要么增强抗肿瘤反应,凸显出巨噬细胞通信的情境依赖性。
用基因与材料对巨噬细胞进行重编程
由于巨噬细胞天然比许多T细胞更易浸润实体肿瘤,研究者正将它们重新设计为活体药物。一种遗传策略借鉴了嵌合抗原受体(CAR)T细胞疗法:加入合成受体以创建CAR巨噬细胞(CAR-M)。这些设计细胞能够识别肿瘤标志,提升对癌细胞的吞噬效率,消化周围基质,释放炎性信号,并通过呈递肿瘤抗原激活T细胞。针对HER2的CAR-M早期人体试验显示出令人鼓舞的安全性和生物学活性,尽管仍需更多工作来证明强劲且持久的疗效。与此同时,非基因方法使用由脂质或聚合物制成的颗粒和“背包”。巨噬细胞可以吞入负载药物的纳米颗粒并像特洛伊木马一样将它们携带到肿瘤深处,或佩戴表面附着的贴片,缓慢释放免疫增强信号,帮助它们在不让细胞内部过载的情况下维持抗肿瘤身份。来源于巨噬细胞的囊泡本身也在作为天然、无细胞递送载体进行测试。
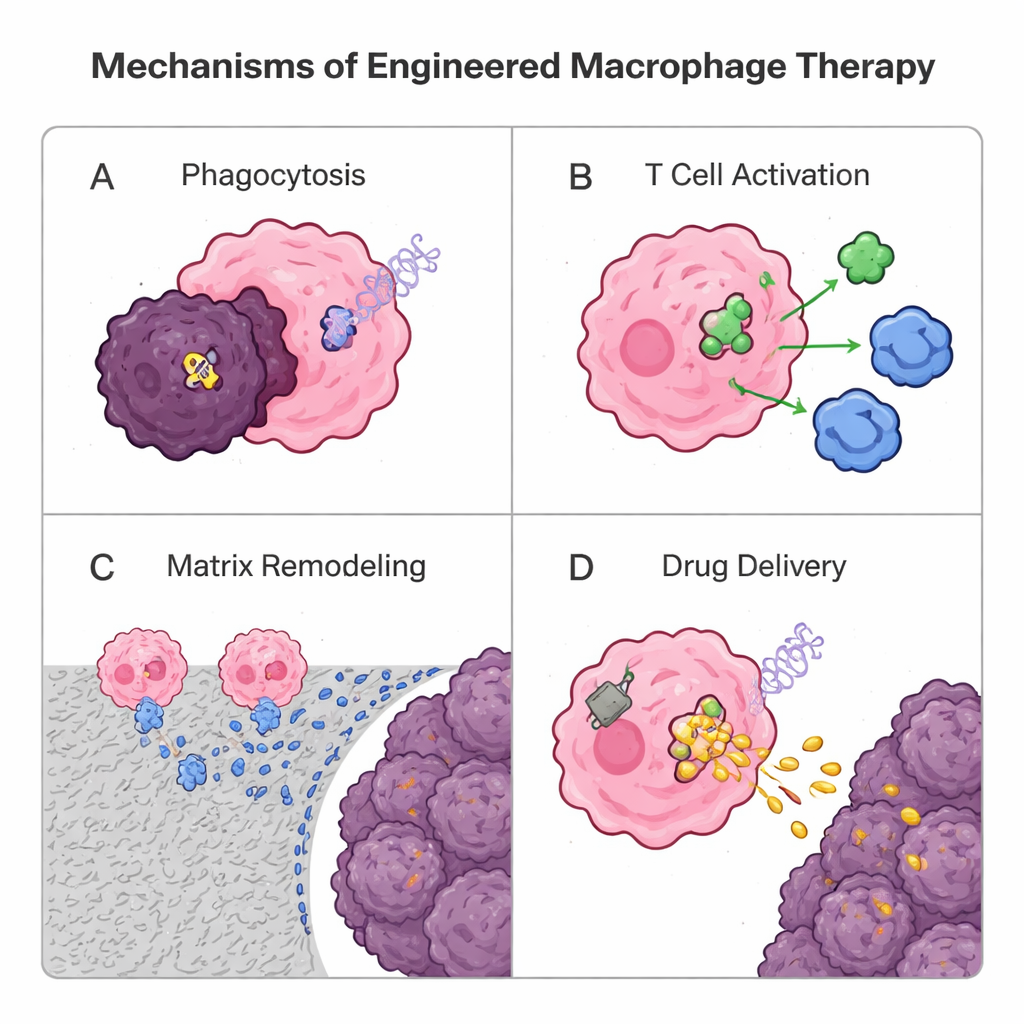
前方的挑战与希望的理由
尽管前景可期,巨噬细胞疗法仍需克服实际障碍。从患者体内产生足够且一致的细胞既耗时又昂贵,而且输注后这些细胞并非能无限存活或增殖。它们内在的可塑性虽在生物学上有用,但在复杂且抑制性的肿瘤微环境中可能难以将其保持在抗肿瘤模式。作者认为,先进的生物工程模型——模拟真实组织力学的三维培养、类器官和器官芯片系统——对于理解和预测工程化巨噬细胞在患者体内的行为将至关重要。即便如此,巨噬细胞天然进入实体肿瘤、吞噬癌细胞并唤醒T细胞的能力,加上早期的安全性记录,表明基于巨噬细胞的疗法可能成为一项重要的新武器,尤其是针对当前对大多数免疫疗法耐受的“冷”肿瘤。
引用: Block, A., Liu, X., Zhang, D. et al. Engineering macrophages for cancer immunotherapy: emerging insights and therapeutic potential. npj Biomed. Innov. 3, 18 (2026). https://doi.org/10.1038/s44385-026-00072-y
关键词: 巨噬细胞免疫疗法, 肿瘤微环境, CAR 巨噬细胞, 吞噬作用, 纳米颗粒药物递送