Clear Sky Science · zh
加速个性化医学:用于预测癌症治疗反应及更多用途的患者来源类器官微型化药物筛选
更快将实验室成果带到病床旁
对于许多晚期癌症患者来说,等待数周才能知道化疗是否有效可能令人痛苦。该研究探索了一种利用患者肿瘤的微型实验室复制品——称为类器官——提前测试药物来加速这一进程的方法。通过将测试流程微型化并实现自动化,研究人员旨在用远少于现有方法所需的组织量和时间预测哪些治疗可能有效。
培养皿中的微型肿瘤
患者来源类器官是从患者自身肿瘤中生长出的三维细胞群。与传统的平面细胞培养不同,这些微型肿瘤保留了原始癌症的大部分遗传多样性和行为特征。早期研究表明,当类器官在体外对某种药物产生反应或未产生反应时,患者在临床上常常表现出类似的反应。问题在于,标准的类器官药物测试每个孔通常使用数百个类器官,这需要大量活检材料并耗时数周,从而限制了其在需要快速开始治疗的患者中的现实应用。
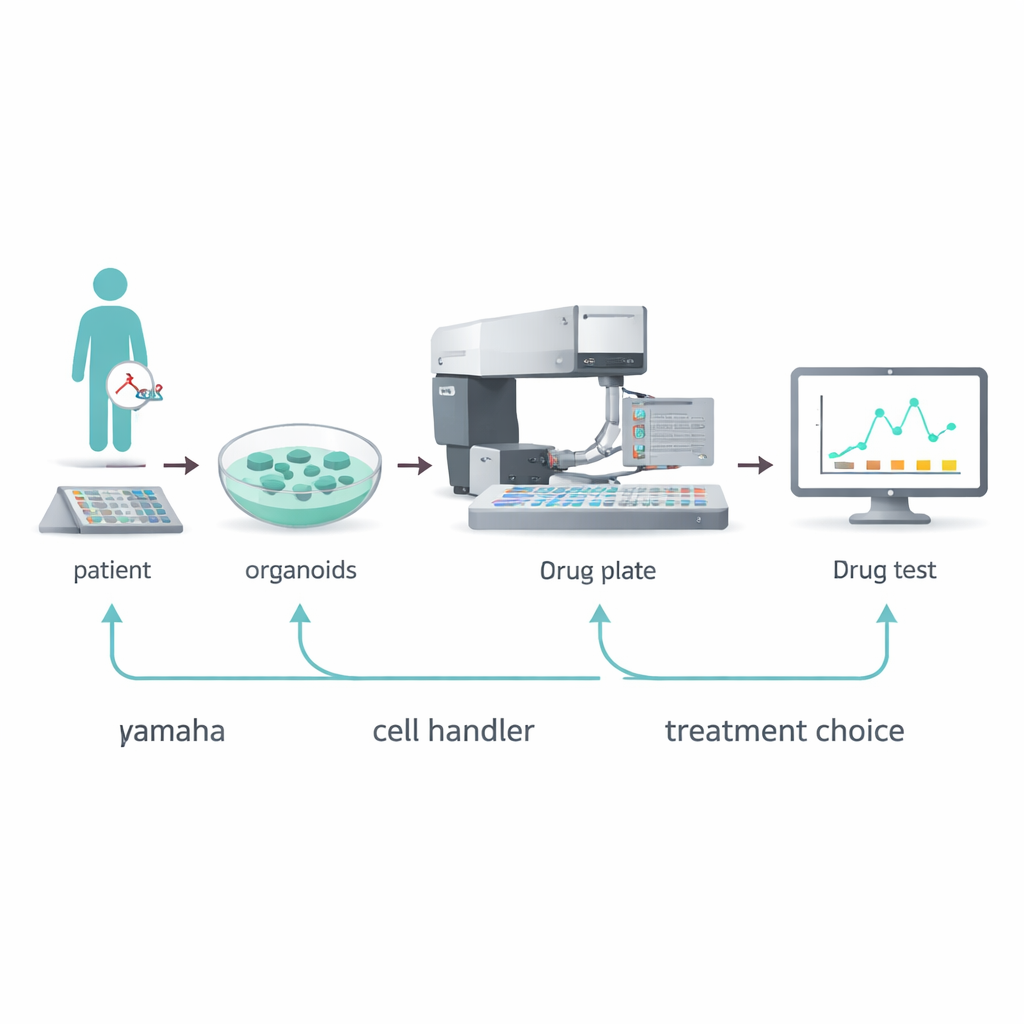
用于微型肿瘤的机器人挑选器
研究团队转向一种自动化设备——雅马哈细胞处理器(Yamaha Cell Handler)来解决这些瓶颈。该机器人使用摄像头在原始板上识别单个类器官,分析它们的大小和形状,然后轻柔地挑取选定的类器官并将其分配到384孔板的微孔中。通过微调接种的类器官数量、类器官在凝胶状基质中的支撑方式以及所用成像染料和读出方法,研究人员确定每孔仅需5到10个类器官即可进行可靠的药物测试。他们还优化了一种基于DNA的荧光测定法,用于报告药物暴露后存活细胞的数量,从而避免了一些旧有能量代谢类测试的陷阱。
用极少细胞做更多事
优化后,微型化系统所用材料仅为传统筛选所需量的0.5%到约5%,将类器官需求减少了约25倍。尽管大幅缩小规模,但每孔10个类器官测得的药物敏感性模式与每孔250个类器官的结果高度一致。该平台甚至能够揭示单个患者肿瘤模型内的隐含差异,例如对常用化疗药物敏感或耐药的类器官亚群。在一个针对性抗体治疗的示例中,携带已知耐药突变的肿瘤来源类器官表现如预期——不响应;而不带该突变的类器官则被强烈抑制,无论是在标准还是微型化格式中测试。
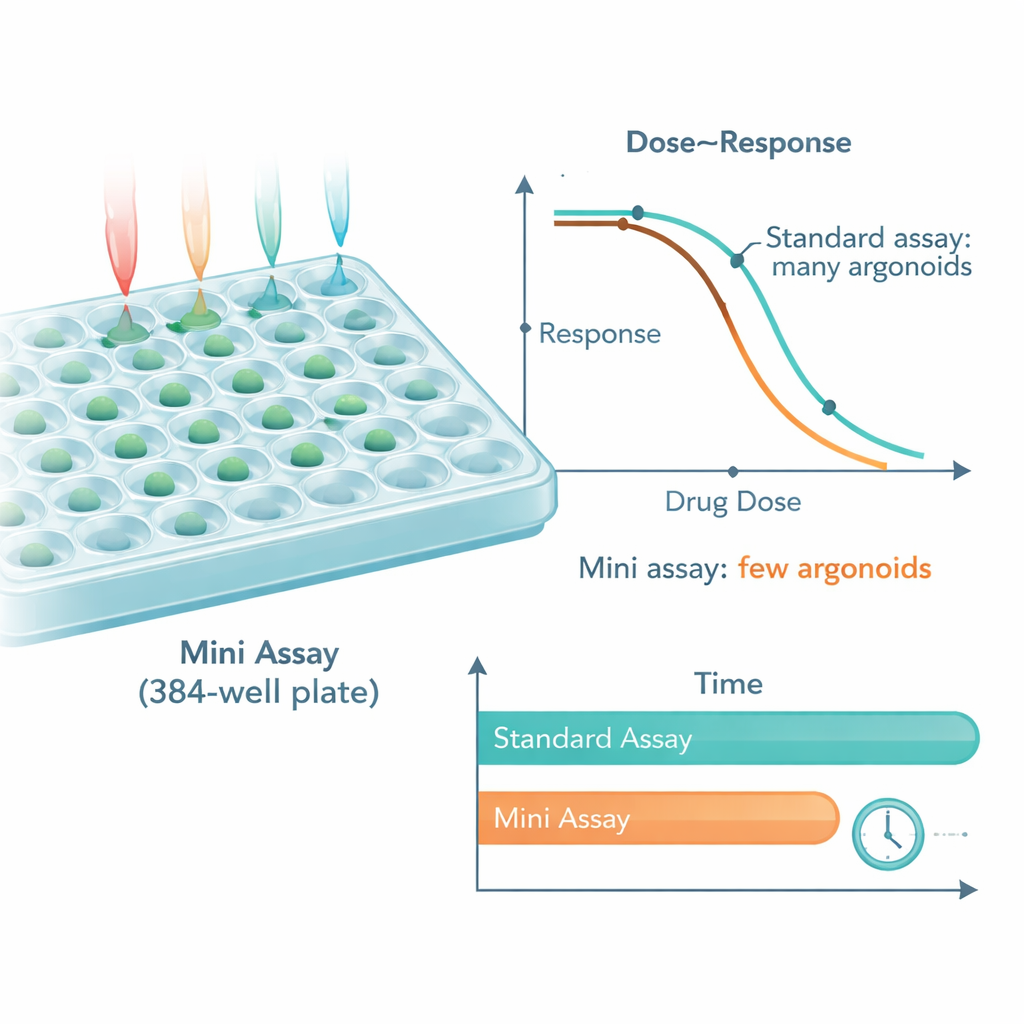
从实验室信号到患者结局
研究人员接着问:这种更精简的测定是否仍能反映真实的患者经历。他们测试了来自接受过临床标准化疗药物的转移性结直肠癌患者的类器官。对于5-氟尿嘧啶和奥沙利铂,微型化测定(每孔仅5–10个类器官且药物浓度更少)中测得的药物反应与更大、传统筛选的结果高度一致。对患者更重要的是,微型测定中类器官的敏感性与患者肿瘤受控时间长短以及在许多情况下的总生存期相关联。减少类器官数量并未削弱这些关联,表明这一精简方法仍具有临床信息价值。
这对患者意味着什么
通过证明可以用远少于以往的类器官数量和更快的流程进行准确的药物反应测试,这项研究将基于类器官的精准医学推向更接近常规临床实践的方向。新的自动化平台将所需细胞数量和周转时间大致减半,使得从活检中培养类器官、测试多种疗法并在指导治疗决策前及时返回结果成为更现实的选择。尽管还需在更多癌种中进一步验证,这种微型化的类器官筛选策略为基于个体肿瘤在体外表现而非单纯依赖群体平均值来选择癌症药物提供了一条务实的路径。
引用: Abouleila, Y., Smabers, L.P., Voskuilen, T. et al. Accelerating personalized medicine: miniaturized patient-derived organoid drug screening for predicting cancer treatment responses and beyond. npj Biomed. Innov. 3, 16 (2026). https://doi.org/10.1038/s44385-026-00067-9
关键词: 癌症类器官, 个性化医学, 药物筛选, 结直肠癌, 肿瘤学自动化