Clear Sky Science · zh
表面改性的静电纺丝支架支持iPSC来源角膜缘干细胞功能
为视力争取第二次机会
当眼睛前方的透明窗——角膜——受损时,人们可能永久失去视力。一个主要原因是位于角膜边缘的特殊细胞——角膜缘干细胞的缺失,这些细胞通常保持表面清晰光滑。本文描述了一种新的实验室制“活性敷料”,未来可用于携带替代干细胞到眼部,相较于现有方法能够更安全、更可靠地帮助恢复视力。
为何角膜缘至关重要
角膜由数层组织构成,必须保持光滑透明以正确折射光线。位于透明角膜与眼白交界处的一小圈干细胞不断更新最外层。损伤、感染或自身免疫疾病可摧毁这些角膜缘干细胞,引发称为角膜缘干细胞缺失的病症。没有它们,血管会入侵原本清澈的角膜,表面变得瘢痕化和不规则,患者可能遭受严重视力下降或失明。医生可以移植健康的干细胞,但仍需要一种安全、结实且透明的载体,将这些脆弱细胞递送到受损的眼部。
构建合成“活性敷料”
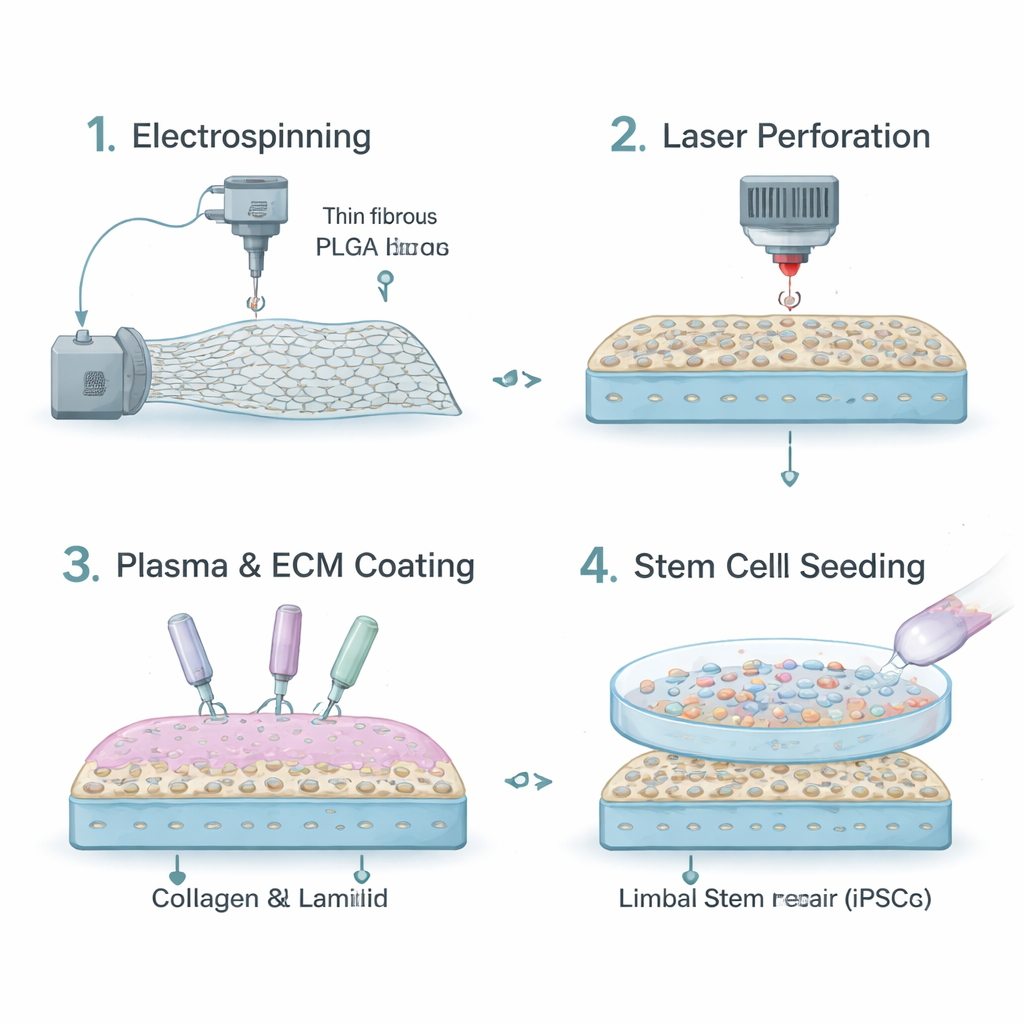
目前许多外科医生依赖羊膜或胶原片等天然组织作为载体。虽然这些材料具有生物相容性,但不同供体间差异较大、可能供不应求,并且无法精确控制它们的降解时间或机械刚度。研究者转而使用一种可生物降解的塑料PLGA,这种材料已被用于某些医疗器械。采用静电纺丝技术,他们将PLGA拉制成类似角膜自身支撑层的微纤维薄膜。这种纤维片在手术中足够坚固,并且可以调节为在眼睛愈合过程中缓慢溶解。
使支架对细胞友好且透明
然而,纯PLGA排斥水分且不天然吸引细胞。为使其表面更具亲和性,团队用大气等离子体处理纤维,添加了可结合蛋白质的化学基团。随后他们在支架上涂覆了IV型胶原和层粘连蛋白‑521,这两种是角膜周围干细胞“巢穴”的关键成分。为改善透明度,他们用精确激光在膜上打出微观孔洞。这些微穿孔将支架透光率从约44%提升到约60%,在保持足够纤维用于细胞附着的同时,使其更接近真实角膜的清晰度。
在新表面上测试干细胞
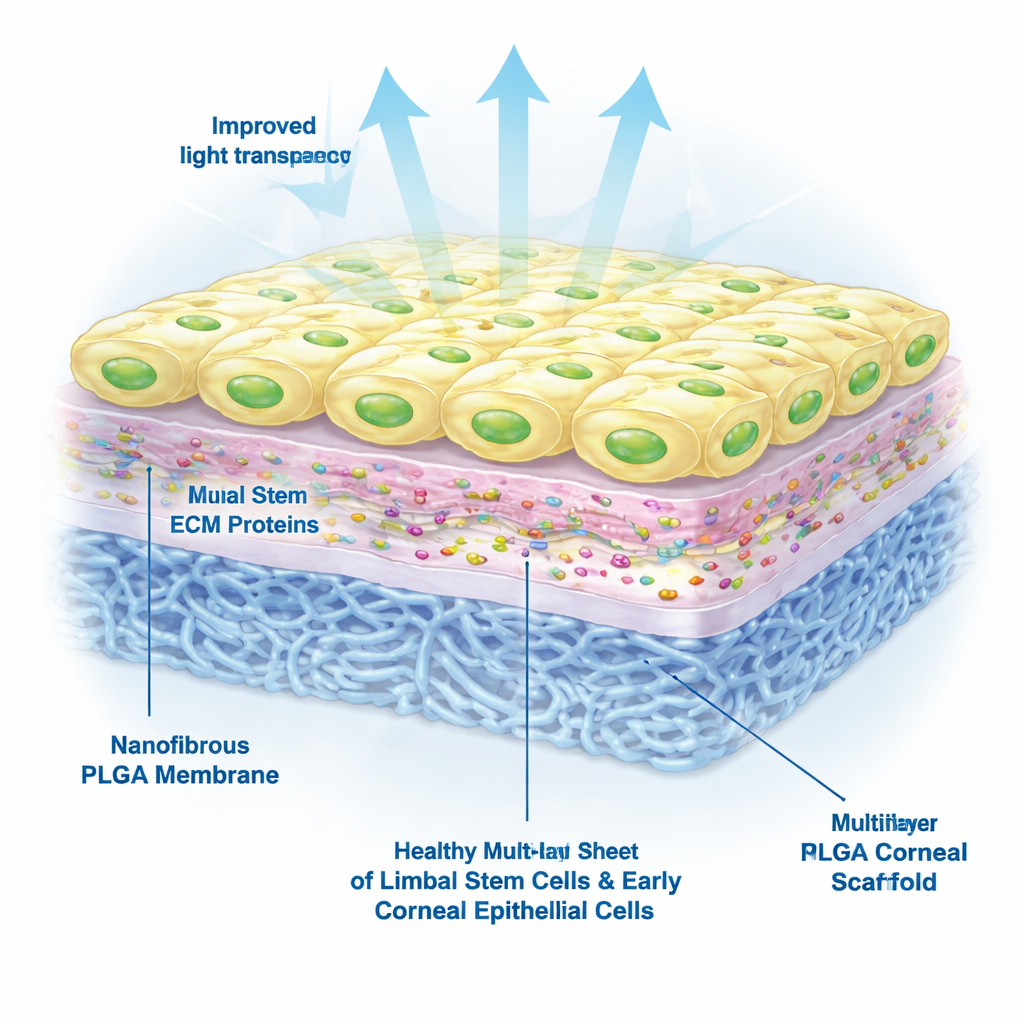
接着团队测试了从诱导多能干细胞(即将成年细胞重编程回灵活的干细胞样状态)分化得到的角膜缘干细胞在该支架上的生长情况。他们比较了不同的表面处理,发现层粘连蛋白‑521是必需的:经等离子体处理并涂覆层粘连蛋白‑521的支架(无论是否同时有IV型胶原)都支持了健康的细胞附着、生存和至少一周的生长。相比之下,放在未处理PLGA或仅涂覆IV型胶原的PLGA上的细胞常常死亡或脱落。在显微镜下,优化后的支架上的细胞形成了紧密的“鹅卵石”状层,类似正常的角膜表面。
保持干细胞处于准备修复的状态
除了存活外,移植的细胞必须保持一种既能自我更新又能分化形成新的角膜表面细胞的状态。研究者通过蛋白染色和基因检测来检验支架上细胞的身份。他们发现与角膜缘干细胞和早期角膜细胞相关的标记物信号强烈,而成熟细胞的标记物信号则较弱。这一模式表明存在一组活跃的干细胞和处于早期分化阶段的后代细胞,已处于重建角膜表面的准备状态,而非一群疲惫或功能丧失的细胞。
对患者可能意味着什么
总体而言,该研究表明经过精心设计的全合成支架可以模拟眼睛自然干细胞环境的许多特征。通过结合可调节的纤维材料、用于改善视力的微穿孔以及专门支持角膜缘干细胞的蛋白涂层,作者创造了一个有前景的未来干细胞移植载体。尽管这项工作仍处于实验室阶段,动物和临床试验尚未进行,但该方法最终可能提供一种更一致、可扩展且个性化的方式,恢复清晰健康的角膜表面,帮助原本难治的视力丧失患者重见光明。
引用: Mahmood, N., Zha, D., Gullion, S. et al. Surface modified electrospun scaffold supports iPSC-derived limbal stem cell function. npj Biomed. Innov. 3, 14 (2026). https://doi.org/10.1038/s44385-026-00066-w
关键词: 角膜再生, 角膜缘干细胞, 静电纺丝支架, 生物材料, 诱导多能干细胞