Clear Sky Science · zh
优化诱导早产婴儿来源肠上皮类器官内炎症的方法
为何这对脆弱新生儿很重要
极早出生的婴儿面临一种危险组合:未成熟的肠道与快速变化的微生物群。二者可能引发失控的炎症,损害肠道并导致危及生命的疾病,如坏死性小肠结肠炎。由于不能直接在早产婴儿身上进行实验,科学家需要逼真的体外肠道模型来测试是什么驱动炎症以及如何阻止它。本研究改进了这样一种模型,使用实验室培养的微小肠道组织,提供更清晰的方法来探查哪些微生物信号会将正常防御转变为有害的炎症。
在培养皿中“长出”早产肠道
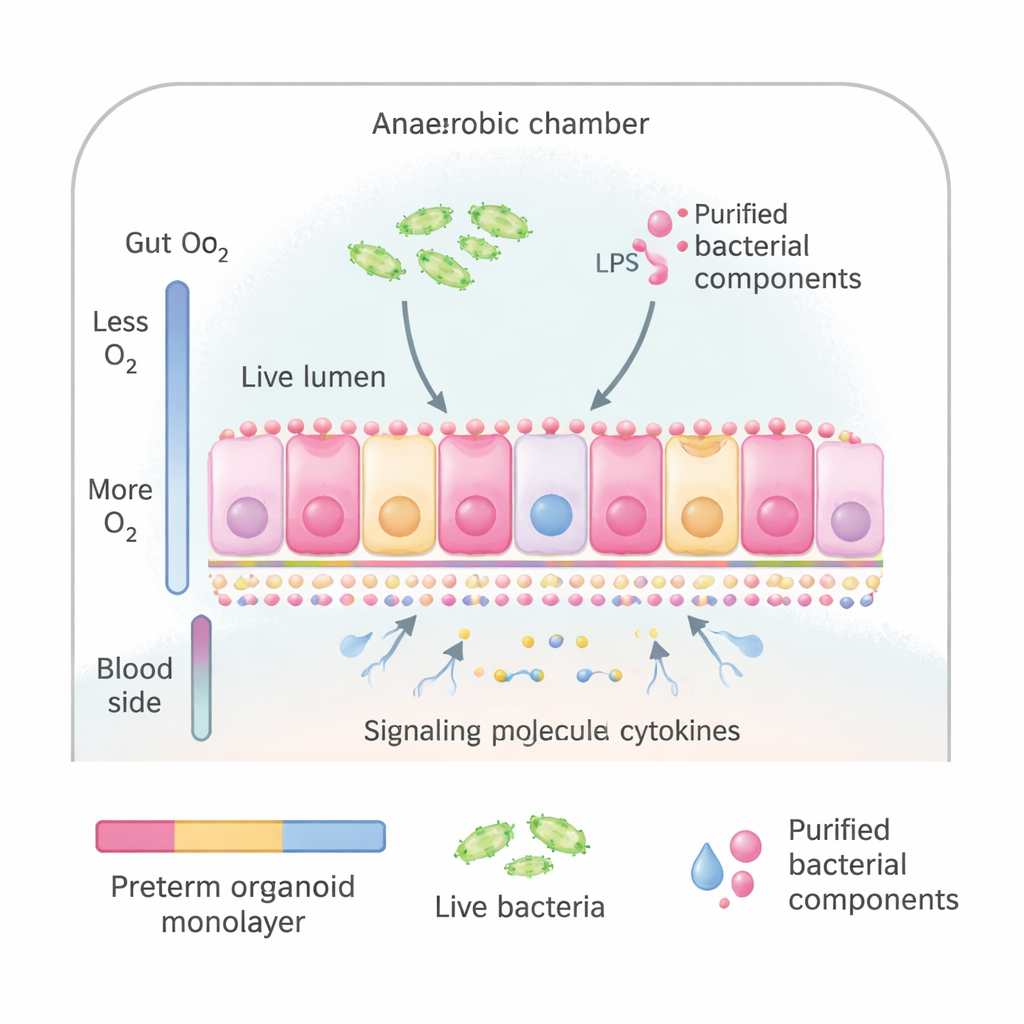
研究者使用肠类器官——由早产婴儿在手术期间取得的干细胞培养出的微型肠道上皮。这些类器官可被铺平成一层薄薄的细胞片,外观和功能都很像小肠的内表面,并保持正确的极性(上侧朝向肠腔内容物,下侧朝向血液)。团队将这些细胞片置于一种模拟肠道天然氧气梯度的特殊培养系统中:面向微生物的一侧氧含量低,而面向血液的一侧氧含量较高。这样他们就能将“肠道”表面暴露于来自早产婴儿的整菌群,或暴露于已知能激活免疫系统的纯化细菌组分。
测试哪种方式最能触发炎性警报
科学家比较了几种诱发炎症的方法:一种来源于患病早产婴儿的常见活菌混合物;用高温杀死的相同细菌;以及两种纯化的细菌信号——来自细菌细胞壁的脂多糖(LPS)和来自鞭毛的鞭毛蛋白(flagellin)。他们测量了IL‑8的释放(IL‑8是一种招募免疫细胞并作为炎症一般标志的信号蛋白),并用大规模蛋白质分析来观察肠上皮细胞内部机制的变化。令人意外的是,在该体系中活菌或死菌即便在24小时后也未显著增加IL‑8。相反,鞭毛蛋白,尤其是鞭毛蛋白与LPS的组合,在仅三小时内就明显提高了IL‑8,表明这些纯化信号能够可靠地开启炎性状态。
寻找最真实且高效的实验方案
为了更贴近真实肠道生物学,团队接着关注每种信号自然起作用的位置。LPS通常在面向肠腔的一侧被感知,而鞭毛蛋白主要在组织(基底)一侧被检测到。研究者使用比早期实验低得多、更符合生理的剂量,将LPS施加到上侧(腔面)而将鞭毛蛋白施加到下侧(血面)的类器官细胞片。这个简单的改变在三小时内产生了强烈且广泛的反应:包括IL‑8、TNF和多种趋化因子在内的多种炎性信使从组织两侧被分泌出来。与此同时,数百种细胞蛋白质丰度发生变化,显示防御通路的大规模激活。
同一模型中的炎症、制动与修复
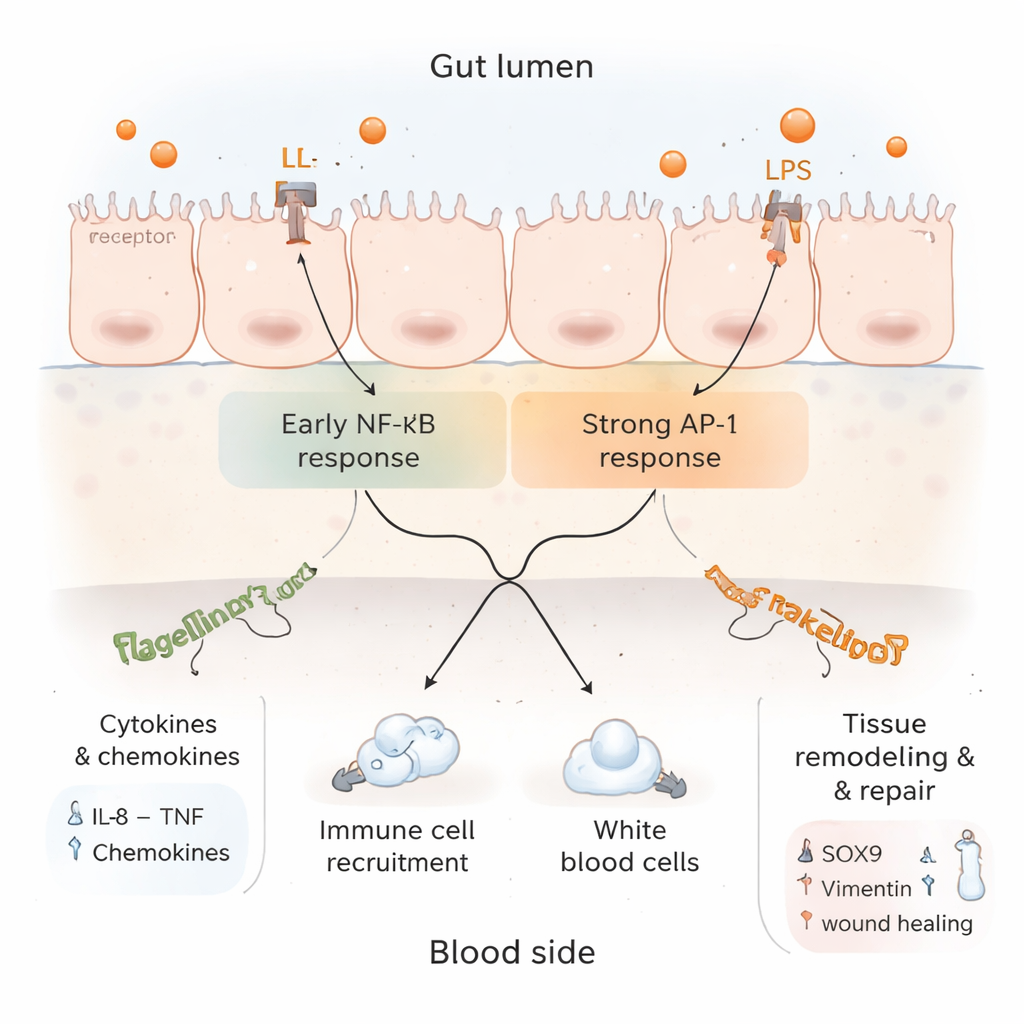
深入分析蛋白质数据后,研究者发现了复杂的图景。一方面,活跃的炎症标志和免疫细胞募集标记上升,与TNF和IL‑17相关的信号通路——这两者在肠道免疫防御中都很重要——被激活。另一方面,驱动许多炎症基因的经典NF‑κB通路的若干组成部分被下调,而涉及AP‑1的替代通路仍然保持活跃。这表明在初始警报之后,组织开始施加制动以防止失控损伤。与此同时,与组织再生、结构重塑和可控性细胞死亡相关的蛋白增加,暗示肠上皮不仅处于炎症状态,还在尝试重塑和自我修复。
这对未来治疗意味着什么
通过系统地比较不同的微生物刺激、剂量、作用位置和暴露时间,作者得出结论:在肠道面低剂量LPS与血面鞭毛蛋白一起作用三小时,是在早产来源肠类器官中诱导炎症最稳健且可重复的方法。这个改进的模型不仅重现了炎症的爆发,还包含了内在的制动、耐受机制和修复反应,契合了脆弱早产肠道的特性。它为其他实验室提供了实用的蓝图,用以研究特定微生物、药物或营养因素如何加剧或缓解极早产婴儿的肠道炎症——这是朝着更安全、有针对性的预防策略迈出的关键一步,以防止这一脆弱人群发生毁灭性的肠道疾病。
引用: Chapman, J.A., Frey, A.M., Dueñas, M.E. et al. Optimising the induction of inflammation within preterm infant-derived intestinal epithelial organoids. npj Gut Liver 3, 5 (2026). https://doi.org/10.1038/s44355-026-00054-2
关键词: 早产婴儿肠道, 肠道类器官, 肠道炎症, 微生物组, 坏死性小肠结肠炎