Clear Sky Science · zh
26S蛋白酶体中ATP驱动蛋白展开的非平衡化学机械能传递
一个微小机器如何维持蛋白质秩序
在每个细胞内部,有一个被称为26S蛋白酶体的微观粉碎机,不断清除受损或不再需要的蛋白质,维持细胞健康。这个机器的核心是一圈环形马达,它消耗化学燃料(ATP)来抓取、展开并将蛋白质拉入中央腔室进行切割。本文利用先进的计算机模拟揭示了该马达如何将化学能转化为机械运动,提供了一个详细且定量的图景,说明了支撑衰老、神经疾病、免疫以及癌症等过程的机制。
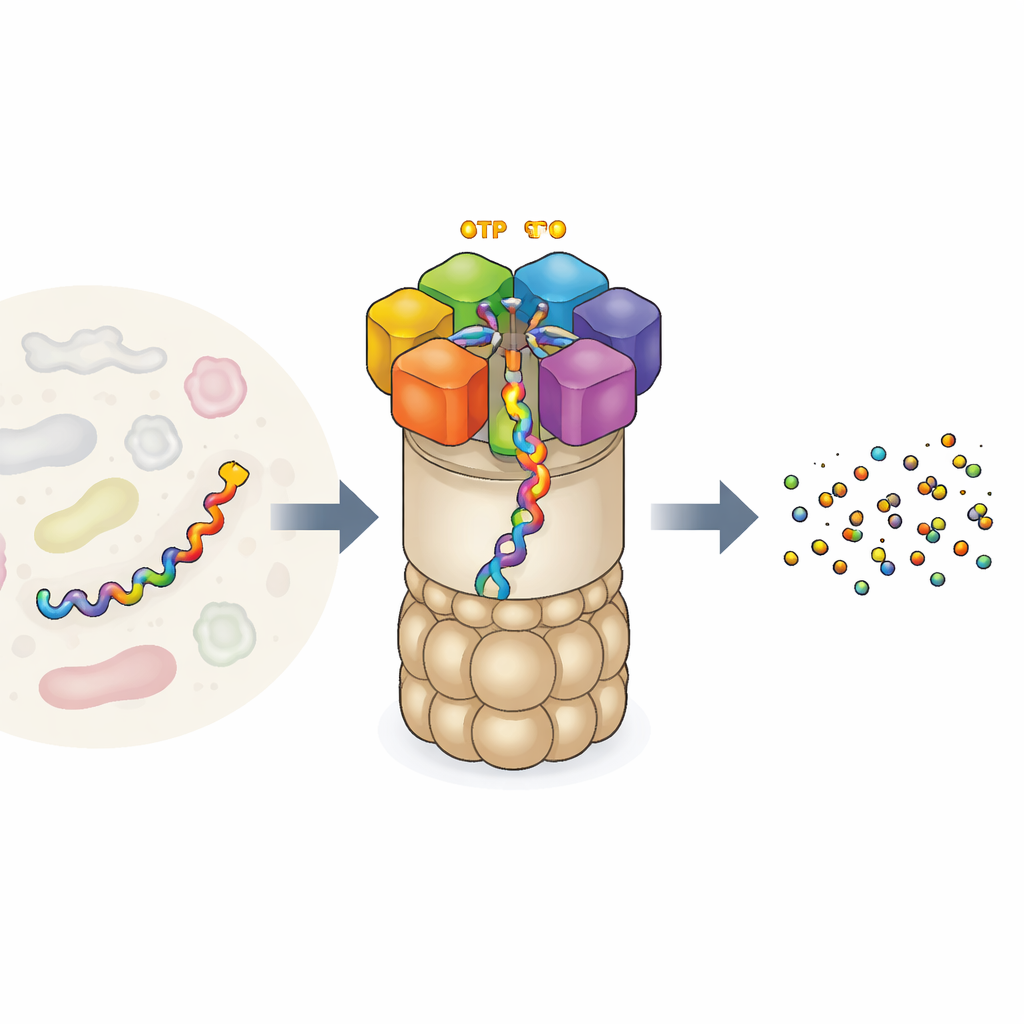
细胞的蛋白质回收工厂
26S蛋白酶体是细胞中最大、最复杂的蛋白质机器之一。它由一个类似桶状的核心负责切割蛋白质,以及一个识别应被降解蛋白的调控帽组成。在入口处是一圈由六个不同马达亚基构成的环。每个亚基都能结合ATP——细胞的通用能量货币——并利用这能量抓住蛋白链并将其拉入核心以便降解。这个马达并非随机工作:早期实验提示六个亚基以协调的“手递手”方式运作,像登山者在绳索上传递一样推进蛋白。但实验只能捕捉到这一动作的少数快照,因此关于完整的运动序列以及燃料消耗如何精确地与机械功连接仍有疑问。
模拟分子拔河
作者建立了一个概率性计算模型,将马达视为在多种可能构象之间跳跃的系统,同时ATP及其产物在结合与解离。模型定义了环的30种主要构象,其中一、二或三个马达亚基失去对蛋白的抓握,以及一种特殊的紧闭态,其中六个亚基都保持抓握。使用模拟随机化学事件的标准算法,他们追踪了数十万步在这些步中发生的ATP结合、ATP水解和马达构象变化。通过这些运行,他们能够预测在不同条件下(如ATP、其耗竭产物ADP以及实验中常用的不可水解ATP类似物浓度变化)蛋白被拉过的速率。
燃料过多反而使马达变慢
模拟再现了若干令人困惑的实验发现。当ATP从低浓度上升时,马达拉动蛋白的速度加快,因为结合燃料是最慢的步骤。但在约1毫摩尔ATP以上,速度达到峰值后反而下降:环更长时间停留在一种堵塞的、不转位的构象中,尽管六个亚基都结合了ATP,但蛋白并未移动。加入ADP或不可水解的ATP类似物会持续减慢马达速度,因为这些分子与ATP竞争结合位点却无法完成完整的动力行程。模型还预测了马达遇到非常紧密折叠的蛋白区段(作为路障)时的行为:在这些情况下,马达会花更多时间与阻力抗争,整体降解速率下降,这与使用人工稳定化蛋白结构域的测量结果一致。
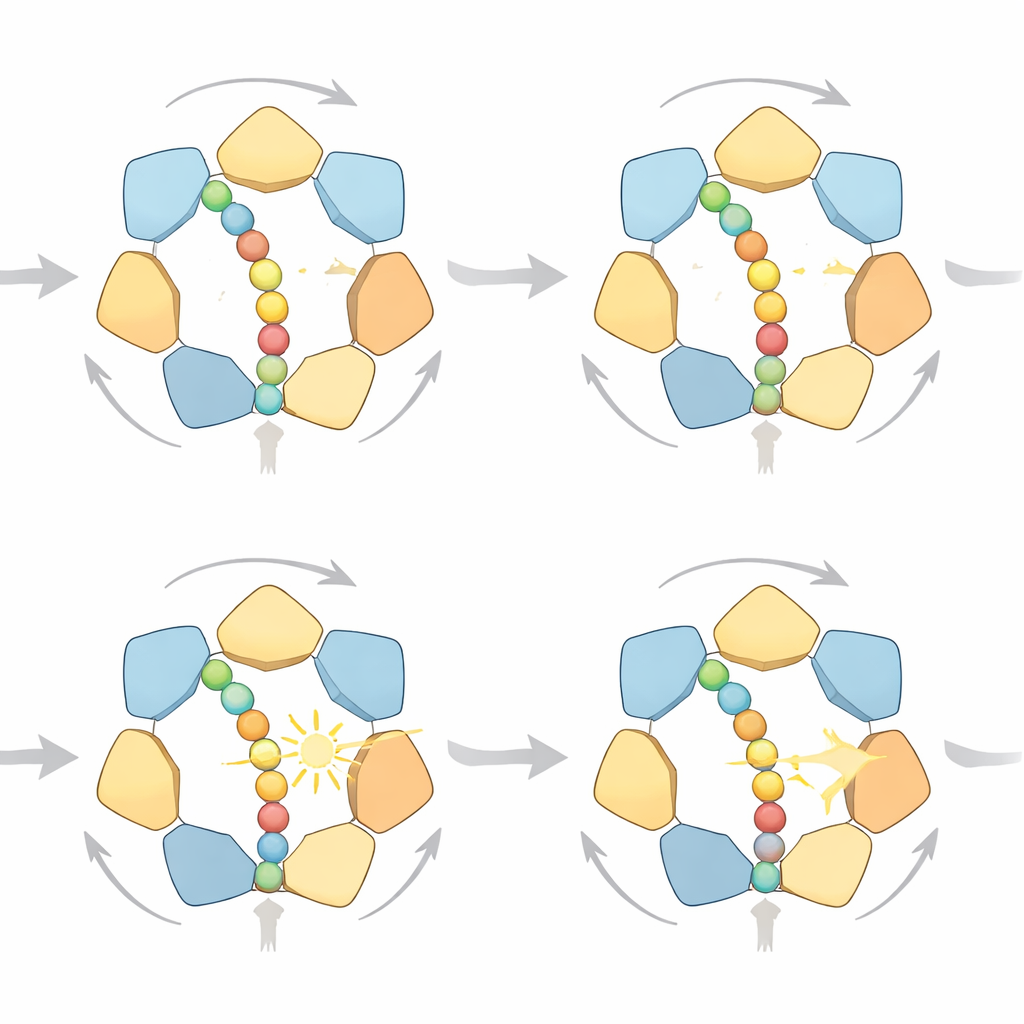
多种方式迈步
通过详细检查模拟轨迹,研究者发现环并不遵循单一刚性的循环。相反,存在多条高概率路径,但都遵守相同的定向“手递手”规则:位于环出口附近的亚基在ATP水解后释放蛋白,移动到亚基螺旋阶梯的顶部,并在更上方重新抓住蛋链。有时蛋白前进一个小步,有时前进两个步,取决于有多少亚基同时放手。在燃料充足时,一步动作占主导,因为它们在对抗外力时消耗的额外功更少;当燃料稀缺时,模型预测更常出现两步跳跃。模拟还将机械负载与马达的化学状态联系起来:随着阻力增加、蛋白停滞,ADP倾向于在更多的六个结合位点中积累——这正是高分辨率结构研究观测到的现象。
能量使用与共同的设计规则
该模型使作者能够描绘出马达在ATP水解时能量如何上升,以及当这能量被转化为运动时如何下降。他们计算出一条效率曲线,表明马达在中等对抗力下工作最佳:阻力太小会浪费性地消耗ATP;阻力太大则几近停滞。团队将他们的预测与来自细菌与酵母中相关蛋白降解机器的数据进行比较,发现不可水解ATP类似物减慢这些马达的趋势非常相似。这表明同一家族的许多环形酶很可能共享一种保守的、拉拽蛋白的机制。
这对健康与疾病的意义
通过将零散的结构快照与生化测量整合为一个可检验的统一框架,这项工作以定量方式展示了一个微小分子马达如何将化学燃料转化为力来回收细胞内的蛋白。该模型不仅解释了大量现有实验,还对燃料水平、机械负载或马达突变如何改变蛋白降解给出预测。因为类似的机器在各种生命形式中普遍存在,且在从神经退行性疾病到癌症等多种病症中处于核心地位,深入理解它们的内部工作原理最终可能有助于设计能够调节、增强或选择性阻断这些微观粉碎机的药物。
引用: Wu, D., Ouyang, Q., Wang, H. et al. Nonequilibrium chemomechanical transduction of ATP-driven protein unfolding in the 26S proteasome. npj Biol. Phys. Mech. 3, 4 (2026). https://doi.org/10.1038/s44341-026-00034-w
关键词: 蛋白酶体, AAA+ ATP酶马达, 蛋白质降解, 分子机器, 化学机械耦合