Clear Sky Science · zh
用于区分路易体病和阿尔茨海默病的微流体纳米磁性分离神经元及星形胶质细胞来源外泌体
这对家庭和医生为何重要
“痴呆”是一个总括性术语,涵盖几种临床症状相似但病因截然不同的脑部疾病。其中两种最常见的阿尔茨海默病和路易体病在临床表现上可几乎难以区分,但对药物的反应和伴随的风险却不同。如今,要在生前确定某人到底患的是哪种病,通常只能通过死后脑组织检查来判断。该研究描述了一种新型血液检测方法,通过读取脑细胞释放的微小信息,目标是在患者仍然健在时区分这两类痴呆。
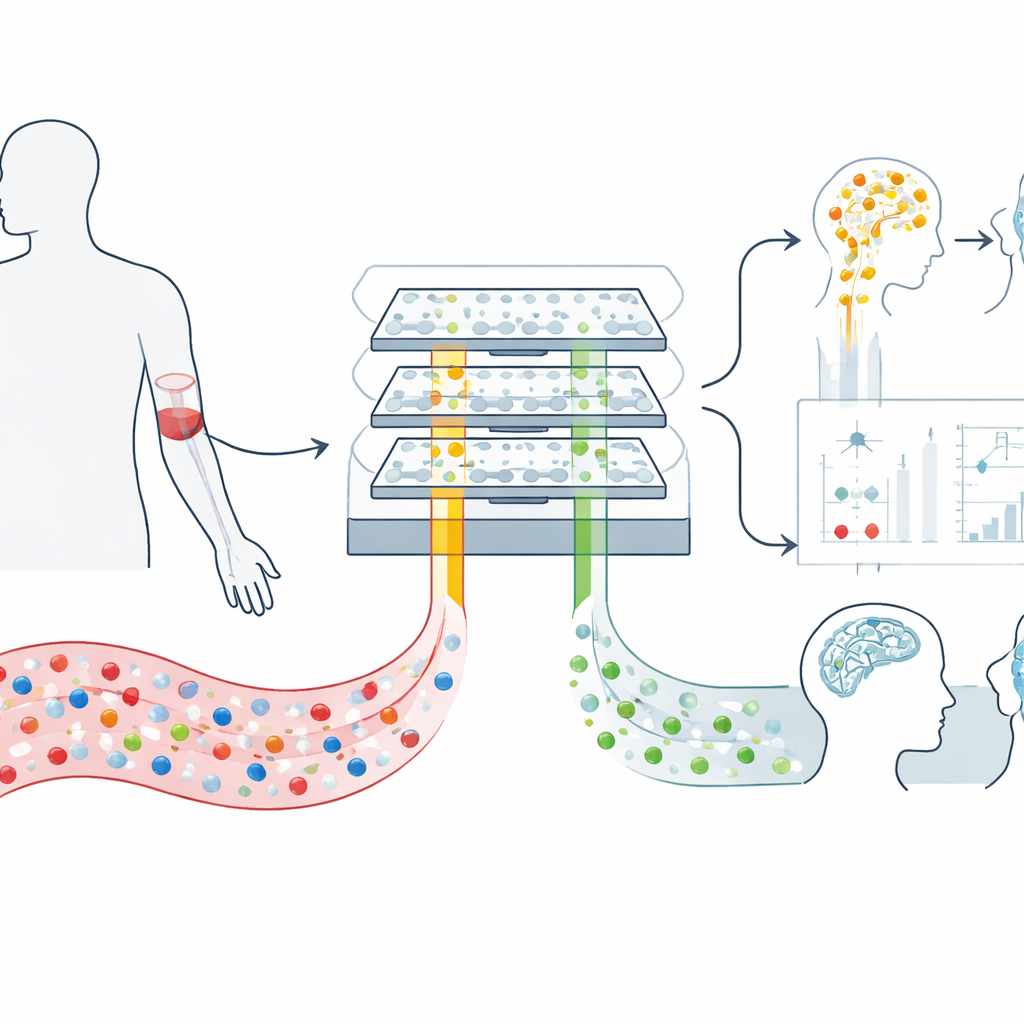
从大脑流向血液的微小包裹
我们的脑不断向血液中释放被称为细胞外囊泡的微小囊泡。这些囊泡像是神经元及其支持细胞寄出的衬垫信封,携带反映脑内状态的遗传物质和蛋白片段。因为它们能穿越血脑屏障并在血液中存活,所以为研究脑生物学提供了一个罕见且侵入性低的窗口。难点在于,每毫升血液中包含来自全身数千亿个囊泡,来源于脑的囊泡数量相对极少,且用常规实验方法难以有效分离。
用于分拣脑信号的磁性芯片
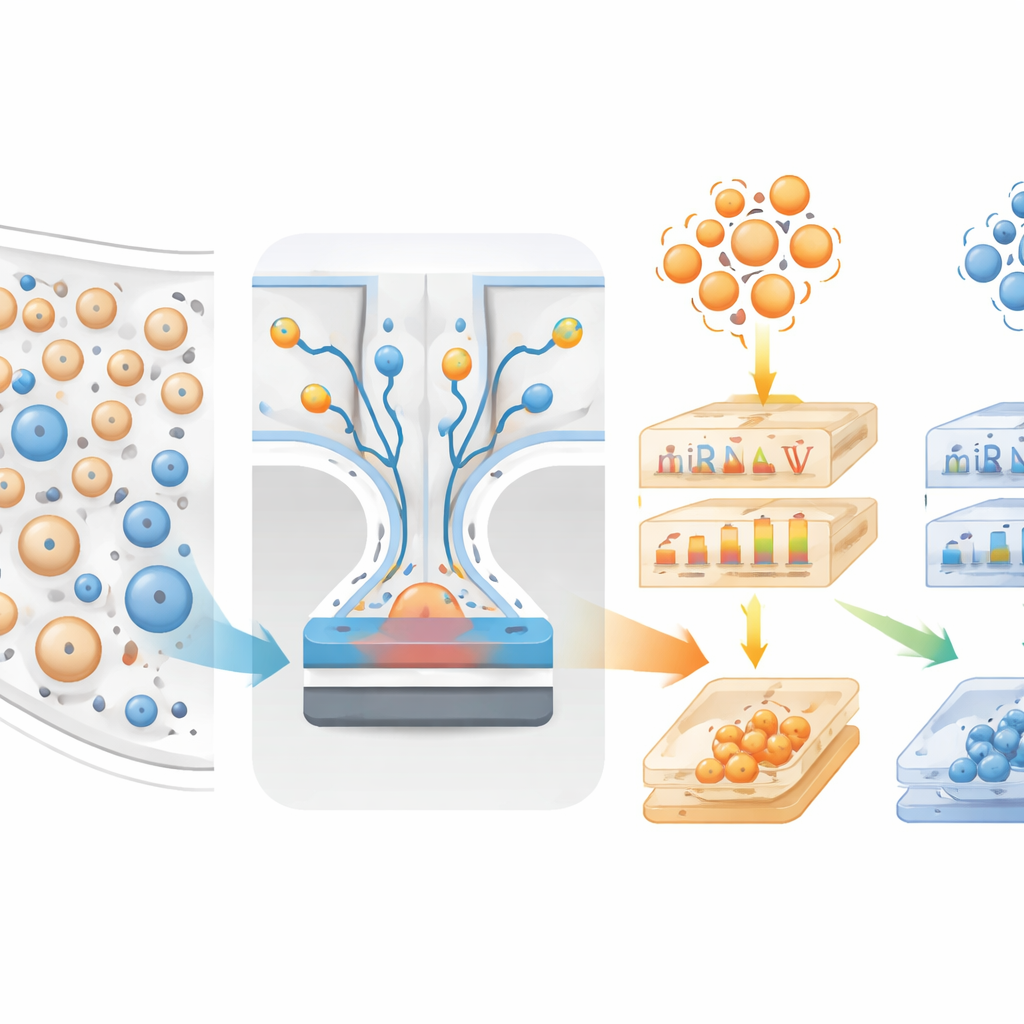
为应对这一挑战,研究者构建了一种称为 mTENPO 的微流体装置,将一块信用卡大小的芯片与强磁场结合。在血样进入芯片之前,研究人员用针对通常出现在神经元囊泡表面蛋白(GluR2)或星形胶质细胞囊泡(GLAST)的抗体,将磁性纳米颗粒标记到囊泡上。当带标记的混合物流经芯片中成百万计的微小孔时,磁场会将高强度标记的脑来源囊泡拉向孔壁并滞留,而其余囊泡随液流被冲洗过去。通过这种方式,团队能够直接从少量血浆样本中独立富集两类囊泡——主要来自神经元的和主要来自星形胶质细胞的。
读取分子指纹
研究团队从137名死后确诊的志愿者样本中分离出这两类囊泡,并测量了经典的阿尔茨海默相关血液蛋白,如不同形式的β-淀粉样蛋白和tau。他们还对囊泡内的短调控RNA(miRNA)进行了测序,比较纯路易体病、纯阿尔茨海默病、混合病理以及无痴呆者之间的差异。若干来自神经元和星形胶质细胞来源囊泡的miRNA,以及血浆中几种与tau相关的蛋白,在线路上在路易体组与阿尔茨海默组之间表现出不同的模式。当研究者映射这些miRNA所靶向的基因时,发现其与细胞存活、炎症和蛋白质处理等通路存在强关联——这些过程已被认为参与了神经退行性变。
构建一个强大的综合血液检测
由于没有单一标志物能清晰区分两种疾病,团队使用机器学习方法从三个来源(神经元囊泡、星形胶质细胞囊泡和血液蛋白)中整合出一组信息量最大的信号。最终的15特征面板包括14种特异性囊泡miRNA和两种磷酸化tau蛋白。经过重复交叉验证以减少过拟合,这一多标志物面板在区分路易体病与阿尔茨海默病时达到约95%的准确率,曲线下面积为0.96——显著优于任何单一指标。脑内具有混合病理的个体通常表现出介于两者之间的标志物水平,表明此类面板未来可能有助于识别混合性疾病,而不是将病情强行归为二选一。
从概念验证到未来临床使用
这项研究是一个早期但重要的证明,显示血液中的脑细胞来源囊泡可以携带足够的详细信息来区分主要的痴呆类型。该工作仍需在更大规模、更具多样性的人群以及随访患者中得到验证,作者也强调目前在为每个囊泡精确确定发源细胞方面仍有局限。尽管如此,可扩展的磁性芯片与经过精心挑选的多标志物面板相结合,为未来可能用于指导治疗选择、改进临床试验并为家庭提供关于亲人痴呆具体病因更清晰答案的血液检测铺就了路线图。
引用: Yang, S.J., Lin, A.A., Shen, H. et al. Microfluidic nanomagnetically isolated neuron- and astrocyte-derived extracellular vesicles to differentiate Lewy body and Alzheimer’s disease. npj Biosensing 3, 19 (2026). https://doi.org/10.1038/s44328-026-00086-x
关键词: 细胞外囊泡, 路易体病, 阿尔茨海默病, 基于血液的生物标志物, 微流体诊断