Clear Sky Science · zh
基于微型器官的微流体生物传感器用于体内持续监测葡萄糖水平
这对糖尿病患者意味着什么
对于 1 型糖尿病患者来说,现有的“人工胰腺”系统仍需不断关注——报告用餐、处理警报,并在夜间担心低血糖。该研究探讨了一种根本不同的葡萄糖传感器,它不依赖单一酶或计算机方程,而是借用体内自身血糖调节机制的一小块活组织:称为胰岛的胰腺细胞簇。通过让这些小型器官执行进化已优化的任务,研究人员旨在构建更智能、更安全的葡萄糖监测器,未来可能在后台更独立地运行。
作为活体传感器的微型器官
目前大多数生物传感器使用纯化分子或单一细胞系来检测化学物质。它们对某一特定物质作出反应,然后将原始信号交给软件去解释。作者认为,这种方法忽视了一个强大的内置“计算机”:微型器官,比如胰岛,它们天然同时感知多种信号并将其转化为协调的反应。每个胰岛包含若干分泌激素的细胞类型,这些细胞不断相互沟通。它们共同将血糖维持在狭窄且安全的范围内,不仅对葡萄糖反应,还会对氨基酸、肠道和应激激素以及体内近期的高低血糖历史作出反应。他们提出,这种内在复杂性可以被利用来产生比简单的葡萄糖氧化酶传感器更丰富、更可靠的信息。
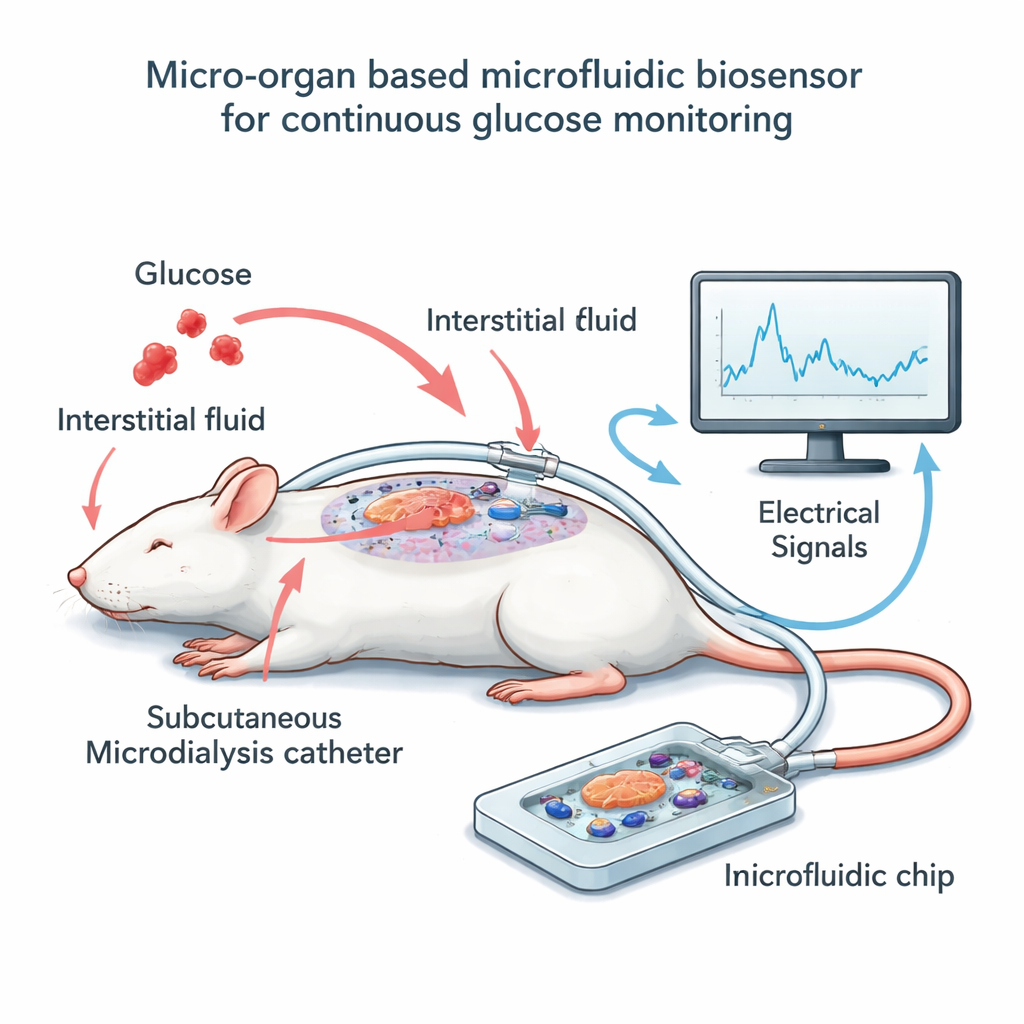
构建芯片与导管系统
为验证这一想法,团队在体外构建了一个小型装置,将几十个小鼠胰岛置于显微电极网格之上。研究者并未直接将这些细胞浸泡在血液中,而是使用了一种称为微透析的技术:一根薄而柔性的导管置于麻醉大鼠皮下,缓慢收集周围组织液,该组织液与血糖密切相关但有短暂延迟。低而恒定的流速将该液体通过狭窄通道流经芯片上的胰岛。随着透析液中葡萄糖水平的升降,胰岛的电活动发生变化,电极将其捕捉为缓慢的波状信号。与此同时,研究人员定期测量大鼠血液和透析液中的葡萄糖,使他们能够将电信号读数与实际血糖水平随时间对齐。
活体传感器对糖变化的响应
首先,科学家测试了电极上的胰岛是否能对真实血液成分而非简单实验室溶液作出反应。他们将胰岛暴露于不同葡萄糖水平的人血清和大鼠血清中,观察到电波的频率和幅度都呈明显的分级变化。这些响应足够强烈,能在与糖尿病相关的范围内区分小幅度的浓度变化。随后他们转入大鼠实验证明效果:先注射葡萄糖使血糖上升,随后注射胰岛素使其下降。在考虑血液到组织液及流经管道所需的时间延迟后,他们发现胰岛缓慢电信号的频率几乎与血糖同步上升和下降。跨多只动物的统计分析显示,信号频率与葡萄糖水平之间存在异常紧密且可重复的关系,而信号幅度虽有信息量,但变异性稍大一些。
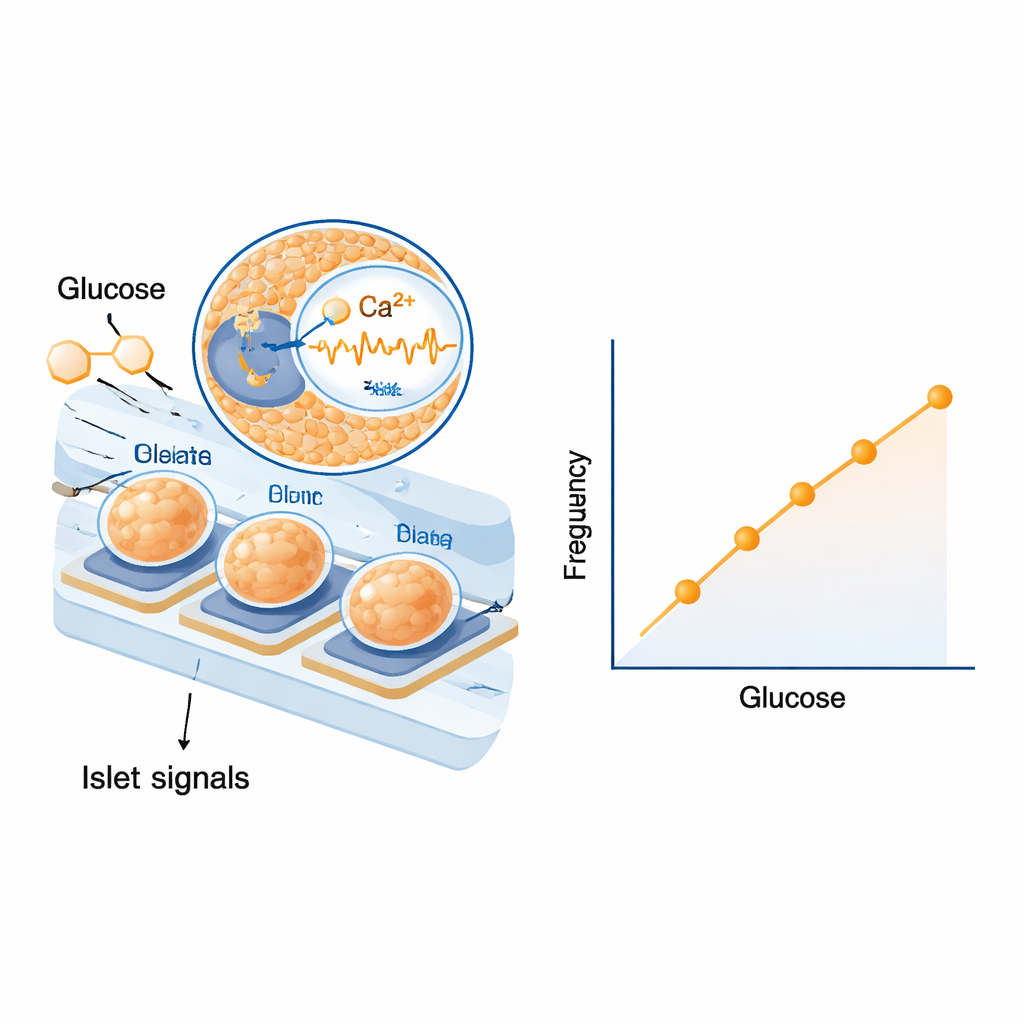
生物学带来的内在安全特性
使用完整胰岛而非单一分子的一个重要优势在于,其行为已包含由进化塑造的安全机制。早期研究和本研究的线索显示,胰岛在血糖下降时的反应通常比上升时更强——这是一种有助于防止危险性低血糖的“滞后”形式。电活动模式也受邻近细胞类型的影响,这些细胞会根据机体需要放大或抑制胰岛素释放。因为芯片只是监听这些集成信号而不加入染料或进行基因改造,便可在不损害细胞的情况下记录数日。作者指出尚存技术挑战,例如避免气泡、确保长期微透析性能以及最终应使用何种来源的人源或干细胞衍生胰岛。不过,基于既有糖尿病模型的计算机模拟表明,这种基于胰岛的传感器在复杂条件下可能与甚至超越现有葡萄糖监测器。
这对未来糖尿病护理的意义
这项工作表明,少量胰腺微型器官在小芯片上保持存活并通过一根细导管与机体相连,可以通过其自然的电活动在活体动物中持续追踪血糖。对非专业读者而言,关键信息是:与其要求一个简单化学传感器测量葡萄糖然后靠计算机推断其对机体的意义,不如直接倾听那种通常决定释放多少胰岛素的活组织。如果进一步改良并实现人体使用,这类活体生物传感器可能成为真正自治人工胰腺系统的核心——能够安静地预测机体需求,减轻糖尿病日常管理的负担。
引用: Puginier, E., Pirog, A., de Gannes, F.P. et al. A micro-organ based microfluidic biosensor for continuous monitoring of glucose levels in vivo. npj Biosensing 3, 12 (2026). https://doi.org/10.1038/s44328-025-00077-4
关键词: 连续血糖监测, 人工胰腺, 胰岛, 微流体生物传感器, 1 型糖尿病