Clear Sky Science · zh
载脂蛋白对动脉粥样性冠状动脉斑块影响的叙述性综述
为何血液中的脂类仍然重要
心肌梗死和中风常常始于供心血管的无声血管改变。本文超越了常说的“好”“坏”胆固醇,关注携带脂质通过血流的蛋白外壳——载脂蛋白。通过追踪四种载脂蛋白如何影响冠状动脉斑块(阻塞心脏动脉的脂质堆积)的生长、成分和治疗,作者说明为何有些人在胆固醇指标看似理想时仍然处于心脏病高风险。
隐藏在胆固醇上的“推手”
我们大多数人听说过低密度和高密度脂蛋白胆固醇,但这些颗粒上都包裹着一种或多种载脂蛋白,决定颗粒去向及其危险性。本综述聚焦四类关键载脂蛋白:载脂蛋白(a)、载脂蛋白A‑I、载脂蛋白B和载脂蛋白C‑III。它们共同控制脂质颗粒的组装、在循环中的停留时间以及进入并损伤动脉壁的难易程度。现代成像工具——动脉内超声、高分辨率光学成像和CT血管造影——现在让医生不仅能看到动脉狭窄程度,还能判断斑块是柔软易破裂还是致密钙化。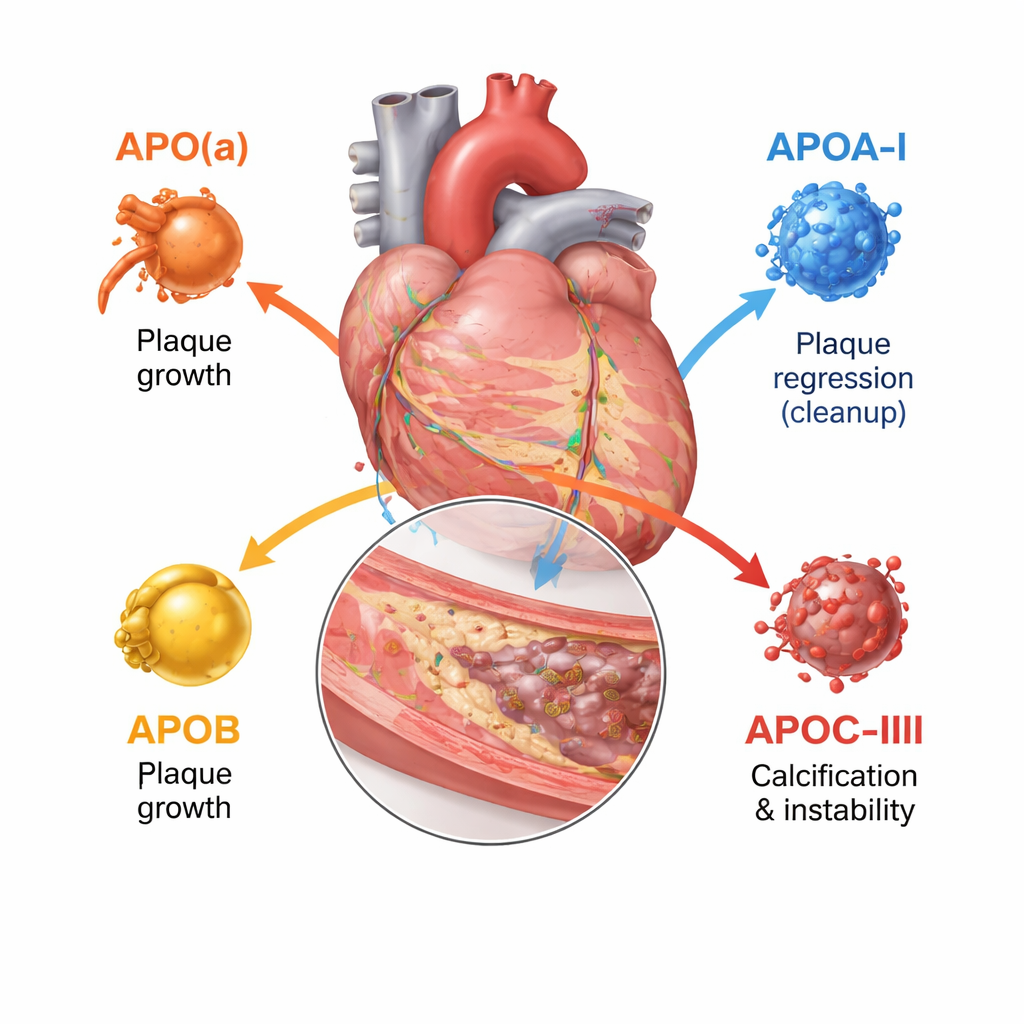
四种蛋白如何塑造危险斑块
载脂蛋白B位于每一个LDL及类似颗粒表面,实际上可用来计数血液中动脉粥样化——堵塞动脉的——颗粒数量。携带ApoB的颗粒越多且在循环中存在越久,冠状动脉中的总斑块负荷越大。基于心脏动脉内成像的研究显示,较高的ApoB水平与更大的斑块、较长的病变长度、更多柔软的坏死核心以及更少的稳定性钙化沉积相关。相反,载脂蛋白A‑I是HDL的主要蛋白,帮助从斑块细胞清除胆固醇并将其送回肝脏。更高的功能性ApoA‑I活性以及HDL胆固醇相对于ApoA‑I的有利平衡与斑块生长更慢、组织更纤维化、更稳定相关,尽管单纯提高血液中HDL胆固醇并未转化为更少的临床事件。
一种特殊的风险蛋白与促硬化者
载脂蛋白(a)与一个类似LDL的核心结合形成称为脂蛋白(a)或Lp(a)的颗粒。Lp(a)几乎完全由遗传决定,通常不受饮食影响。数千名患者的成像研究表明,Lp(a)高的人总体斑块更多,低密度、富含脂质的区域更多,以及更多局灶性的“高危”斑块——这些斑块易于破裂,即使LDL胆固醇已经被积极控制。综述认为,Lp(a)代表一种主要的“残留风险”,常规降胆固醇疗法难以完全覆盖。载脂蛋白C‑III主要存在于富含甘油三酯的颗粒上,减缓其清除并促进炎症。ApoC‑III较高的人冠状动脉钙化更多,斑块内更常见复杂的钙化结节,这些特征与晚期疾病和动脉硬化相关。
针对正确靶点的新药物
由于这些蛋白比单独的胆固醇更精确地反映风险,它们正成为直接的药物靶点。针对Lp(a)的几种注射型基因药物——反义寡核苷酸和小干扰RNA药物——在早期试验中可将水平降低80–95%,一种抑制颗粒组装的口服药也显示出大幅降低。针对ApoC‑III的新获批疗法可以显著降低甘油三酯和ApoC‑III本身,早期数据提示它们可能减少胰腺炎并有潜力改变斑块钙化。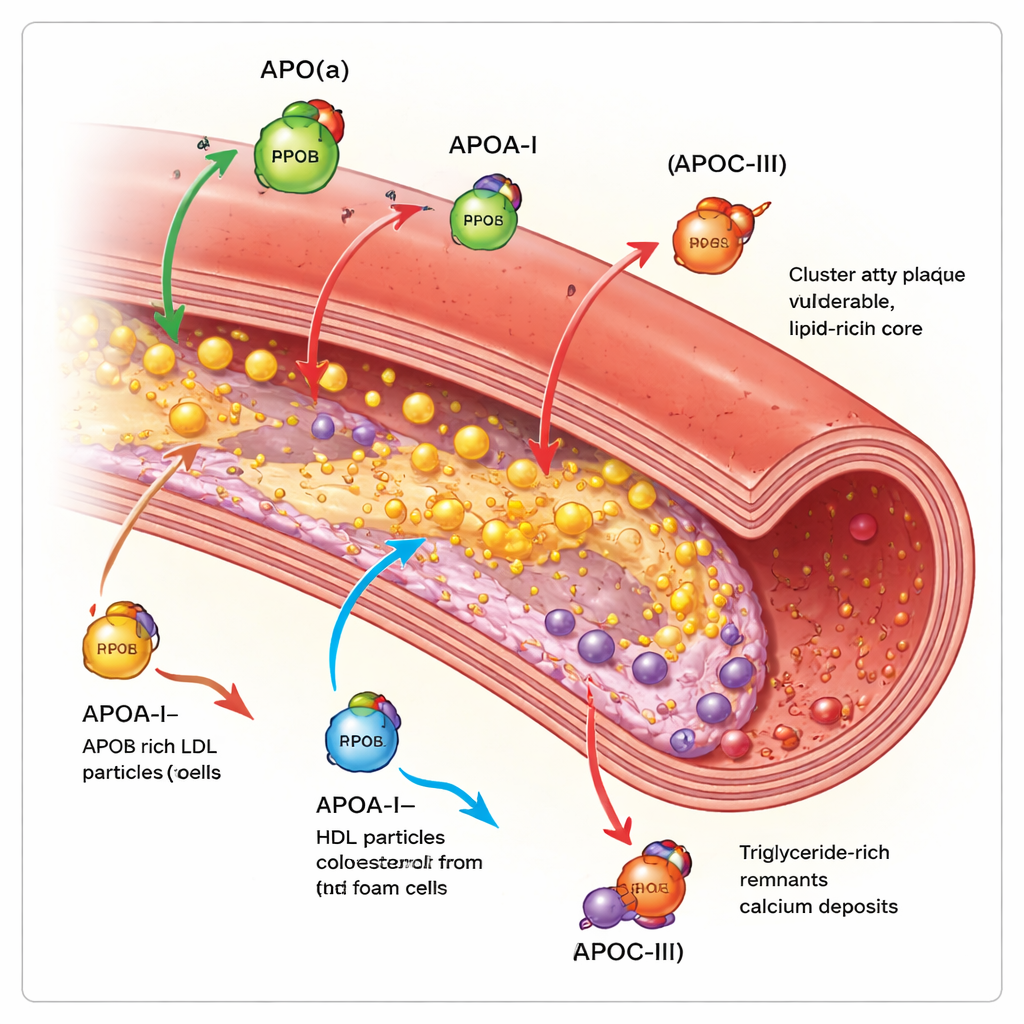
这对保护心脏意味着什么
简言之,本综述认为,谁会发生心肌梗死并非仅由胆固醇水平决定,而是由携带胆固醇的蛋白包被颗粒的种类和行为决定。ApoB反映多少“有害”颗粒冲击动脉壁,ApoA‑I反映将胆固醇清除的系统,Lp(a)增加额外的、由遗传设定的风险,ApoC‑III则倾向于产生硬化、炎症性的斑块。针对性降低Lp(a)和ApoC‑III的新药,以及在常规检测中更精确地使用ApoB和ApoA‑I,可能使医生能够根据每位患者的斑块生物学定制预防策略,发现常规血脂检测遗漏的隐性风险。
引用: Fukase, T., Dohi, T. A narrative review of impacts of apolipoproteins on atherosclerotic coronary plaques. npj Cardiovasc Health 3, 4 (2026). https://doi.org/10.1038/s44325-026-00104-x
关键词: 脂蛋白(a), 载脂蛋白B, 载脂蛋白A-I, 载脂蛋白C-III, 冠状动脉斑块成像