Clear Sky Science · zh
减缓神经退行性改变的生活方式策略及其机制启示
日常习惯为何影响大脑老化
随着人们寿命延长,越来越多的人开始担心记忆力下降、痴呆以及像阿尔茨海默病这样的疾病。本文综述探讨了一个令人鼓舞的观点:日常选择——我们如何进食与活动——能够影响大脑老化的速度。作者并非把注意力放在新药上,而是梳理了大量动物与人类研究,评估特定饮食与运动模式是否能保护脑细胞、延缓衰退,并可能降低神经退行性疾病的风险。
大脑随时间如何退化
阿尔茨海默病及相关痴呆目前影响着全球超过5500万人,且这一数字正快速上升。在大脑深处,这些疾病以粘性的蛋白质沉积(称为淀粉样斑块)、另一类蛋白tau的缠结、持续性炎症,以及神经细胞与脑体积的逐步丧失为特征。现有药物,包括某些能清除部分淀粉样蛋白的新型抗体药物,虽然能在一定程度上减缓症状,但不能阻止或逆转疾病。许多患者因副作用或费用原因无法使用这些药物。因此,研究者开始认真关注可以与药物协同作用——或为从未接受药物治疗的人提供帮助的生活方式策略。
将身体燃料“切换”的饮食模式
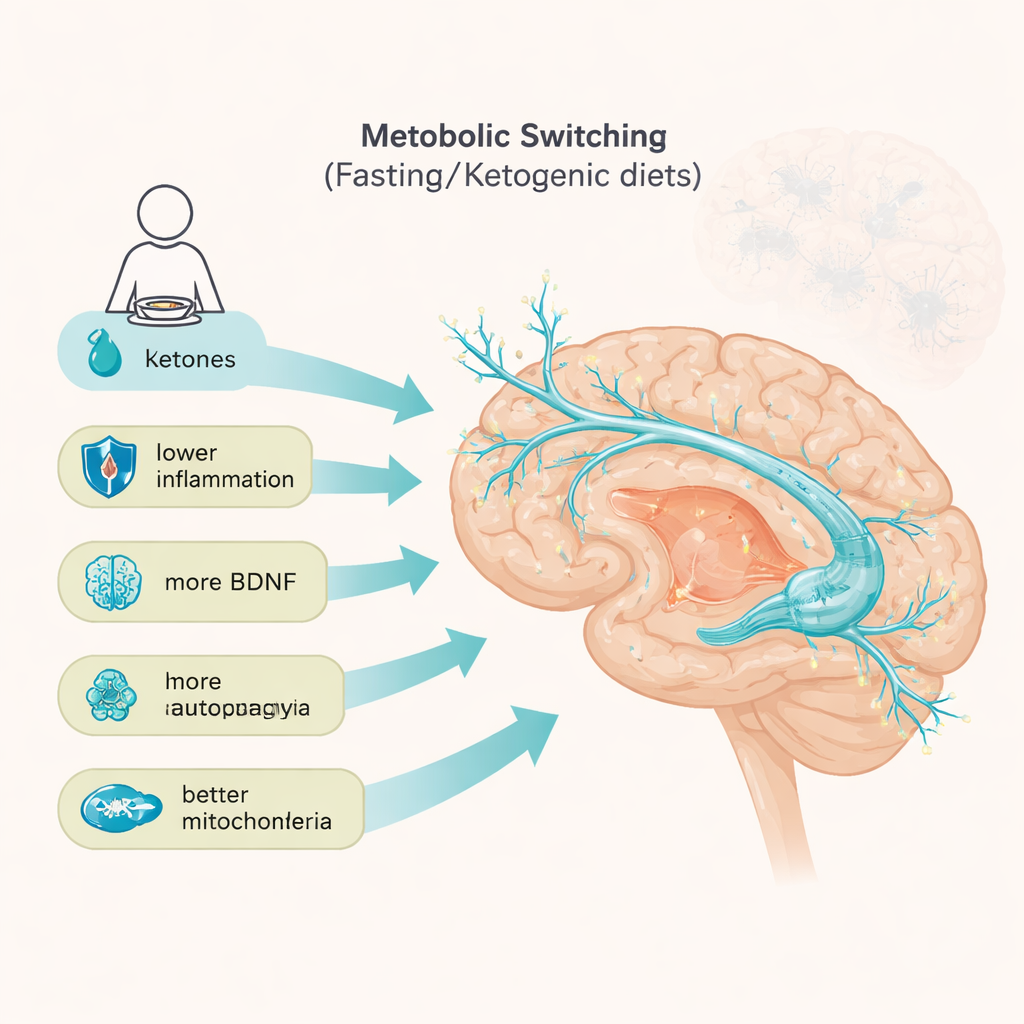
文章的一个主要关注点是“代谢切换”,即身体周期性地从燃烧糖转向燃烧脂肪与酮体。这种切换可通过间歇性禁食、限时进食(例如每天仅在8–10小时窗口内进食)、隔日禁食,或极低碳水的生酮饮食实现。在动物研究中,这些模式一致地减少了大脑炎症与氧化应激,促进大脑的天然清洁系统(称为自噬),并降低有害蛋白的堆积。禁食与酮体还会提高脑源性神经生长因子(BDNF)的水平,BDNF支持神经连接的生长、生存与可塑性。早期的人类研究,包括在多发性硬化或轻度记忆问题患者中的小型试验,表明禁食式方法可改善脑体积、炎症标志物、睡眠以及部分认知测量,但仍需更大规模和更长期的研究来确认。
少吃且更高质的饮食
热量限制——在不导致营养不良的前提下摄入比平常更少的热量——长期以来被证实可延长多种物种的健康寿命。在聚焦大脑的实验中,动物减少热量摄入常常能降低淀粉样斑块负担、抑制脑内炎症、改善能量产生的线粒体功能,并激活与禁食相似的多种保护性通路,包括BDNF与与健康老化相关的SIRT蛋白家族。由于严格的热量限制和严苛的禁食对某些人来说难以坚持或不安全,作者也评估了高质量饮食模式的证据,如地中海饮食、DASH饮食和MIND饮食。这些饮食富含蔬菜、水果、全谷物、坚果、橄榄油和鱼类,能提供抗氧化物和有益脂肪,同时限制高度加工食品。在动物模型中,橄榄油等植物性成分能减少炎症与氧化损伤、支持线粒体功能,有时还能降低淀粉样蛋白与tau的水平。大型人群队列研究显示,更接近MIND类饮食与生物学老化减慢和痴呆风险降低相关,尽管最近的一项为期三年的试验尚未单独显示明确的认知优势。
运动作为大脑的强心剂
运动被视为一种强大且多面向的大脑保护因子。在阿尔茨海默和帕金森小鼠模型中,有氧运动可减少神经细胞死亡、降低淀粉样蛋白积聚、改善线粒体健康并刺激自噬与“线粒体自噬”(清除受损线粒体的定向回收)。运动还释放“运动因子”(exerkines)——如BDNF、Irisin以及酮体β-羟基丁酸等信号分子,似乎能增强突触功能并促进新神经元的生成。重要的是,身体活动还可以重塑肠道微生物组,从而减轻炎症。在人类研究中,多成分运动项目(有氧加力量与平衡训练)通常会提高血中BDNF水平并能改善认知技能与大脑健康标志,具有更好体能或更多瘦体重的人群其发生阿尔茨海默病的风险往往较低。
对日常生活的启示
作者的结论是,没有单一的生活方式改变能成为神奇的治疗方法,但综合证据强烈表明,饮食与运动可以影响驱动大脑老化的生物学过程。那些鼓励周期性代谢切换、适度热量减少、高质量饮食与规律身体活动的方法,都汇聚到一组共同益处:更少的炎症、更好的细胞清洁、更健康的线粒体以及更少的有毒蛋白沉积。仍有许多问题有待解答——例如应何时开始、习惯需多严格或持续多久、以及如何最好地将这些策略与药物结合——但总体信息是充满希望的。审慎的餐桌选择与终生持续的身体活动是减缓神经退化、支持更健康老年大脑的有前景且可及的工具。
引用: Gunning, J.A., Hernandez, M.I., Gudarzi, B. et al. Lifestyle strategies and mechanistic implications for slowing neurodegeneration. npj Metab Health Dis 4, 10 (2026). https://doi.org/10.1038/s44324-026-00101-9
关键词: 阿尔茨海默病, 间歇性禁食, 地中海饮食, 热量限制, 运动与大脑健康