Clear Sky Science · zh
使用对称色散双楔棱镜在光谱单分子定位显微镜中最大化光子利用率
更清晰地观察微小世界
许多生物学中最重要的主角——位于细胞内的单个分子——远小于常规显微镜的分辨极限。过去十年,新的“超分辨率”方法改变了这一点,但这些方法常常要求研究者在成像清晰度与色彩信息或繁复的实验之间做出权衡。本文介绍了一种巧妙的光学附加模块,帮助研究者同时在三维中以更高的细节和更少的麻烦观察多种分子。
逐一观察单个分子
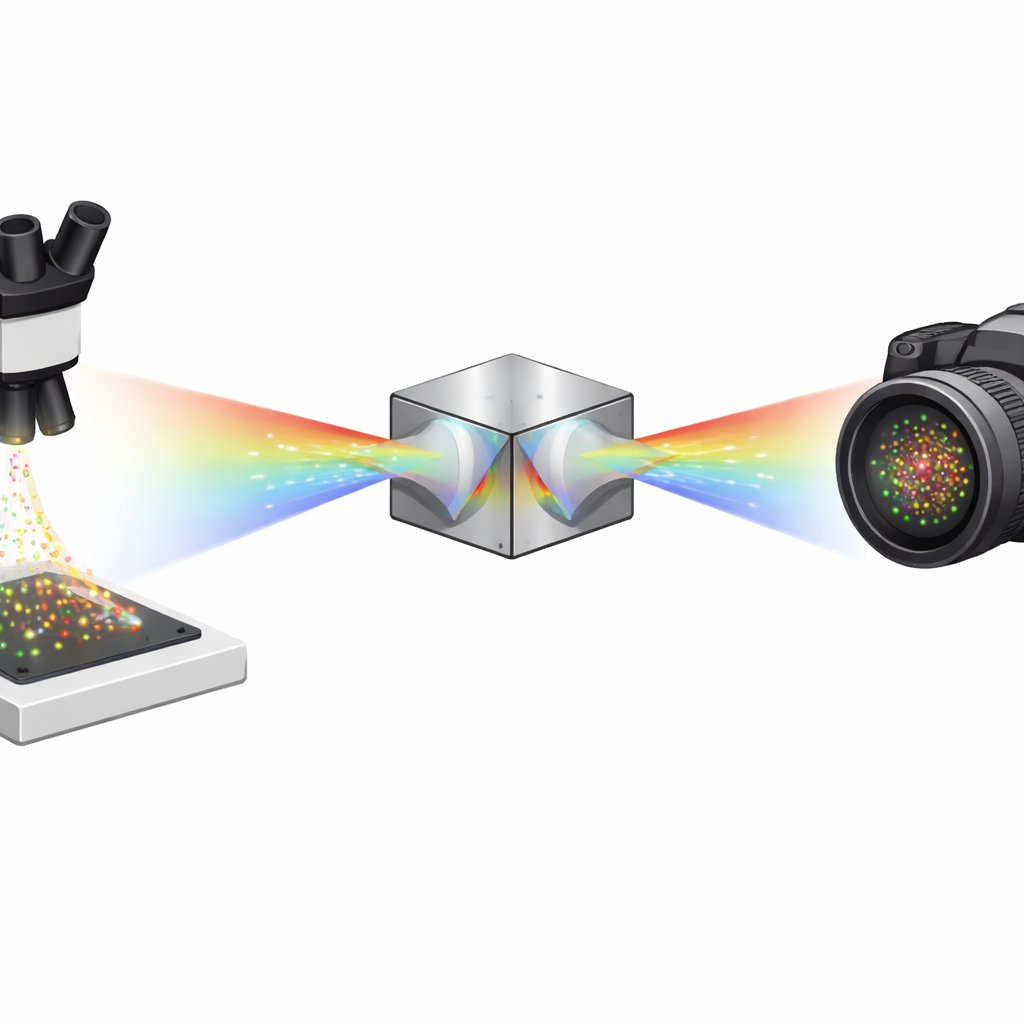
像 STORM 和 PALM 这样的超分辨率方法通过让只有少数荧光分子在任一时刻闪烁,然后以高精度定位每次闪烁,并把成千上万帧合成成详细图像来工作。光谱单分子定位显微镜(sSMLM)更进一步:它不仅确定每个分子的位置,还测量其颜色光谱。额外的光谱信息非常有用,因为它允许研究者使用光谱有重叠的多种染料并仍能区分它们。问题在于,传统 sSMLM 通常必须在“位置”图像和“光谱”图像之间分配宝贵的光子,这会模糊最终图像并使微弱分子难以检测。
每个光子同时发挥双重作用
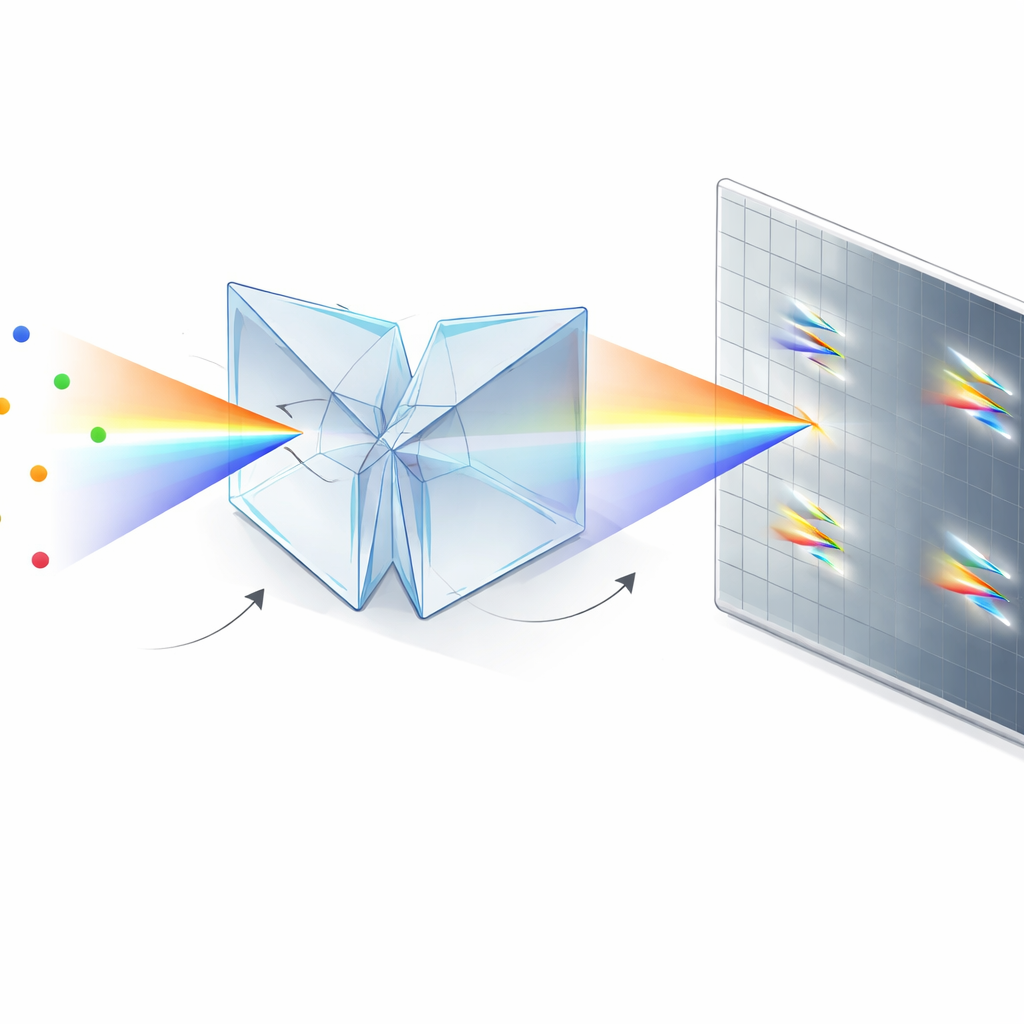
作者通过一个基于两块相同双楔棱镜和一个分束器的紧凑光学模块解决了这一问题。他们不是将光子送入“位置”通道和单独的“颜色”通道,而是其对称色散双楔棱镜(SDDWP)设计在同一相机上为每个闪烁的分子产生两份镜像的、经光谱展开的图像副本。由于这两幅图像完全对称,简单计算即可同时恢复分子的真实位置(由两斑点中点确定)和其光谱(由斑点间距决定)。实际上,所有收集到的光子既为空间信息贡献,也为光谱信息贡献,从而显著提高了系统定位和识别每个分子的精度。
在三维中获得更锐利、更清晰的颜色
通过解析模型和经过精心校准的测试样品,团队表明与他们先前的棱镜系统相比,SDDWP 在横向(平面内)定位精度上提高了约 27%,在光谱精度上提高了约 48%。随后他们将设计扩展到三维成像,采用“双平面”方法,其中两个光谱图像分别在相反方向上略微失焦。通过分析两个平面上每个斑点尺寸的变化,系统可以确定分子位于焦平面上方或下方的距离,在大约半微米的有用深度范围内实现约 18 纳米量级的轴向精度。尽管增加了三维成像的复杂性,新设计仍保持接近二维水平的光谱清晰度,允许在光谱强烈重叠的染料间进行非常细致的区分。
在细胞结构和运动颗粒间分离颜色
为演示其实用性,研究者使用单一红色激光和三种通常光谱重叠的远红染料对固定 HeLa 细胞进行了三维成像。他们标记了过氧化物酶体、微管和线粒体,并展示系统能够在保持各深度上高空间细节的同时,基于微妙的光谱差异可靠地区分这些结构。他们还使用光谱不同的量子点作为微小标记,在黏性溶液中同时追踪大量运动颗粒。将每个颗粒的光谱视为独特的“指纹”后,SDDWP 配置能够准确追踪数百条在高密度下本会在路径交叉时变得纠结的轨迹,在颗粒密度接近理论极限时也能将跟踪误差降至仅几个百分点。
从复杂光学到简单附加件
除了性能外,该方法的一个关键优点是实用性。SDDWP 单元是一个小型、主要为整体结构的组件,可固定在标准倒置荧光显微镜的侧出射口,仅需适度对准。其基于棱镜的设计比衍射光栅浪费更少光子,并且机械上足够稳定,经过例行检查即可在较长时间内保持校准。这使其成为许多现有单分子实验室的现实升级路径。
这对未来显微镜学意味着什么
通过重新思考光的分割与重组合,这项工作表明可以从相同的有限光子池中同时获得更清晰的位置和更明确的颜色信息。通俗地说,它让研究者在拥挤的三维环境中区分更多种类的分子,并同时跟踪许多被标记的颗粒,而不会牺牲图像质量。随着该技术的采用与改良——甚至可能用于用温和红光进行活细胞成像——它有望成为探索复杂分子装配体和细胞器如何组织及其在活细胞内如何运动的多功能工具,分辨尺度达纳米级别。
引用: Yeo, WH., Brenner, B., Shi, M. et al. Maximizing photon utilization in spectroscopic single-molecule localization microscopy using symmetrically dispersed dual-wedge prisms. npj Imaging 4, 20 (2026). https://doi.org/10.1038/s44303-026-00152-z
关键词: 单分子显微镜, 超分辨率成像, 光谱成像, 三维细胞成像, 单粒子跟踪