Clear Sky Science · zh
使用纳米颗粒作为通用螺母的一步放射性标记策略,适用于 PET、SPECT 和治疗性放射性核素
为何微小的放射性颗粒重要
现代癌症治疗越来越依赖能够同时成像与治疗肿瘤的放射性药物,这类药物可以在扫描中将肿瘤照亮,并在某些情况下从内部对其进行破坏。然而,每种新放射性药物的研发通常慢且繁琐,因为大多数设计必须围绕特定的放射性金属量身定制。本研究探讨了一种截然不同的方法:使用一种基于铁的纳米颗粒作为“通用插座”,可以容纳多种用于成像与治疗的医学同位素,可能加速此类药物的制备与优化。
从多把钥匙到一个锁
当前的放射性药物通常依赖被称为螯合剂的化学“爪子”来抓住金属原子并将其连接到抗体或其他靶向分子上。每种放射性金属往往需要其专属的螯合剂及配方——温度、酸碱度和反应时间等条件都会变化。对于一些重要的医疗金属,尤其是用于强力α粒子治疗的同位素,仍缺乏理想的螯合剂。作者认为,这种逐金属定制的方式已成为瓶颈:可用同位素的名单在不断扩大,而相应的化学处理方法跟不上需求。
将纳米颗粒作为通用插座
为了解决这一问题,研究者转向了非常小的氧化铁纳米颗粒,这种材料已在磁共振成像(MRI)对比剂方面有所探索。他们设计的颗粒具有约三纳米宽的氧化铁核,并由柠檬酸分子包覆以维持血液中的稳定性。在单一步骤、耗时10分钟且借助微波辅助的合成过程中,他们向核中掺入了十种常用于 PET、SPECT 或体内放射治疗的不同放射性金属之一。这种一锅法工艺产出的颗粒尺寸一致、产率高,且关键是在人血清中具有优异的稳定性——即便是对传统螯合剂来说具有挑战性的治疗性同位素,如镭‑223 和 锕‑225,其衰变产物也能被很好地束缚住,不易逸散。
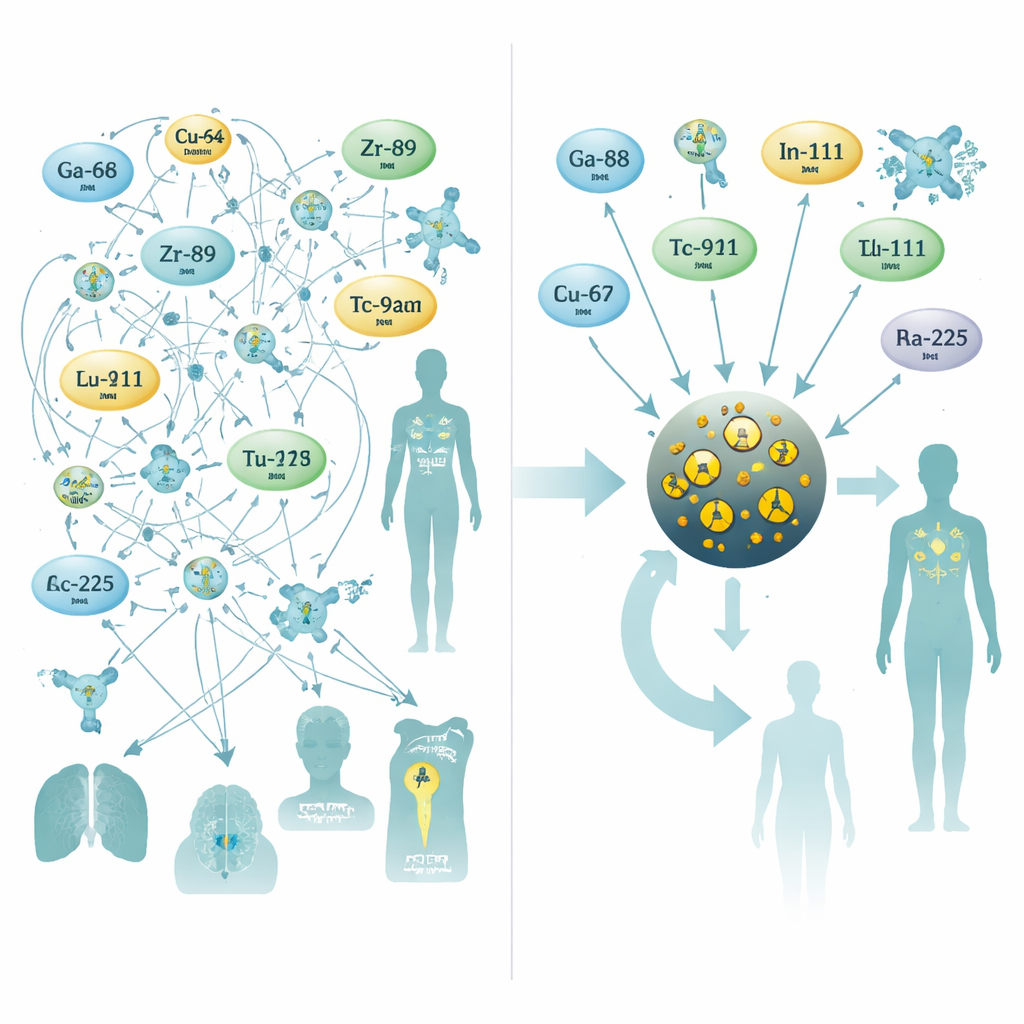
用于成像血栓与脑肿瘤
在证明可以将多种同位素困于相同纳米颗粒设计后,团队在活体动物中测试了这些“纳米示踪剂”的功能。在小鼠胶质母细胞瘤模型中,标记有镓‑68 的颗粒通过静脉注射进入血流,并以 PET 与 MRI 联合成像。颗粒在足以破坏血脑屏障的肿瘤处富集,使相同配方既能提供明亮的 MRI 对比,又能产生灵敏的 PET 信号。在另一项实验中,研究者对颗粒进行了化学修饰,使其能通过高度选择性的 click 反应与定位于血栓内激活血小板的抗体“快速拼接”。在颈动脉受损的小鼠中,这种两步的“预靶向”策略在血栓部位产生了清晰的 PET 信号,而对照组动物则未显示该热点。
从诊断到治疗与更安全的清除
同一平台也被用于递送治疗。当装载有镥‑177 的纳米颗粒直接注入小鼠的胶质母细胞瘤肿瘤内时,颗粒在至少两周内大多局限于肿瘤组织。在此期间,未治疗的肿瘤体积增长到数倍,而接受治疗的肿瘤则停止生长,这表明局部放射剂量足以阻止进展。考虑到反复治疗可能导致肝脾铁负荷过重,研究团队随后调整了合成条件,制备出更小的颗粒——约四到五纳米——足够小以被肾脏滤过。这些缩小的颗粒仍能牢固携带放射性载荷,但能迅速通过膀胱排出,降低了在主要器官中的长期蓄积。
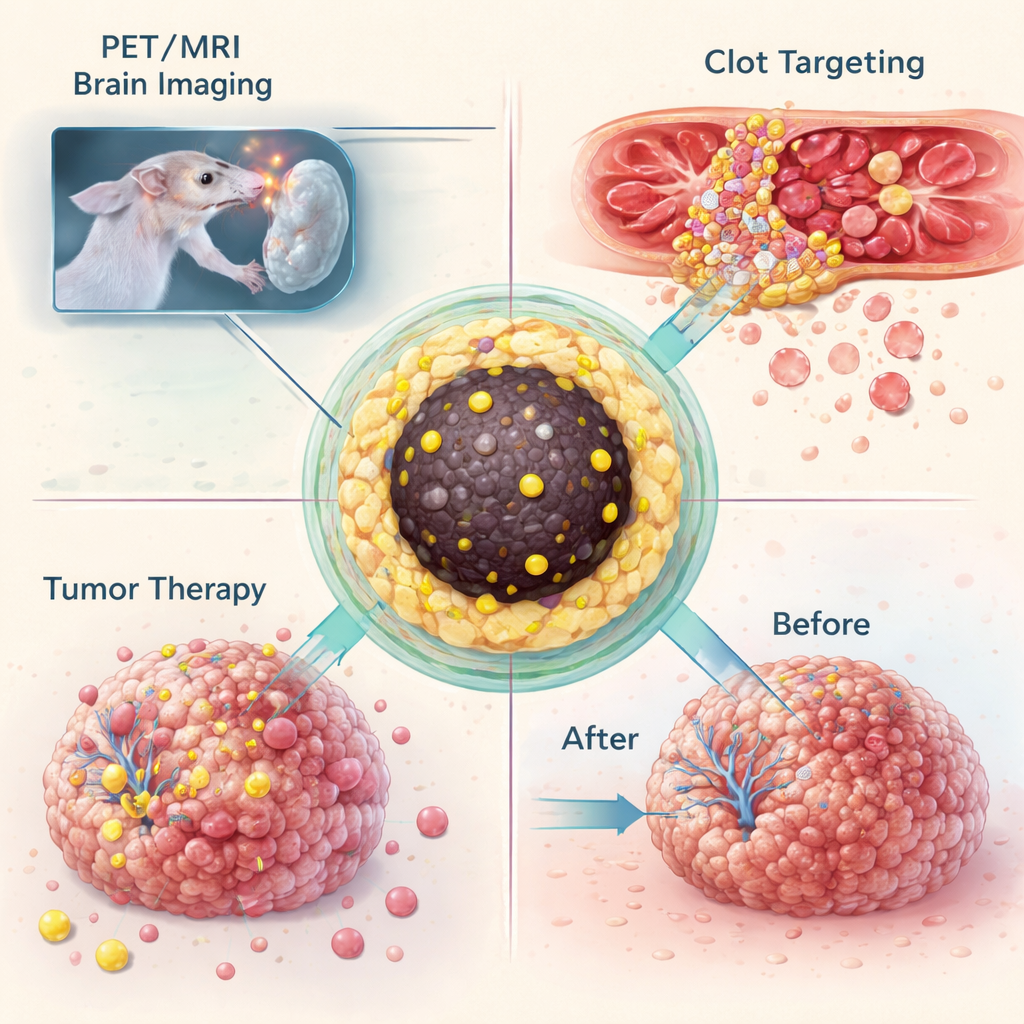
对未来癌症治疗的潜在意义
对非专业读者来说,核心信息是研究者构建了一个单一而灵活的纳米颗粒平台,可以与多种放射性金属配对,而无需每次都重新发明化学方法。在动物模型中,相同的基础颗粒既能帮助发现脑肿瘤、标记血栓、将放射性直接传递到肿瘤中,也能被调节为通过肾脏排出体外。尽管在临床应用之前仍需更多工作,这一方法为设计一系列具有相同行为特征、仅在所携带辐射类型上有所不同的诊断与治疗剂提供了有希望的路径。这种一致性可能简化开发流程、改善安全性评估,并最终使先进的核医学工具更广泛可及。
引用: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
关键词: 放射性治疗诊断学, 纳米颗粒, PET 成像, 多形性胶质母细胞瘤, 靶向放射治疗