Clear Sky Science · zh
在杂交小鼠模型中加速并局部化的α-突触核蛋白病:对正电子发射断层扫描研究的启示
这项研究为何重要
帕金森病以震颤和运动障碍最为人所知,但在大脑深处它始于难以察觉的微小变化。临床医生迫切需要能够早期发现这些变化的方法,并快速评估新药物。该研究描述了一种改良的小鼠模型,能在仅几周内在非常特定的大脑区域重现帕金森样脑损伤的关键特征,且专为使用称为 PET 的高级脑成像技术而设计。 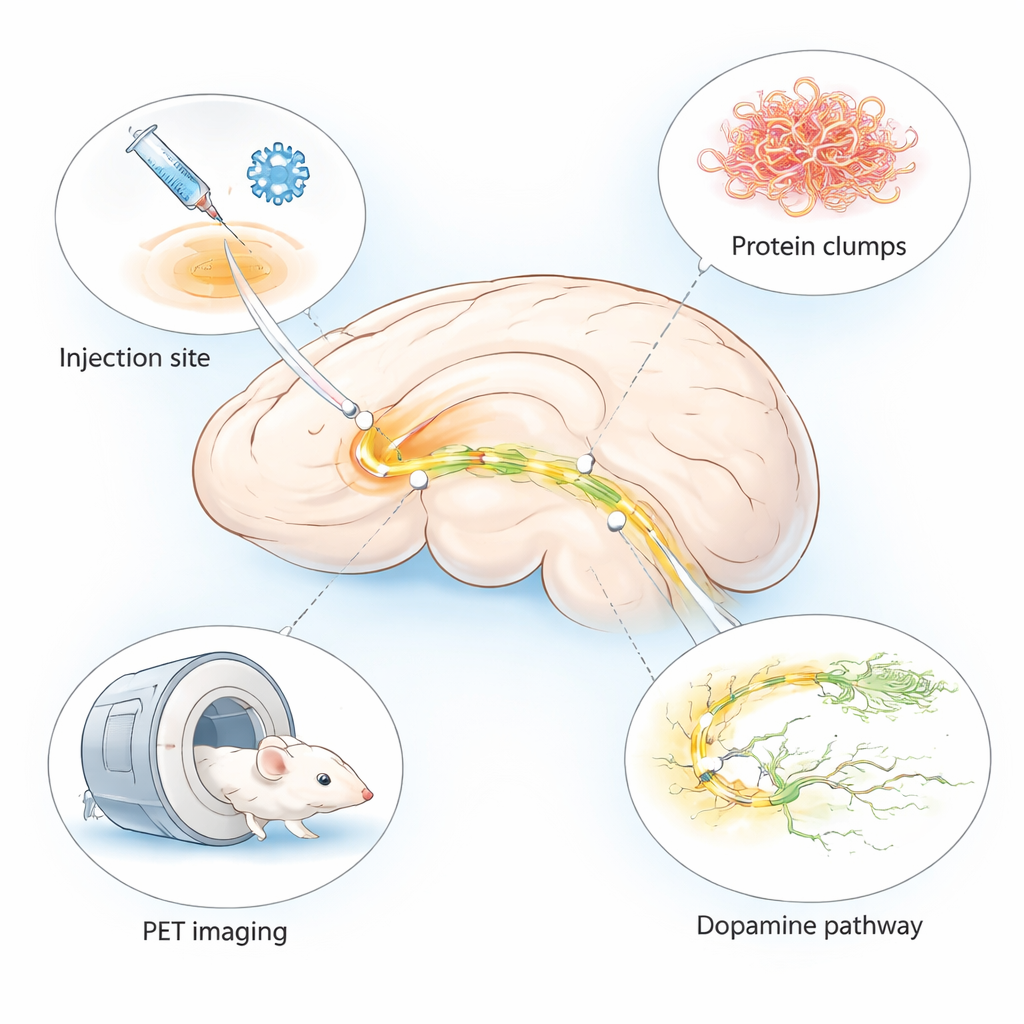
构建更快、更聚焦的疾病模型
许多现有的帕金森病动物模型需要数月才能出现症状,或无法显示患者大脑中观察到的全部改变。作者将两种既有方法结合成一种“杂交”模型:他们注入一种无害的病毒,使脑细胞产生人源 α-突触核蛋白——一种在帕金森病中会聚集的蛋白质——并同时注入预先形成的纤维(pre-formed fibrils),这些纤维作为种子触发进一步聚集。两者都被送入小鼠大脑一侧的一个与运动相关的小区域——黑质。该设计在注射侧产生局部但强烈的类疾病改变,而另一侧则相对健康,可作为对照。
追踪蛋白聚集与神经细胞死亡
注射后仅两周内,小鼠在目标脑区就表现出高水平的人源 α-突触核蛋白及其异常磷酸化形式。在显微镜下,研究者观察到类似路易体和路易神经纤维的结构,这些是帕金森病的标志。接下来几周,这些异常沉积不断增加。与此同时,产生神经递质多巴胺——对平滑运动至关重要的细胞——开始消失。这类细胞的标志物在第五周时降至未受影响侧水平的约 60%,证实了多巴胺系统的明显且进行性丧失。
炎症、突触衰退与能量工厂疲乏
大脑的免疫细胞——小胶质细胞——在受损区域周围也转入高度活跃的炎性状态。对若干与炎症相关蛋白的染色在 α-突触核蛋白沉积附近明显强于对侧晚些时候,团队检测到突触的丧失——即神经细胞间用于通讯的微小接触点——以及线粒体(细胞的能量工厂)功能受损的迹象。综合这些发现表明,该模型不仅产生蛋白聚集;它还捕捉到了导致神经细胞死亡的连锁反应:炎症反应、连接失效和能量危机。 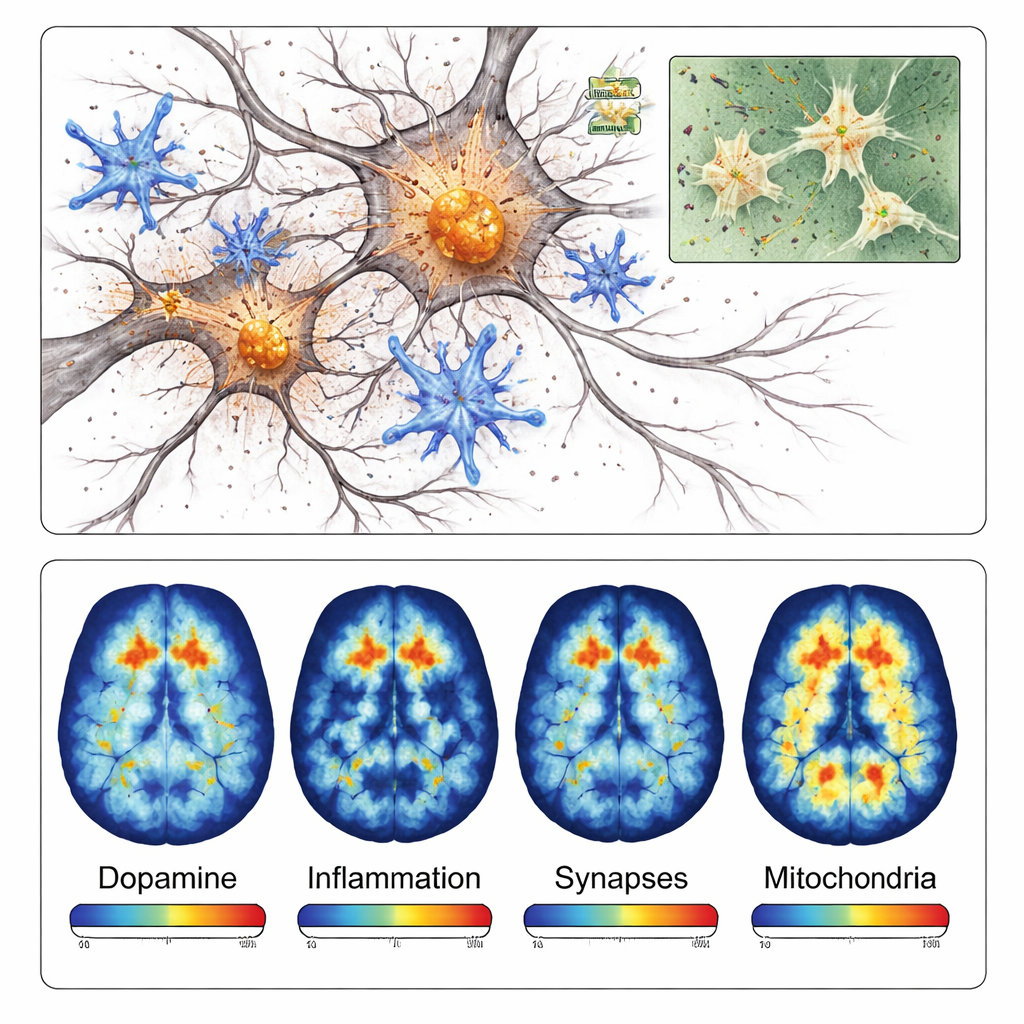
让 PET 扫描发挥作用
由于该模型为局部性且发展迅速,它特别适合用于正电子发射断层扫描(PET),这种扫描技术可在活体大脑中测量特定分子。研究者测试了四种不同的 PET 示踪剂,分别结合多巴胺神经末梢、炎性小胶质细胞、突触蛋白和线粒体酶。在每一种情况下,PET 扫描在注射侧均显示出与显微镜发现相吻合的信号减弱或增强。例如,靶向多巴胺通路的示踪剂在受损侧显示约 40% 的信号下降,而炎症示踪剂在受影响区域则显示超过 40% 的信号升高。
对患者与未来治疗的意义
这种新型小鼠模型在短时间内集合了许多人类帕金森病大脑中需历经数年才能出现的关键改变。由于损伤局限在小且明确的区域内,并可用 PET 扫描跟踪,研究者可以更高效地评估新的成像示踪剂和潜在疗法。虽然没有任何小鼠模型能完全复制人类状况,但这种方法提供了一个强大且实用的工具,有助于弥合基础实验与人体研究之间的差距,最终有助于改进诊断并加速寻找更好治疗方法的进程。
引用: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
关键词: 帕金森病, α-突触核蛋白, 突触核蛋白病, PET 成像, 小鼠模型