Clear Sky Science · zh
产前病毒感染对母体及子代免疫影响的机械性见解
病毒与妊娠:对家庭为何至关重要
每年都有数百万例妊娠在艾滋病毒、COVID-19 和流感等病毒暴发的阴影下发生。即便婴儿并未被直接感染,研究人员也发现母亲对这些病毒的免疫反应可以在孩子的健康上留下长期痕迹。本文综述汇集了最新研究,解释常见的产前病毒感染如何在不显眼处重塑子宫环境、胎盘和发育中的免疫系统,其影响可能从出生延续到成年。
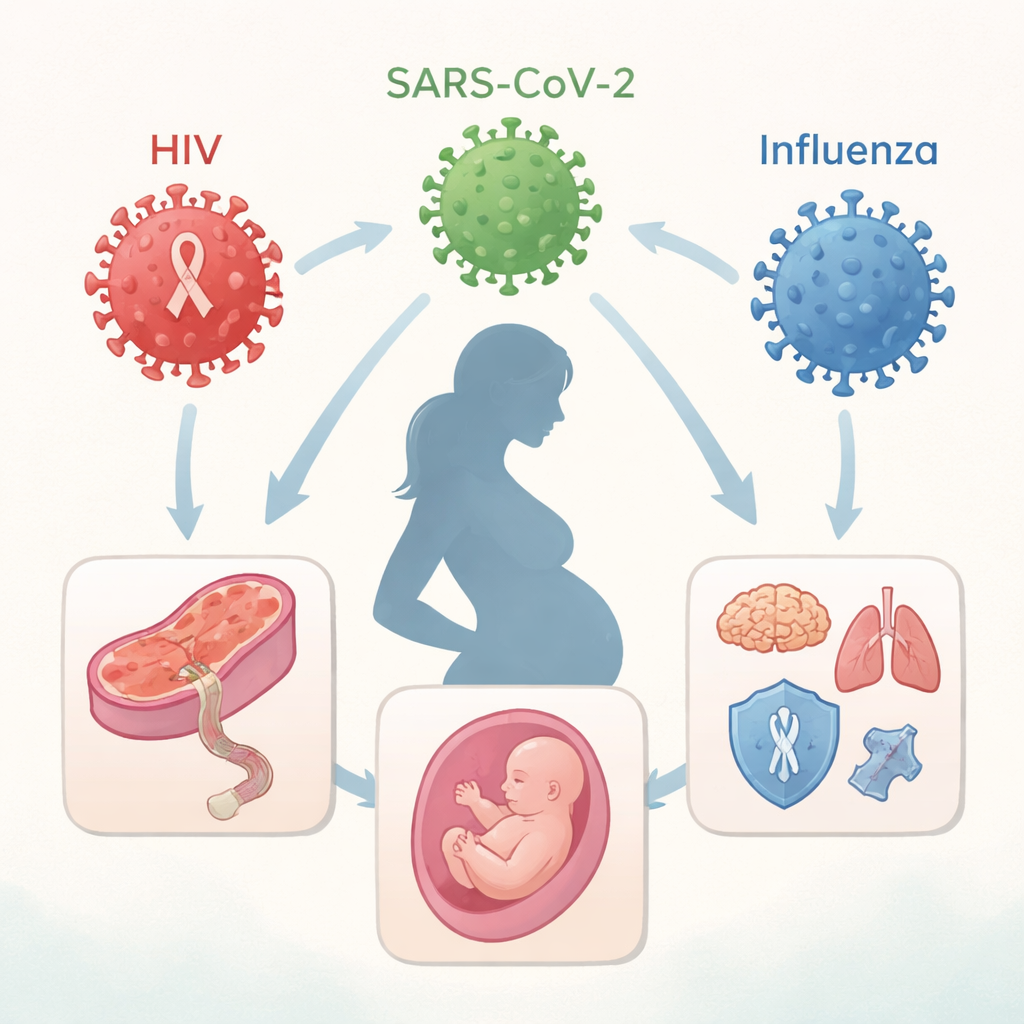
三种不同病毒、同样的挑战
文章聚焦三种全球重要的病毒:艾滋病毒(HIV)、SARS-CoV-2(引发 COVID-19 的病毒)和流感。这些感染在传播方式和持续时间上各不相同——HIV 为慢性感染,而 COVID-19 与流感通常为短期病程。但三者都可能扰乱妊娠期母体免疫的精细平衡。传统上,临床关注的重点主要是“垂直传播”,即病毒穿过胎盘直接感染胎儿。如今的证据表明,即便没有直接的胎儿感染,母体的免疫反应与炎症也能改变胎盘结构、影响血流和营养供给,并左右婴儿免疫与神经系统的发育。
胎盘如何成为战场
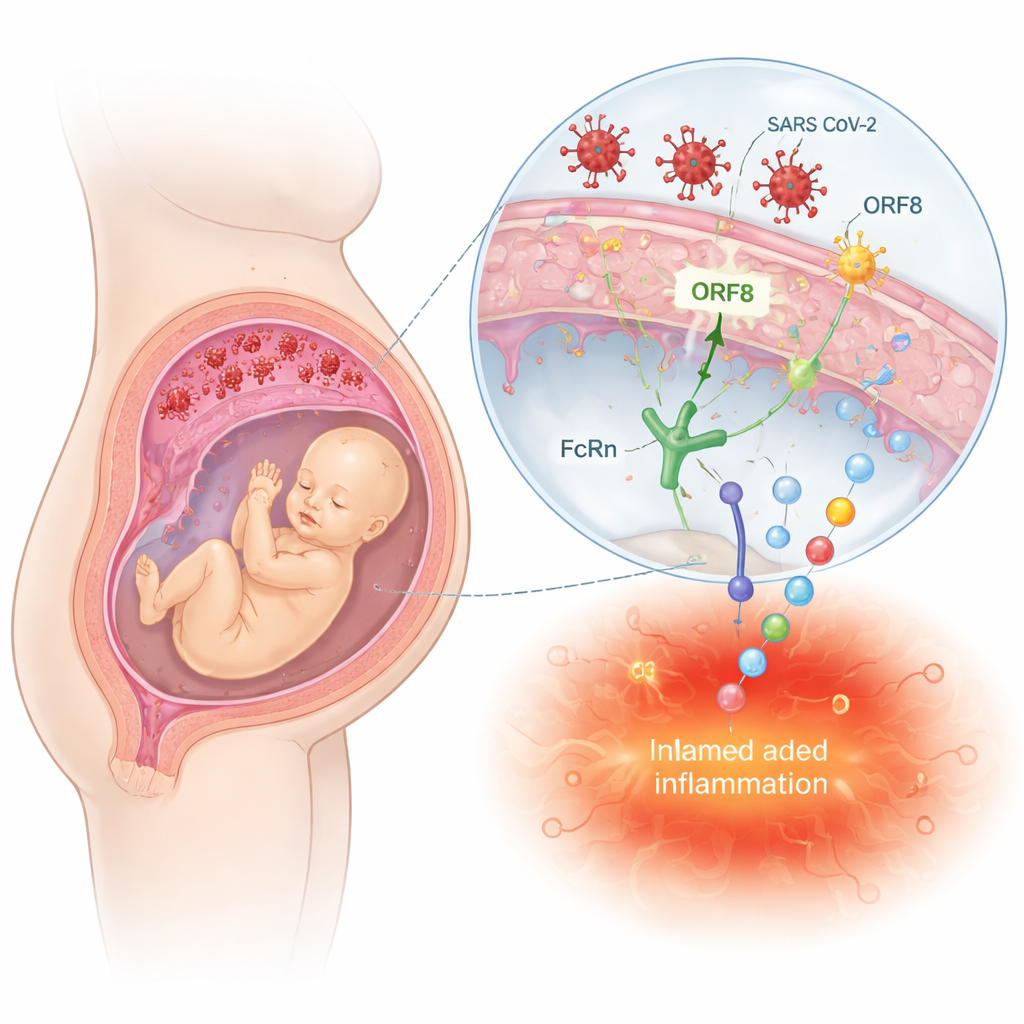
胎盘既是屏障也是桥梁,连接母体与胎儿。HIV 可以通过感染免疫细胞和胎盘细胞,或借助通常将保护性蛋白输送给胎儿的抗体“搭车”进入这一屏障。相比之下,SARS-CoV-2 和流感很少到达胎儿组织,但仍可损伤胎盘血管并引发炎性级联反应。综述描述了病毒蛋白(如 HIV 的 Tat 和 Nef 蛋白,或 SARS-CoV-2 的 ORF8 与刺突蛋白)如何与胎盘和免疫细胞中的受体及信号通路相互作用。这些相互作用可触发强烈的炎性反应、干扰抗病毒防御并扰乱激素的产生——这些变化可能不会导致明显的先天缺陷,但能在隐蔽中重新编程胎儿发育。
对子代免疫与大脑健康的持久印记
论文中一个重要观点是:产前感染可以以持续到出生后很久的方式“训练”婴儿的免疫系统。宫内暴露于 HIV 但出生时未被感染的婴儿,往往表现出关键免疫细胞数量与功能的改变、更高水平的炎性分子以及肠道菌群的差异。对于暴露于 SARS-CoV-2 的儿童以及动物研究中的流感暴露,类似的模式也在出现。这些早期变化与婴幼儿期更高的严重感染风险、疫苗反应差异以及过敏和免疫介导疾病风险增加有关。对于大脑而言,母体免疫激活——尤其是 IL-6 和 IL-17 等细胞因子的激增——在人与动物研究中与随后的神经发育问题相关,包括学习困难、行为问题,以及在某些情况下,自闭症和精神分裂症等疾病的发病率升高。
保护母婴:可以采取哪些措施?
综述还审视了临床护理如何发展以降低这些风险。对于 HIV,母亲早期且持续的抗逆转录病毒治疗,加上为新生儿量身定制的用药方案,已在许多环境中将直接传播率压低至 1% 以下,尽管与炎症相关的影响仍需仔细随访。对于 COVID-19 与流感,孕期接种疫苗是强有力的工具:接种疫苗的母亲可通过胎盘传递保护性抗体,降低婴儿在生命最初几个月住院的几率。新兴策略还包括单克隆抗体、小分子抗病毒药物以及能够在不压制必要免疫防御的前提下适度抑制过度炎症的疗法——这些方法都需要在孕妇人群中进行专门测试。
这对未来父母与儿童意味着什么
总体而言,文章得出结论:产前暴露于病毒不仅是直接的即时威胁,还是对健康的“长远赌注”。即便婴儿避免了直接感染,母体的免疫反应也能悄然塑造其免疫系统、脑发育与微生物组,影响其对感染的反应并可能改变成年后的慢性病风险。理解这些途径为更智能的疫苗、更安全的孕期抗病毒药物以及对暴露儿童的长期监测打开了大门。对家庭与临床医生而言,信息明确:妊娠期保护母体健康就是对下一代终身健康的投资。
引用: Salem, G.M., Azamor, T., Familiar-Macedo, D. et al. Mechanistic insights into the impact of prenatal viral infections on maternal and offspring immunity. npj Viruses 4, 7 (2026). https://doi.org/10.1038/s44298-026-00174-9
关键词: 产前病毒感染, 母体免疫激活, 胎盘炎症, 子代免疫力, 神经发育