Clear Sky Science · zh
呼吸道合胞病毒的可溶性G蛋白通过TLR2介导的NLRP3初始激活与焦亡促进病毒扩散
这类肺部病毒为何与每个人息息相关
呼吸道合胞病毒(RSV)通常被视为冬季婴幼儿的主要威胁,但它也会使许多年长者和免疫功能低下的人住院。即便有了新疫苗与保护性抗体,RSV仍会反复感染人群并能造成严重的肺损伤。本研究关注一种鲜为人知的病毒蛋白——RSV G蛋白的可溶性形式,揭示了它如何悄然使肺细胞为剧烈炎症做好准备,并帮助病毒更有效地在气道中传播。
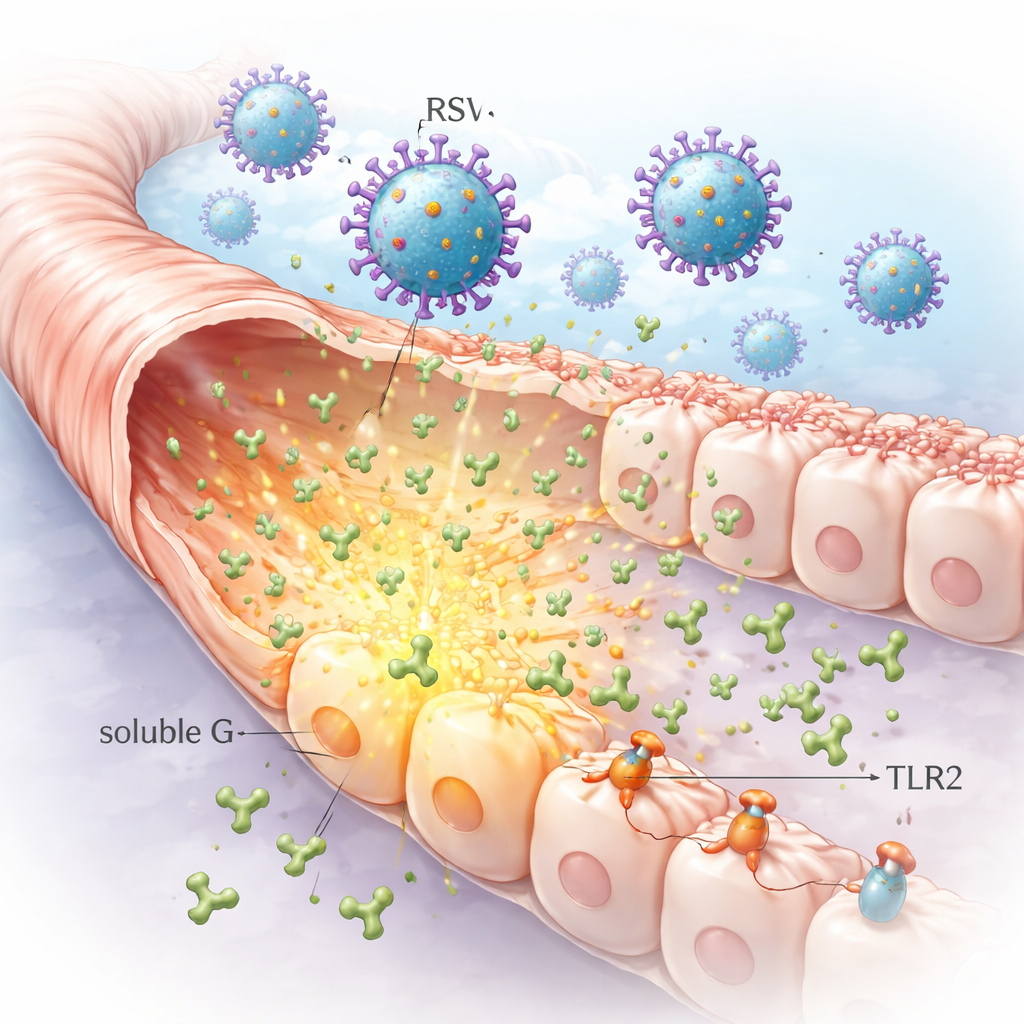
一种在感染前就分泌并扩散的病毒蛋白
RSV表面携带一种称为G的附着蛋白,帮助它附着到气道细胞。不同寻常的是,受感染的细胞还会大量释放这种蛋白的游离版本,即可溶性G。研究者展示了体外受感染的肺细胞可以将非常高水平的可溶性G释放到周围环境中。由于这种形式能够从原发感染部位扩散开来,它可以到达尚未被感染的邻近细胞,从而比病毒本身引起的变化更广泛地影响肺上皮。
可溶性G作为同时作用于细胞表面的双重钥匙
通过显微镜观察、生化牵拉实验和酶处理,研究团队描绘了可溶性G与细胞结合的方式。他们发现它可以附着在一种称为糖胺聚糖的多糖链上,也可以结合已知的RSV受体CX3CR1。关键的是,可溶性G还可与免疫细胞和气道细胞表面的模式识别分子TLR2结合。G蛋白中的一个微小基序CX3C对与CX3CR1的强结合以及对TLR2的有效招募至关重要。这意味着可溶性G可以先在细胞表面被松散捕获,然后再与控制细胞应答的更特异性受体互动。
为炎性细胞死亡对肺细胞进行初始激活
可溶性G与TLR2的结合并非无害。在带有报告系统的免疫细胞与人肺细胞系中,可溶性G激活了TLR2下游的MyD88–NF-κB信号通路,导致促炎信号分子如IL-6和IL-8的释放。同时,它还提高了被称为NLRP3炎症小体的分子“警报系统”组分以及产生一氧化氮和氧自由基等反应性分子的酶的产量。单独这些改变只引起轻微损伤,但当已被初始激活的细胞随后被RSV感染时,第二次打击触发了完整的炎症小体组装、半胱天冬酶‑1(caspase‑1)的激活、细胞膜孔洞形成,以及一种被称为焦亡的剧烈炎性细胞死亡形式。该过程在细胞上打出孔洞,释放炎性内容物,并伴随培养液中传染性病毒数量的增加。
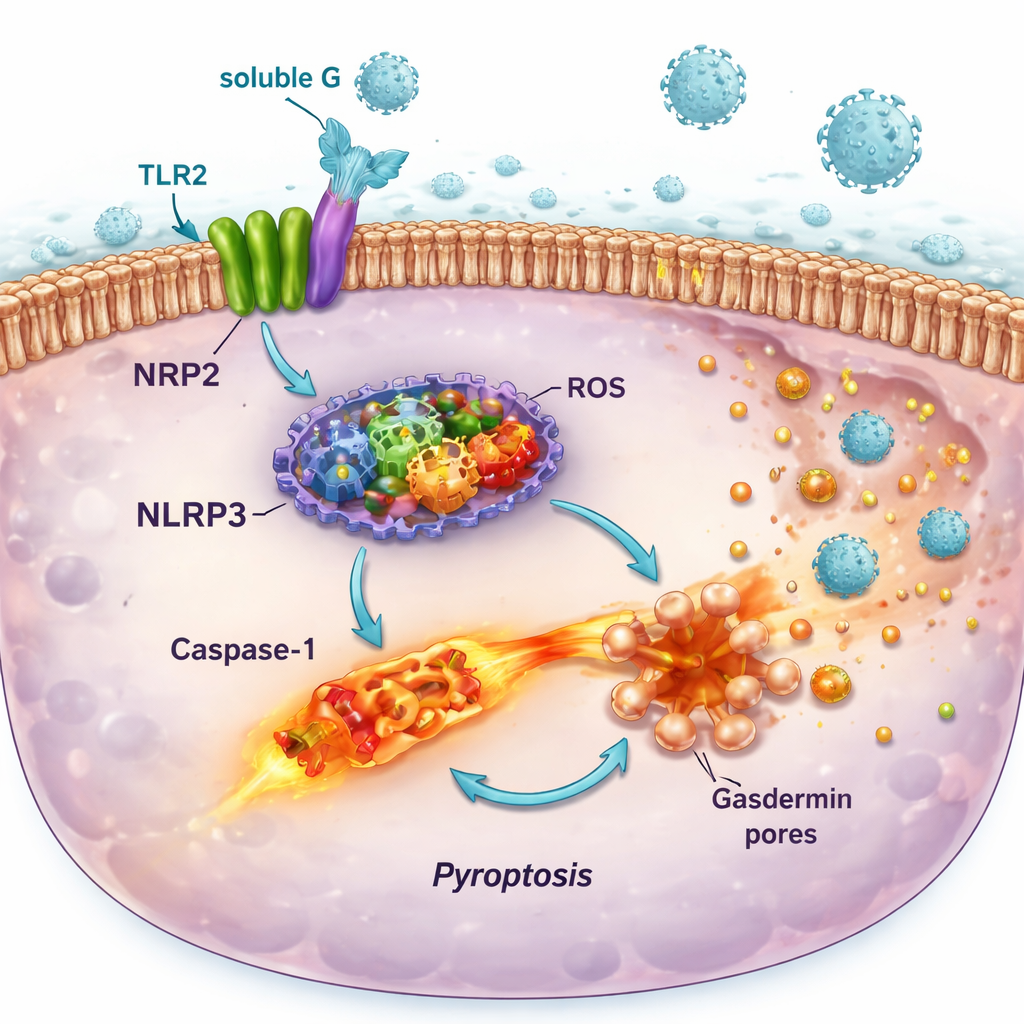
这一连锁反应如何可能加重肺病
可溶性G的促死亡作用在气道上皮细胞中最为明显——这正是RSV偏好感染的细胞类型——且依赖于NLRP3炎症小体,因为特异性NLRP3抑制剂在很大程度上能恢复细胞存活率。相反,某些富含TLR2但缺乏CX3CR1受体的免疫细胞在相同条件下并未发生强烈的溶裂性死亡。这种模式表明,RSV利用可溶性G选择性地削弱并破坏气道的保护性上皮层,同时保留部分仍能持续产生信号的免疫细胞。结果是肺内更多的炎症、更多的细胞碎片,以及更多让新病毒颗粒逸出并感染邻近细胞的机会。
这对未来治疗意味着什么
对非专业读者来说,关键的信息是RSV并不只依赖病毒直接侵入造成的损伤。通过释放大量可溶性G蛋白,它可以通过TLR2“软化”邻近细胞,使它们更容易以炎性方式死亡并释放病毒。本研究识别了该链条中的几个潜在药物靶点——可溶性G本身、其CX3C基序、TLR2以及NLRP3炎症小体。原则上,阻断可溶性G与TLR2相互作用的疗法,或抑制NLRP3活性的手段,可能同时减少肺损伤与病毒传播。这类策略将来或可作为现有RSV疫苗和抗体的补充,为最年幼和最易受影响的患者提供更好的保护。
引用: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
关键词: 呼吸道合胞病毒, 可溶性G蛋白, TLR2 炎症小体, 焦亡, 肺部炎症