Clear Sky Science · zh
围绝经期激素治疗与神经精神疾病风险:一种药物靶点孟德尔随机化研究
为什么这项研究很重要
许多女性想知道,在绝经期前后服用激素是否会保护大脑,或会增加记忆力下降、抑郁或焦虑等问题的风险。医生对此也意见不一,因为既往研究给出了相互矛盾的结论。本文采用一种基于遗传学的方法,类似于长期随机对照试验的思路,提出一个简单问题:当大脑中的雌激素受体以围绝经期激素治疗(MHT)可能产生的方式被轻微调整时,这会改变阿尔茨海默病或常见心理健康问题的风险吗?
围绕激素与大脑的难题
女性比男性更容易出现抑郁、焦虑和阿尔茨海默病。一种主要观点认为,雌激素——一种重要的女性性激素——在生命过程中塑造大脑并可能起到保护作用,直到中年时其水平波动或下降。在绝经过渡期,许多女性使用围绝经期激素治疗来缓解潮热和睡眠问题等症状。然而关于MHT究竟有益还是有害于大脑健康的研究结论不一:有的发现痴呆风险升高,有的提示有保护作用,许多研究则未显示明确效果。这些不一致可能源于试验持续时间短、药物配方不同,以及症状更严重的女性更容易被处方激素等因素。
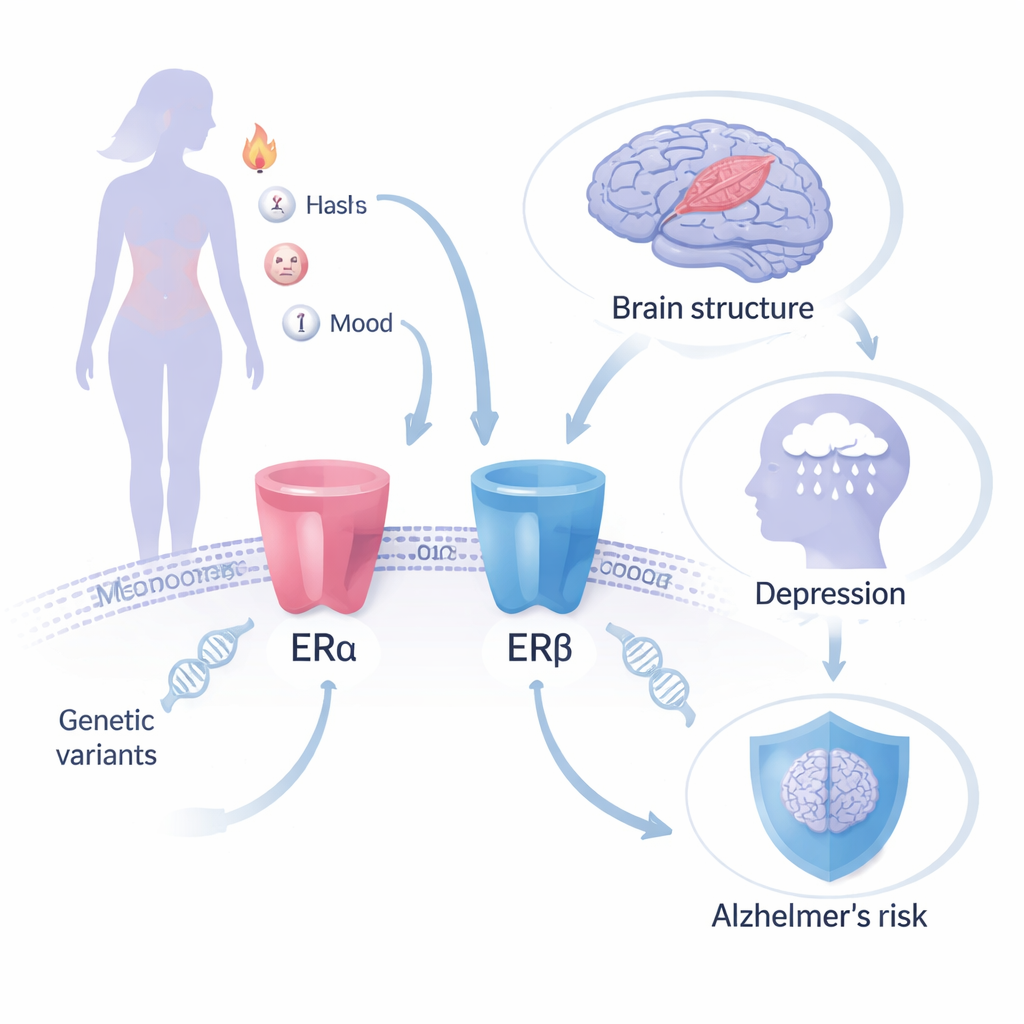
将基因作为自然实验
研究者没有跟踪服用激素药物的女性,而是采用孟德尔随机化方法,将自然存在的遗传差异作为长期、随机分配“处理”的替代。他们聚焦于两种被围绝经期激素治疗旨在激活的体内蛋白——雌激素受体 ERα 与 ERβ。编码这些受体的基因(ESR1 和 ESR2)中的特定遗传变异已知会影响在雌激素作用下发生变化的“下游”性状,例如骨密度、携带性激素的血浆蛋白(性激素结合球蛋白)以及血红蛋白水平。通过追踪这些与受体相关的变异如何与大型基因组关联研究中关于阿尔茨海默病、大脑结构、抑郁和焦虑的结果相联系,团队可以估算调整每种受体活性可能对长期大脑和精神健康风险产生的影响。
遗传证据显示了什么
作者构建了三种遗传工具:两种反映 ERα 活性的工具(分别通过与骨密度相关的变异和与性激素结合球蛋白相关的变异)和一种反映 ERβ 活性的工具(通过与血红蛋白相关的变异)。然后,他们将这些工具与一些可获得的最大规模全基因组关联研究(GWAS)结果相结合,涵盖阿尔茨海默病、大脑 MRI 指标(总体灰质、海马体积和与衰老相关的白质“斑点”)、抑郁和焦虑。总体而言,他们未发现令人信服的证据表明以遗传方式模拟的任一雌激素受体变化会显著改变阿尔茨海默病风险或影响这些大脑结构测量。对灰质或海马体积的少数弱信号在统计校正后并未通过,提示这些发现可能来自偶然而非真实的生物学效应。
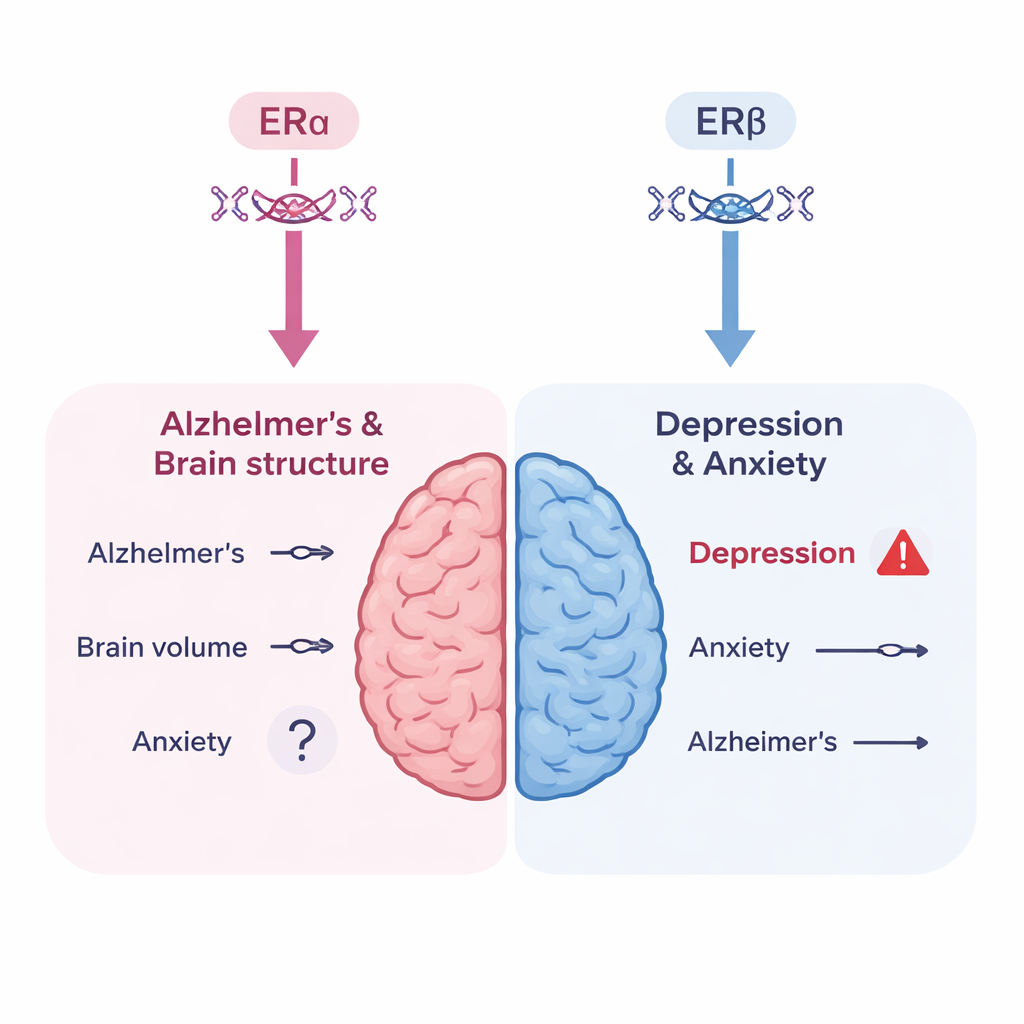
抑郁风险的一个警示信号
关于情绪的结果则有所不同。当研究者查看由血红蛋白为基础的遗传代理反映的 ERβ 活性时,观察到与抑郁风险升高之间存在统计学上稳健的关联。该发现与已知 ERβ 在大脑中特别活跃的区域一致——如参与情绪调节的海马和丘脑等。不过,作者也提醒血红蛋白这一代理并不完美:低血红蛋白本身可能导致疲劳和情绪低落,从而使结论变得模糊。他们未发现有力的遗传证据表明单独的 ERα 活性会增加抑郁风险,只有一个提示性的、非决定性的迹象指向 ERα 可能与焦虑有关。重要的是,自出生起持续发挥作用的遗传效应并不等同于在中年开始使用激素治疗,因此这些结果不应被直接解读为对任何特定 MHT 方案的直接预测。
这对女性及其医生意味着什么
转化为日常决策,这项研究表明,以类似于 MHT 的方式靶向雌激素受体并未明确增加或减少终生的阿尔茨海默病风险,也未在大脑结构上引起重大变化,至少在欧洲血统人群中是如此。与此同时,指向 ERβ 与抑郁之间关联的结果强调了对激素敏感的大脑回路与情绪的联系,以及不同雌激素受体可能带来不同的心理健康含义。这项工作不能替代临床试验,但它提供了一个强有力的遗传学“现实检验”,有助于改进未来的激素疗法并指导围绕为更安全、更个性化治疗绝经期女性的研究。
引用: Schindler, L.S., Gill, D., Oppenheimer, H. et al. Menopausal hormone therapy and risk of neuropsychiatric disease: a drug target Mendelian randomisation study. npj Womens Health 4, 10 (2026). https://doi.org/10.1038/s44294-026-00130-1
关键词: 围绝经期激素治疗, 雌激素受体, 阿尔茨海默病, 抑郁风险, 孟德尔随机化