Clear Sky Science · zh
重新思考子宫内膜异位症复发:从临床挑战到生物学机遇
为何这与日常生活相关
子宫内膜异位症影响全球数百万人的生活,常引起剧烈疼痛、乏力和生育问题。手术可带来显著缓解,但对许多人来说,症状或病灶会再次出现。本文综述探讨为何子宫内膜异位症在手术后如此常复发,以及这种“复发”如何实际上揭示疾病的生物学线索——并为开发更个性化、更持久的治疗提供机会。
“复发”可能意味着不同的情况
临床医生和研究者尚未就子宫内膜异位症复发达成统一定义。有时复发指缓解一段时间后疼痛再次出现;有时则指影像或再次手术中发现新的或增大的病灶。这两种情形常重叠,但并非总是如此。有些人在未见明确病灶的情况下仍有剧烈疼痛,而另一些人虽有病灶再生却感觉良好。疼痛可能源自神经系统的改变、瘢痕形成或其他盆腔疾病,而不仅仅取决于病灶的大小或数量。这种不一致使得研究间难以比较,也让医生难以向患者清晰说明手术能达到和不能达到的预期。
医生目前如何追踪并尝试预防复发
由于再次手术具有侵入性并可能损伤卵巢,大多数随访依赖超声或MRI,这些影像学方法能较好地发现较大的卵巢囊肿,但可能漏检其他部位的小病灶或隐匿病灶。目前尚无简单的血液检测能可靠地随时间追踪子宫内膜异位症的活动性。研究者已开始使用临床因素(如年龄、手术时病变范围和粘连存在情况)以及实验性的组织和血液标志物构建预测工具。更年轻的年龄、病情更严重、大囊肿和术前疼痛强烈倾向于增加复发风险,而妊娠和长期激素抑制则倾向于降低风险。然而目前的预测模型能力有限,需要在更大、更具多样性的患者群体中验证。
激素有帮助,但很少能治愈
术后长期激素治疗——例如连续服用避孕药或使用子宫内激素释放装置——可将病灶和疼痛复发的风险降低大约三分之一到三分之二。这些药物主要通过维持较低的雌激素水平并抑制月经周期来发挥作用,从而“饿死”异位组织并减轻炎症。然而,一旦停药,这种保护作用很快消退,且副作用、个人偏好或想要怀孕的意愿常限制了使用时长。有些患者在生物学上对某些激素(尤其是孕激素)似乎“耐受”,或其疼痛主要由神经与大脑的改变驱动,而激素并不能完全解决这些问题。因此,许多人仍面临症状反复、治疗与复发的循环。
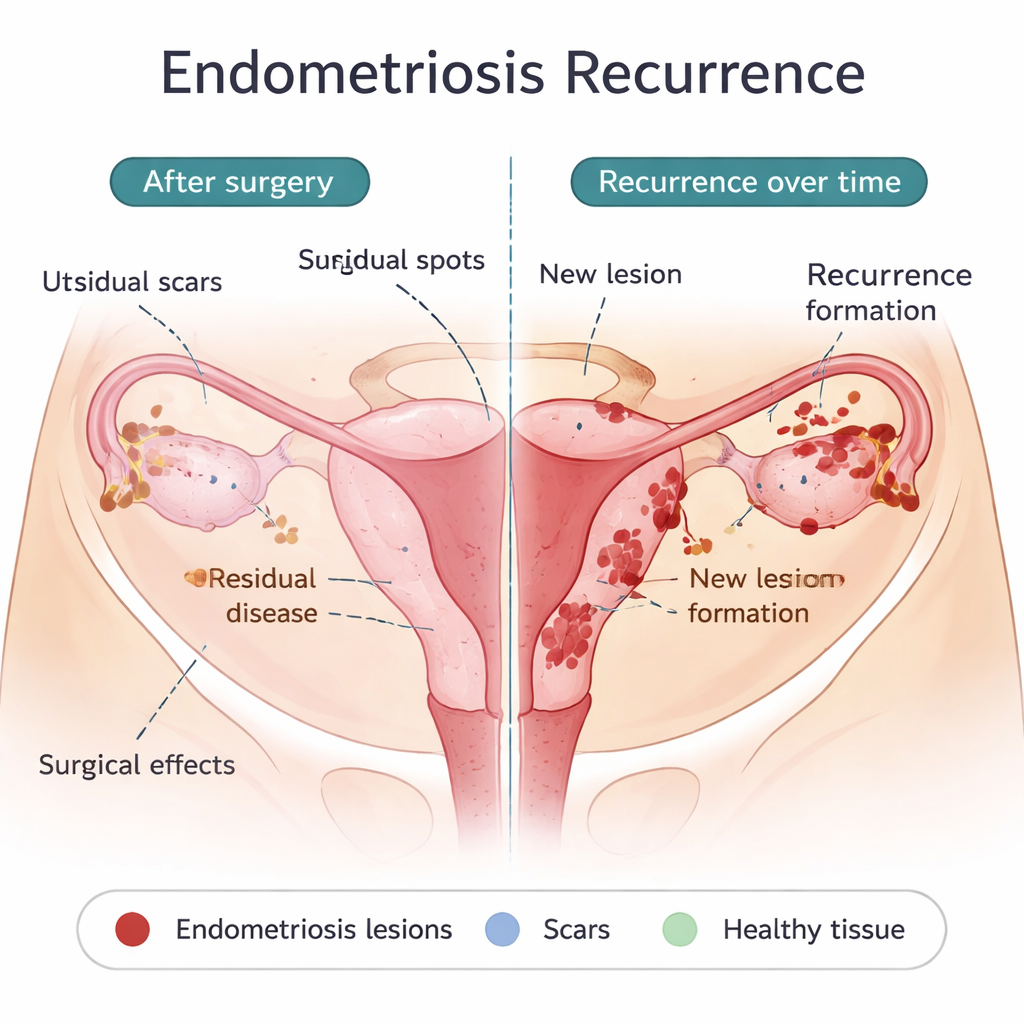
手术可能留下的残余——以及真正新生的病灶
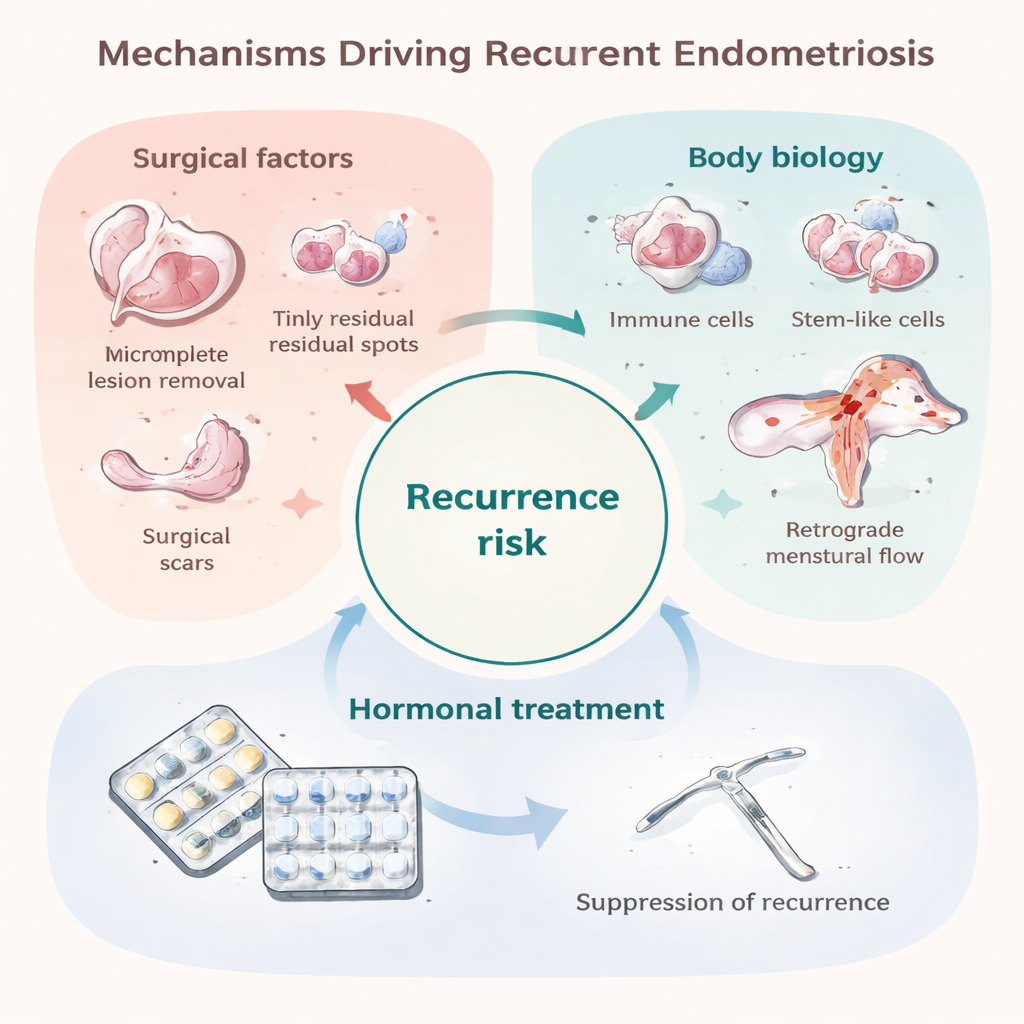
早期复发的一个主要原因是极少量残留病变:首次手术未能或无法切除的小植入物。这些植入物肉眼难见,但在术后激素保护消退后可能再次生长。某些手术选择,例如对卵巢囊肿采取更保守的处理,与更高的复发率相关,而更激进的切除可降低复发,但自身也带来风险。手术本身也可能在腹腔内播散子宫内膜细胞,或形成提供“肥沃土壤”的瘢痕,促使新病灶形成。同时,一些复发出现在数年之后或新部位,这表明至少在部分患者中,确实可能是新病灶形成而不仅仅是旧病灶再生。与最初导致子宫内膜异位症的过程相同——月经血倒流入盆腔、免疫系统未能清除游离细胞、易于植入的类干细胞以及一个容忍且血管丰富的环境——也可能推动这些晚期复发。
将挫折转化为生物学线索
作者认为,与其仅将复发视为手术失败,不如把它当作理解子宫内膜异位症的关键。那些在看似彻底手术后仍然复发的人,可能具有独特的免疫、遗传或组织特征,使其身体对子宫内膜细胞格外“友好”。对这些个体进行长期研究——采用标准化的症状、影像学发现和实验室标志物测量方式——可能揭示对病灶存活与再生真正重要的生物通路。这些知识可推动更好的风险评分、更明智的激素使用与疗程选择,乃至开发针对疾病根源而非仅仅抑制症状的新疗法。如此,令人沮丧的复发现象反而可能成为改善长期个体化治疗的重要契机,从而提升子宫内膜异位症患者的长期护理质量。
引用: Masferrer-Ferragutcasas, C., Delgado-Gil, R. & Colas, E. Rethinking endometriosis recurrence: from clinical challenge to biological opportunity. npj Womens Health 4, 4 (2026). https://doi.org/10.1038/s44294-026-00128-9
关键词: 子宫内膜异位症复发, 术后激素治疗, 盆腔疼痛, 个体化妇科, 女性生殖健康