Clear Sky Science · zh
用于识别同源重组修复缺陷性乳腺癌或卵巢癌易感基因的全面基因组框架
为什么有些家族面临更高的癌症风险
许多患有乳腺癌或卵巢癌的女性有明显的家族病史,但遗传检测常常找不到明确原因。这一差距有时被称为“缺失的遗传力”,使家庭无法获得答案,并可能限制获得个性化筛查或靶向药物等治疗的机会。本研究旨在建立一种更强大的方法,通过将多种基因组和临床信息结合起来,而不是单独查看每一种信息,从而在DNA中寻找隐藏的癌症易感基因。 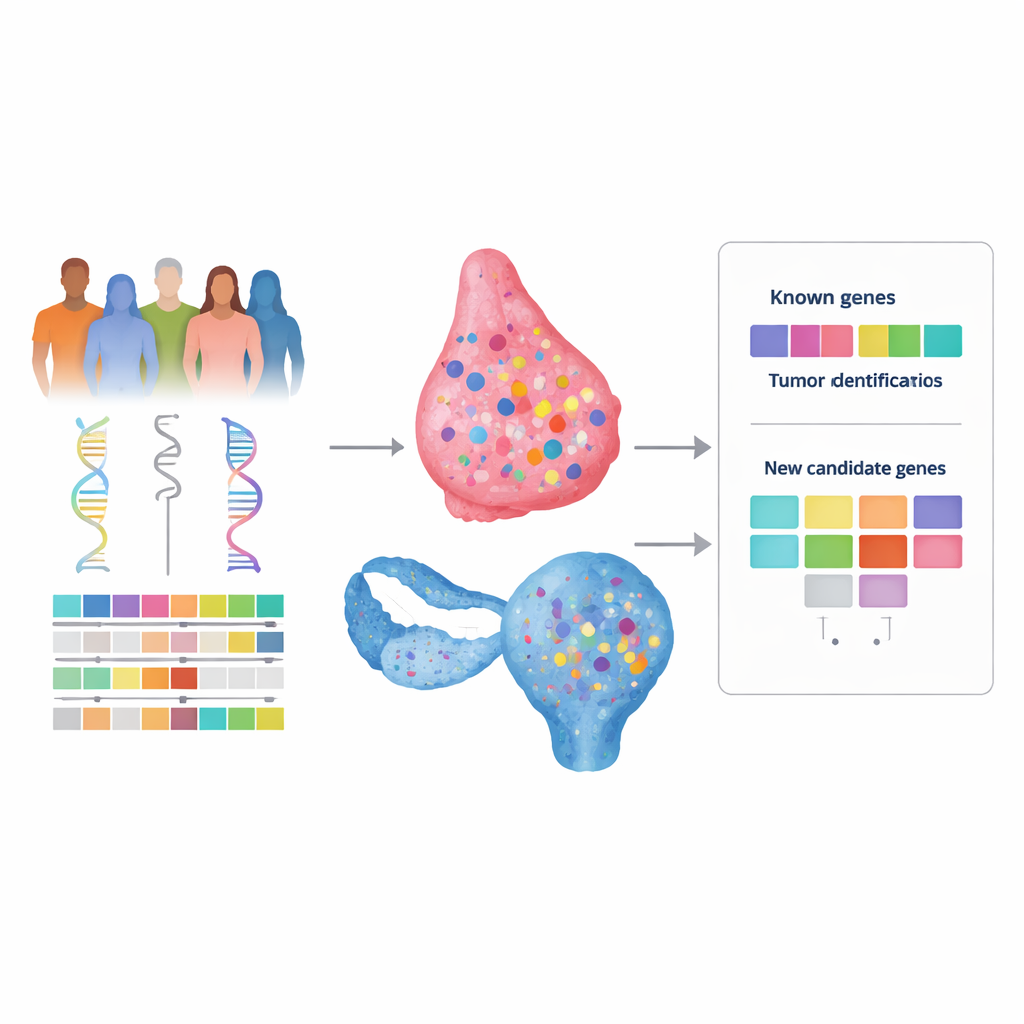
寻找损伤 DNA 修复的指纹
研究者将注意力集中在一种特定的DNA损伤修复机制——同源重组修复上,这一机制通常负责修复基因组中的危险断裂。当该修复系统失效时,细胞会积累一种明显的“突变特征”——肿瘤DNA中一组特征性改变,类似分子指纹。这种模式在某些难治的乳腺癌和卵巢癌中尤为常见。研究团队推测,如果肿瘤显示这种指纹,说明该肿瘤很可能失去了某个DNA修复基因的两个功能拷贝(无论该基因是否已知),而这种情况可能源于该基因的遗传变异。
构建结合遗传与临床的框架
为检验这一想法,作者分析了来自癌症基因组图谱(The Cancer Genome Atlas)中数百名乳腺癌和卵巢癌患者的DNA数据,该数据库同时提供血液(遗传)和肿瘤(获得性)基因组信息及临床资料。他们在全外显子区——蛋白编码的基因部分——中搜索罕见的、看起来有害的遗传变异,并寻找在肿瘤中出现的“第二次打击”事件,例如剩余健康拷贝的丢失。对于每个基因,他们随后询问此类两次打击事件是否在带有修复缺陷特征的肿瘤中比在没有该特征的肿瘤中更常见。关键在于,他们并未局限于预设基因面板,从而允许意想不到的候选基因浮现。
验证方法有效性并发现新嫌疑基因
作为现实检验,该框架正确地将广为人知的乳腺癌和卵巢癌基因BRCA1和BRCA2标示为与两种癌症中的修复缺陷特征强相关,确认了该方法的可行性。在乳腺癌中,它还标出了一个额外基因THBS4,并且提示KIF13B和TESPA1等基因可能参与。然而,逐例的详细审查显示,THBS4的变异常与其他更确立的修复相关事件同时出现,使其作为驱动基因的证据不那么令人信服。 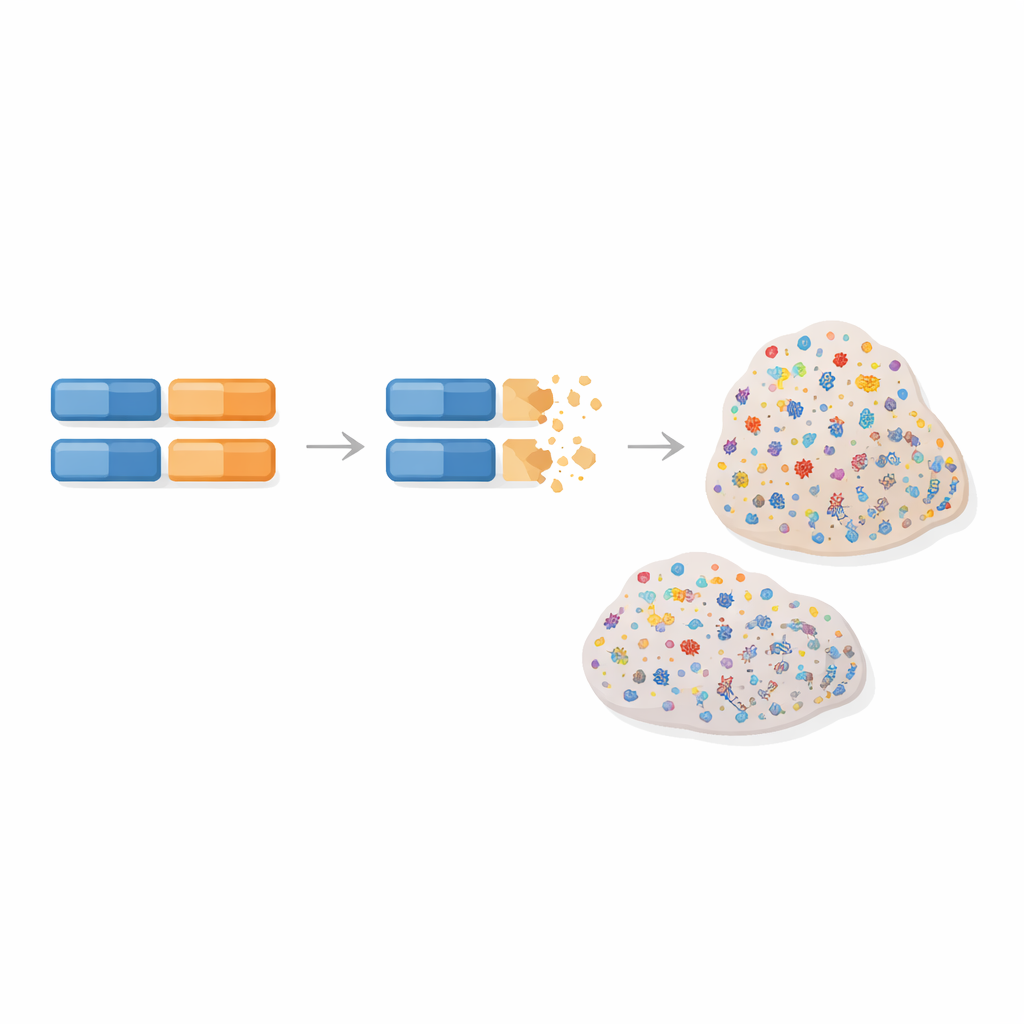
聚焦无法解释的高风险肿瘤
为了超越统计学分析,研究者加入了临床细节,如肿瘤亚型、确诊年龄和祖源信息。他们聚焦于那些肿瘤明确显示修复缺陷特征且属于已与该生物学相关的临床群体——基底样乳腺癌和高分级浆液性卵巢癌——但缺乏已知的BRCA型事件的患者。在这些患者中,他们再次寻找伴有第二次打击的遗传变异,这一次在一个广泛而经策划的癌症和DNA修复基因列表内。这个“临床-组学”视角将若干参与DNA双链断裂修复及密切相关的Fanconi贫血通路的基因,例如RAD51B、RAD54B、RAD54L、FANCD2等,突出为有可能的新遗传风险贡献者。
对患者和未来研究的意义
该研究并不声称已确凿证实新的癌症易感基因;每个候选基因影响的患者数量仍然很少,需要更大且更多样化的队列来确认它们的作用。相反,作者提供了一个可复用的蓝图:一种将遗传和肿瘤DNA、特征性突变指纹以及临床特征结合起来,系统性地优先排序可能解释无法解释家族性癌症的基因的方法。随着将该框架应用于更大数据集和其他癌症类型,可能逐步缩小“缺失的遗传力”差距,优化遗传检测面板,并帮助更多患者了解其个人风险以及预防和靶向治疗的选择。
引用: Camacho-Valenzuela, J., Matis, T., Roca, C. et al. A comprehensive genomic framework for identifying genes predisposing to homologous recombination repair-deficient breast or ovarian cancer. BJC Rep 4, 15 (2026). https://doi.org/10.1038/s44276-026-00218-w
关键词: 同源重组缺陷, 乳腺癌遗传学, 卵巢癌, DNA 修复基因, 癌症易感性