Clear Sky Science · zh
STAR(肿瘤-基质 AI 风险)评估:AI 导出肿瘤-基质比例与患者生存率相关,并在上皮性卵巢癌中提供超越 KELIM 的预后附加价值
为什么肿瘤周围的“邻里”很重要
当我们想到癌症时,通常会想象一团失控的细胞。但肿瘤并非孤立存在,它生活在由支持组织、血管和免疫细胞组成的繁忙邻里——基质中。本研究提出了一个简单但有力的问题:我们能否利用人工智能在常规显微镜切片上测量肿瘤细胞与周围组织之间的平衡,来预测哪些卵巢癌患者在治疗开始前更可能有更好或更差的结局?
以新方式解读常规活检切片
上皮性卵巢癌患者通常在手术或活检时取下组织。这些样本在每家医院都会被染色并在显微镜下检查。研究人员关注一个称为肿瘤–基质比例(TSP)的特征:图像中由支持组织占据的面积与癌细胞相比的多少。在早期工作中,病理学家通过目测估计这一比例,发现富含基质的肿瘤往往更具侵袭性并且更容易耐受以铂类为基础的常规化疗。在本研究中,团队使用深度学习的 AI 系统在数字化切片上自动测量 TSP,旨在将一项人工且带有主观性的任务转化为一种快速且可重复的诊断读数,可在确诊时直接获得。
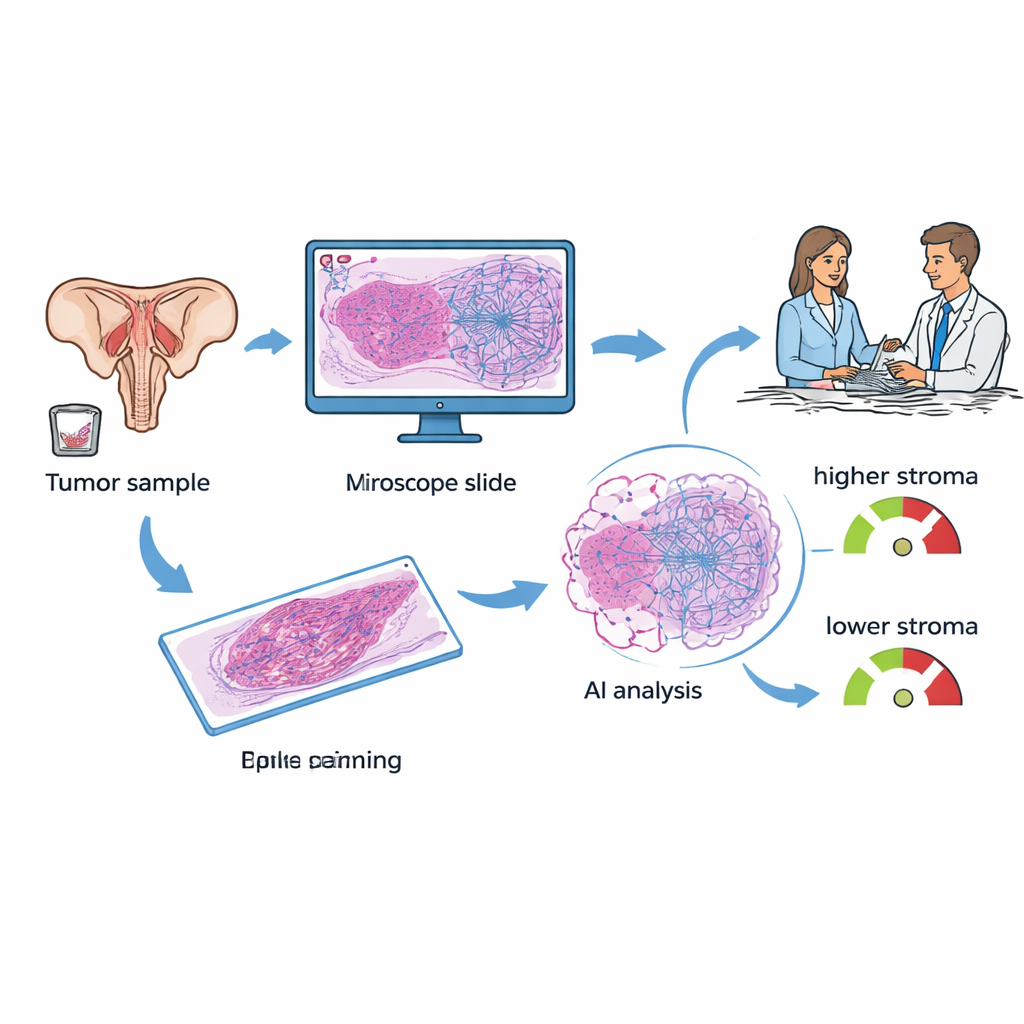
将 AI 组织分析与血液评分进行比较
目前,一个被广泛讨论的卵巢癌工具是 KELIM,这一评分基于化疗前 100 天内血液标志物 CA-125 下降的速度。KELIM 费用低且有用,但只能在数周治疗后计算,而且并非所有患者都有足够的早期血检来生成该评分。研究者汇集了来自单一癌症中心的 89 名患者的数据,这些患者既有组织切片又至少有三次 CA‑125 测量。他们为每位患者计算 KELIM,由病理学家在切片上标注肿瘤区域,然后让 AI 模型估算 TSP,并将每例分类为“低基质”(基质少于 50%)或“高基质”(基质 50% 及以上)。
AI 与专家匹配并标识高风险肿瘤
AI 的判定与经验丰富的病理学家高度一致:在 94% 的病例中,自动化的 TSP 分类与人工分类相符,这一吻合程度被认为是优秀的。当团队检视患者结局时,发现被 AI 判定为高基质的患者总体生存显著低于低基质患者。从统计学角度看,高 TSP 在随访期间几乎将死亡风险翻倍,即便在考虑 KELIM 评分后,这一效应仍然存在。相比之下,在这组现实世界的患者中,KELIM 与肿瘤是否对铂类药物耐药相关,但与患者生存时间并无明确关联。
这对治疗决策可能意味着什么
由于 TSP 可从确诊时的常规切片中测得,基于 AI 的 TSP 提供了一种在化疗开始前评估风险的方式,可能比 KELIM 提前数月得到结果。高 TSP 结果可能提示临床医生该肿瘤更具侵袭性且更难治疗,从而促使更密切的监测、更早考虑额外治疗或不同的手术策略。该方法成本相对较低:它依赖现有病理图像和软件模型,而非新增的实验室检测。作者认为,自动化 TSP 可与其他标志物(如基因检测和 CA‑125 趋势)共同使用,在不给患者或病理团队增加重大负担的情况下细化预后评估。
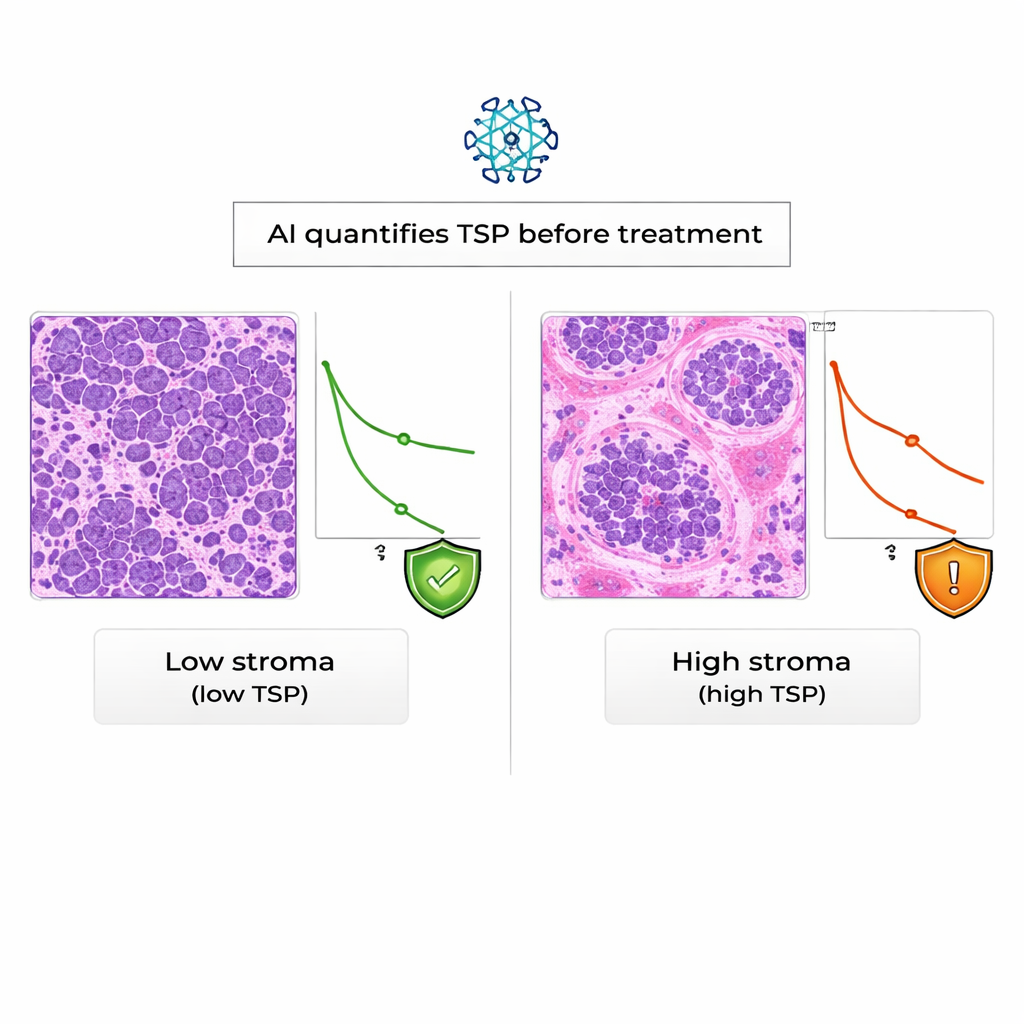
前瞻:为患者提供更智能、更早期的指引
对非专业读者而言,主要信息是并非所有卵巢癌都相同,肿瘤周围的支持组织携带着关于疾病行为的重要线索。本研究表明,AI 能在标准活检切片上可靠地读取这些线索,而且基质占比高的肿瘤通常与较差的生存率相关,这一关联独立于现有的血液评分。尽管在将该方法纳入常规临床之前仍需更大规模和更多样化的研究,AI 导出的 TSP 有望成为一种早期警示信号,帮助医生更有针对性地制定治疗方案,并在一开始就为患者提供更清晰的预期。
引用: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
关键词: 卵巢癌, 人工智能, 肿瘤微环境, 预后生物标志物, 数字病理