Clear Sky Science · zh
基因组调查揭示变形杆菌群体中一种多药耐药优势谱系的出现
为什么这种医院病原体与你有关
对许多人来说,泌尿道感染是偶发且疼痛的烦恼。但在医院和养老院中,某些感染由顽固的细菌引发,它们能附着在导尿管上、抵抗多种抗生素,并在人与动物之间悄然传播。本研究追踪了其中一种元凶——变形杆菌(Proteus mirabilis),利用其DNA作为旅行日记,揭示在过去一个世纪内一个难治家族谱系如何悄然崛起并占据主导地位。
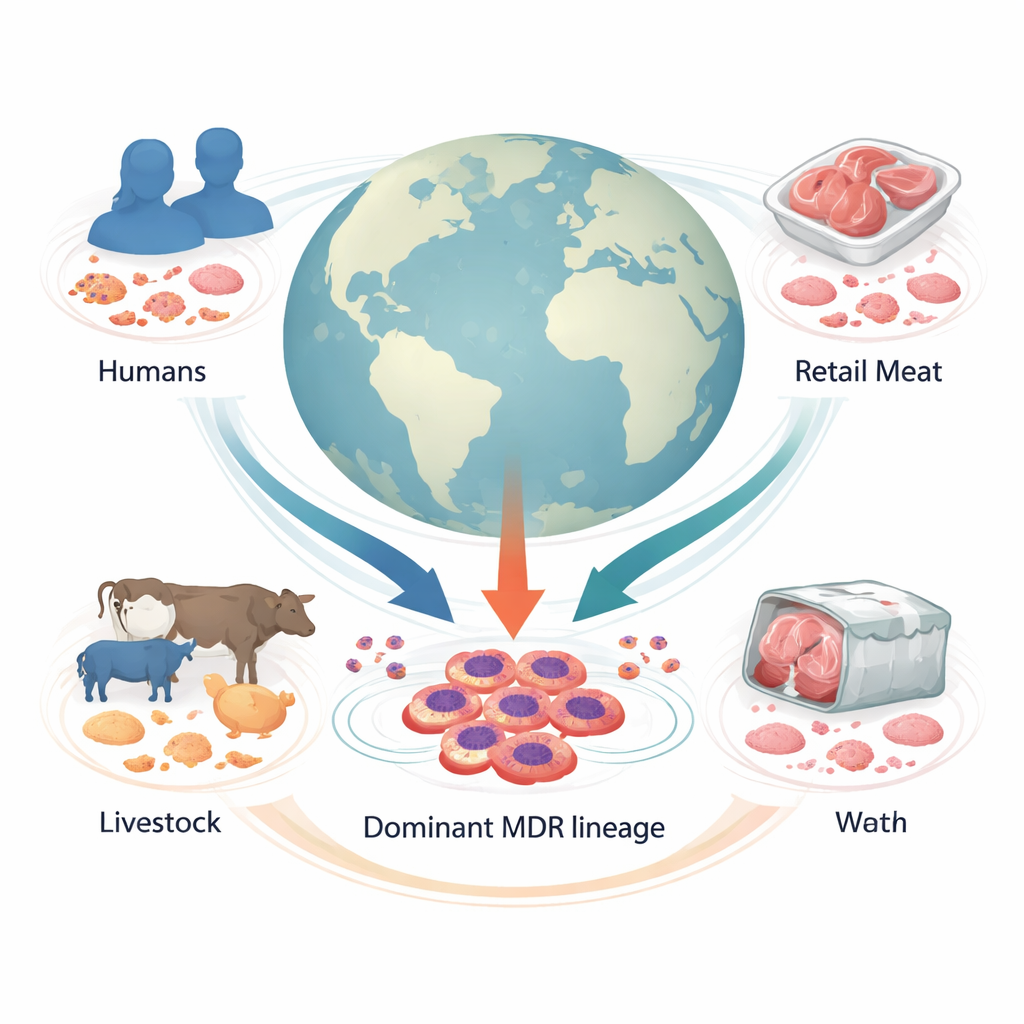
一次全球范围的隐蔽威胁调查
研究者汇集了来自34个国家的1,142个变形杆菌样本基因组,这些样本来自人类、畜禽、零售肉类和其他环境。通过比较全基因组,他们将细菌划分为178个遗传谱系。其中一个特别突出:“Cluster-1”,这是一个主要谱系,占所有样本的五分之一,包含来自多大洲医院的菌株。这些菌株大多来自人类,但也有相当一部分来自农场动物和肉类,表明该谱系跨物种并沿食物链流动。
一个配备许多药物防御的谱系
当团队在基因组中搜索抗生素耐药基因时,Cluster-1携带的耐药基因明显更多。平均每个成员携带近18个耐药基因,远高于其他谱系。这些基因包括可以破坏部分最强效抗生素(如通常作为最后手段使用的碳青霉烯类)的基因。许多耐药基因位于一个称为PmGRI1的大型DNA“岛”内,该岛可在细菌间转移。有些版本的该岛一次携带超过20个耐药基因,实际上将变形杆菌变成一个行走的药物库,使临床治疗选项大幅受限。
帮助细菌附着的粘着性特征
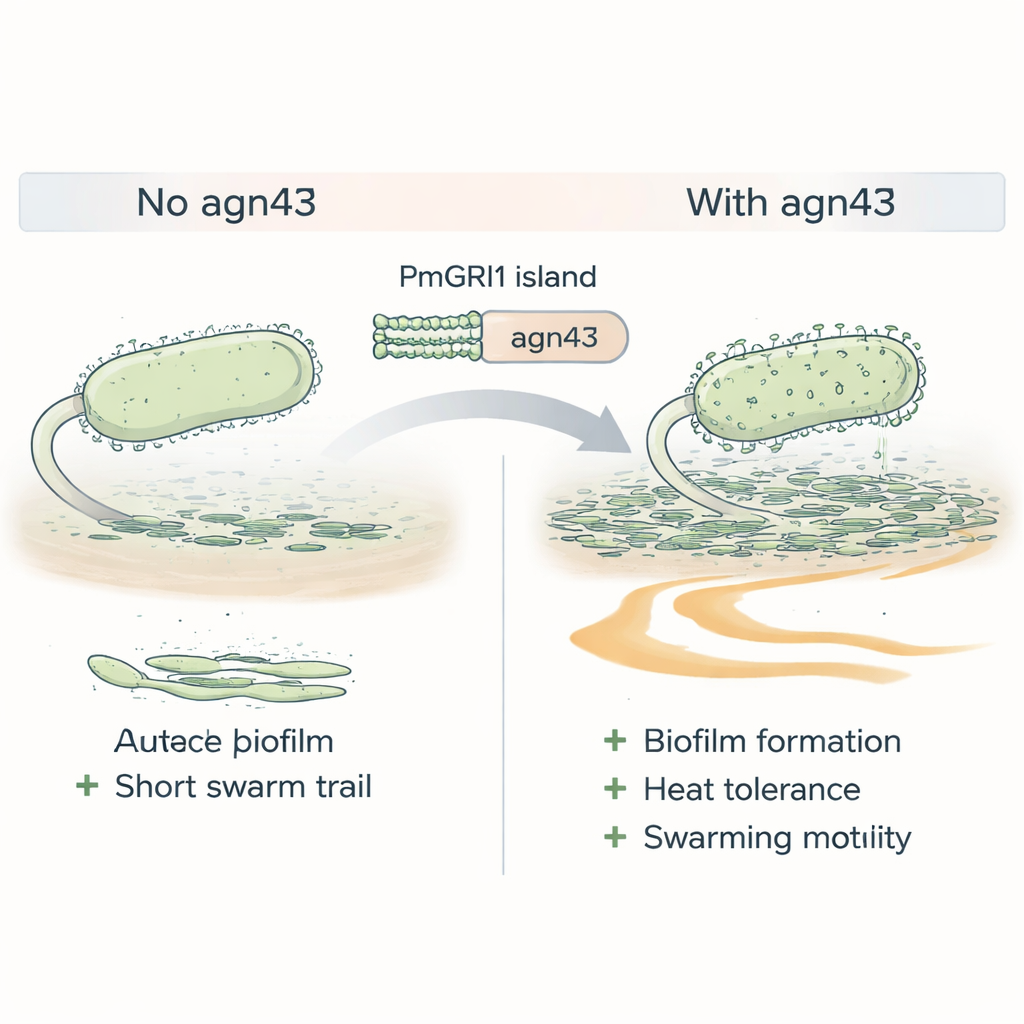
仅有耐药并不足以保证成功;细菌还必须善于在体内和医院环境中存活。Cluster-1菌株富含与附着细胞和形成生物膜相关的基因——生物膜是能保护细菌免受药物和免疫系统侵害的黏滑群落。PmGRI1岛上一个突出的基因,称为agn43,编码一种表面蛋白,类似分子魔术贴,帮助细胞聚集。当科学家在一个Cluster-1菌株中删除agn43时,突变体形成的生物膜较弱,对热胁迫的耐受性下降,且在表面蠕动的能力变差,这些性状通常有助于变形杆菌定植导尿管并在泌尿道内传播。
该超强谱系如何以及在哪里传播
通过将遗传差异与分离日期相结合,研究者重建了Cluster-1的时间线。他们估计其最近的共同祖先约在1910年出现,早于现代抗生素广泛使用的年代。该谱系随后分化为两个在临床上重要的分支:一个主要见于中国,携带一种能破坏碳青霉烯的基因blaKPC-2;另一个主要见于美国,携带相关的blaIMP-27基因。从20世纪80年代末开始,Cluster-1迅速扩张,并多次被检测到在国家间以及人类、畜禽和肉类之间流动,凸显其流行病学潜力。
对患者和公共卫生意味着什么
对非专业读者而言,结论是:某一变形杆菌家族通过结合两项优势演化为高度成功的医院病原体——一是厚重的抗生素耐药基因盔甲,二是额外的“粘附性”,有助于其形成保护性薄膜并在导尿管和组织上持久存在。这种组合使感染更难治疗且更易传播。研究强调需要在医院和农业中对该谱系进行密切的基因监测、加强导尿管相关的感染控制,以及谨慎使用抗生素,以遏制此类多药耐药株的上升和全球传播。
引用: Zhang, T., Wei, H., Ju, Z. et al. Genomic survey uncovers the emergence of a multidrug-resistant dominant lineage in Proteus mirabilis populations. npj Antimicrob Resist 4, 17 (2026). https://doi.org/10.1038/s44259-026-00189-5
关键词: 抗生素耐药性, 泌尿道感染, 医院感染, 细菌基因组学, 生物膜