Clear Sky Science · zh
对抗生素暴露的全球反应揭示核苷酸代谢在高水平β-内酰胺耐受性中的关键作用
为什么有些细菌能抵挡我们最好的抗生素
抗生素本应消灭有害细菌,但许多感染仍顽固地持续或在治疗后复发。本文探讨了一个常被忽视的原因:有些细菌可以暂时蛰伏,即使在非常高剂量的强效药物(如青霉素)下也能存活。通过揭示这些微生物如何重塑其内部化学以度过攻击,研究人员指出了可能恢复现有抗生素效力的新方法。
感染内部的一种隐秘生存策略
暴露于β-内酰胺类抗生素(例如青霉素)时,许多危险的革兰氏阴性细菌并非立即死亡。相反,它们可以脱掉坚固的细胞壁,变成脆弱的、圆形的体态,称为球形体(spheroplasts)。在这种形态下,它们停止增殖但仍然存活且代谢活跃。药物消失后,它们重建细胞壁,恢复正常的杆状形态,并可能重新引发感染。因为这种“耐受”是通向完全抗药性和治疗失败的垫脚石,理解球形体如何生存对未来医学至关重要。
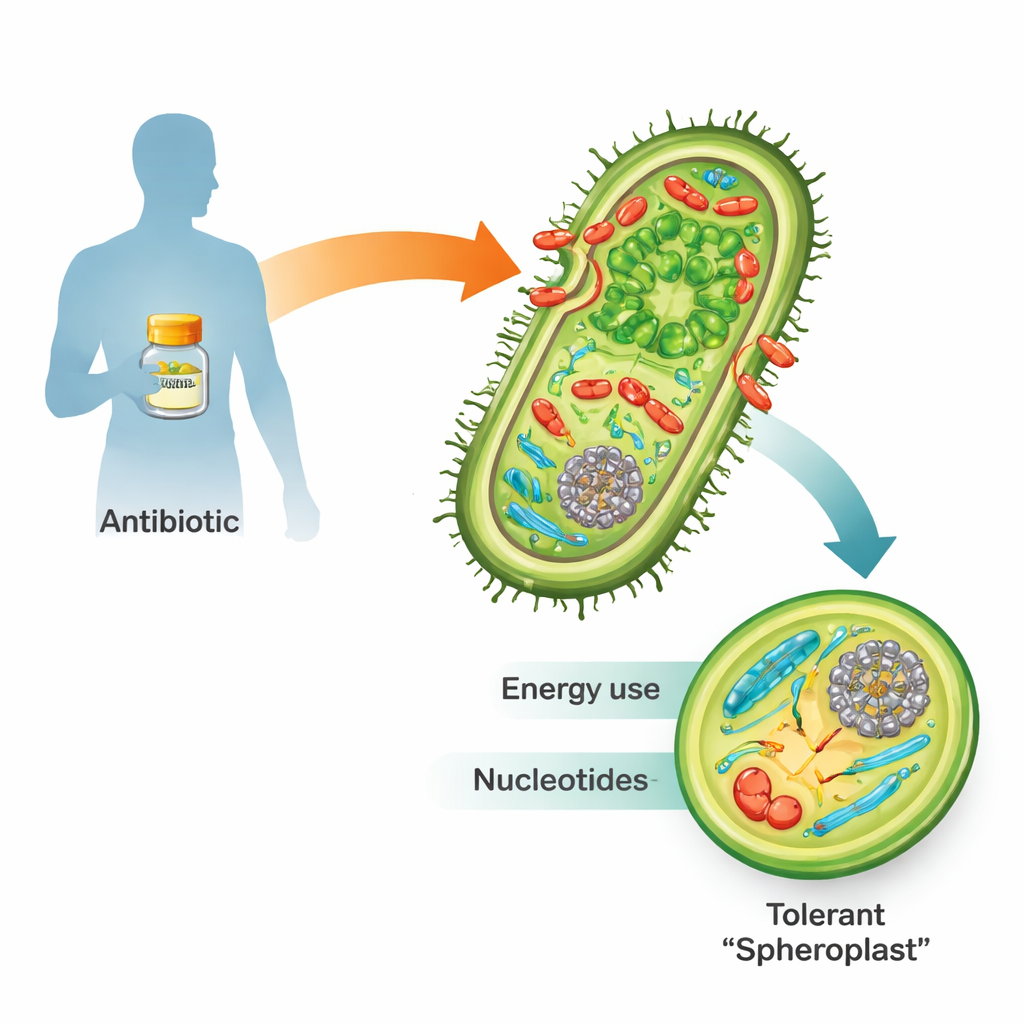
监听细胞的紧急广播
研究团队以霍乱弧菌(Vibrio cholerae)为模型,因为它对β-内酰胺类异常耐受且易于基因操作。他们用十倍最低致死量的青霉素处理细菌,并用两种强大的工具随时间跟踪反应。转录组学记录哪些基因被开启或关闭,而代谢组学测量数百种供给和构建细胞的小分子。两者结合,这些“多组学”技术绘制出耐受细胞在药物攻击期间如何随时间重构其内部运作的图谱。
代谢改道与一个隐藏的薄弱点
数据揭示了核心通路的广泛变化。合成细胞壁的基因强烈上调,与细胞试图修复损伤并为恢复做准备一致。热休克和应激响应系统也被启动,可能用于处理抗生素诱导应激下产生的错误折叠或氧化蛋白质。与此同时,中央碳代谢发生了变化:三羧酸循环(细胞的主要能量发生器)的某些步骤被增强,而糖酵解的关键中间体如葡萄糖-6-磷酸和果糖-6-磷酸被显著耗竭。这些中间体通常既供能又用于细胞壁合成,暗示持续且浪费的细胞壁物质“徒劳循环”正在消耗资源。
核苷酸承压
最显著的变化涉及核苷酸——DNA、RNA及许多能量载体的构件。许多核苷酸及其前体在青霉素处理的细胞中急剧下降,即使从头合成这些分子的基因被强烈激活。同时,参与“回收”核苷酸的基因被下调,仿佛细胞在努力保存那为数不多的存量。这些模式表明球形体处于严重的核苷酸压力之下。当研究人员有意干扰为核苷酸前体供给的通路(例如戊糖磷酸途径),或用另一种药物甲氧苄啶(trimethoprim)阻断核苷酸合成时,与β-内酰胺联合使用能够杀死的细菌远多于任一药物单用。这种强烈的协同效应不仅在霍乱弧菌中观察到,也出现在高度耐受的临床肺炎克雷伯氏菌(Klebsiella pneumoniae)和大肠埃希菌(Escherichia coli)菌株中。
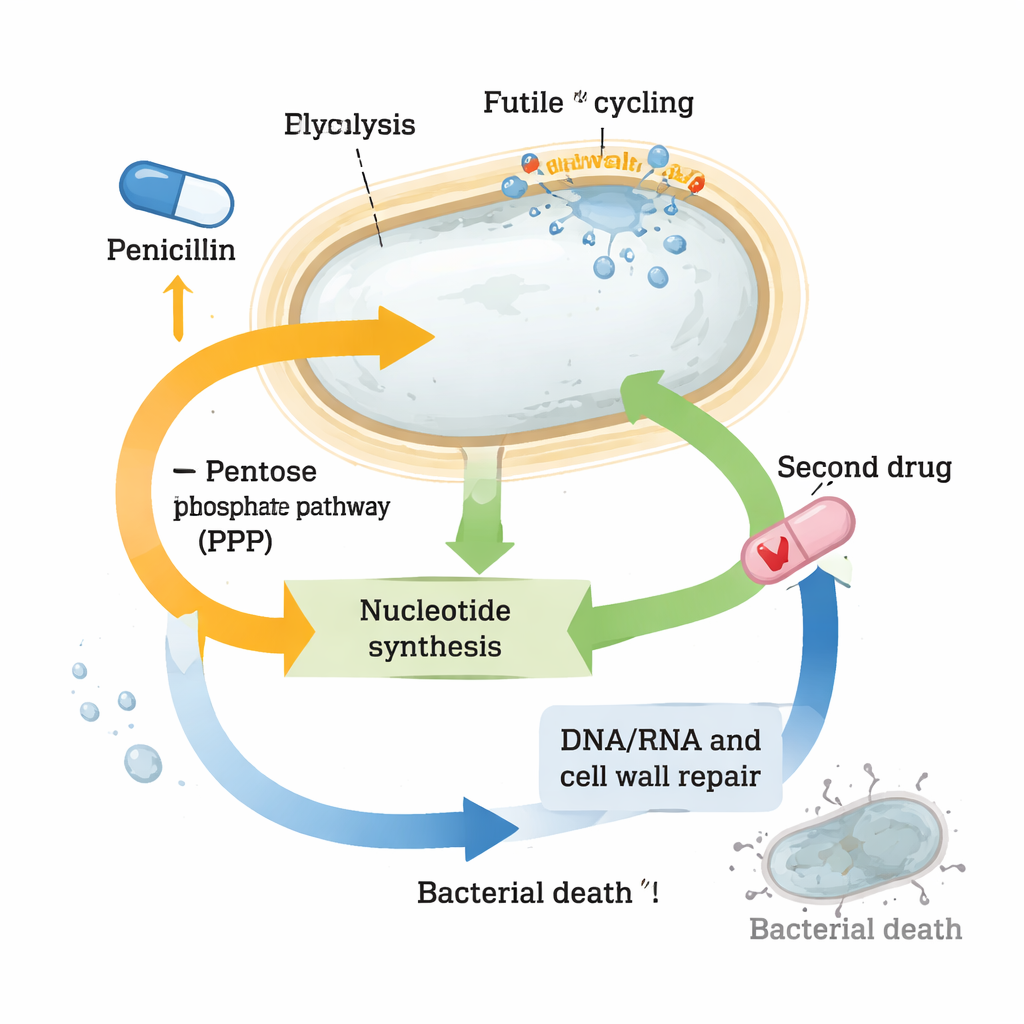
把生存化学转化为治疗优势
尽管代谢发生了重大重塑,耐受的球形体仍设法维持其能量货币ATP的相对稳定并避免灾难性损伤,这有助于它们在长时间抗生素暴露中存活。但研究表明,为此它们把核苷酸池压到了边缘。这种岌岌可危的平衡创造了一个弱点:用第二种药物将核苷酸代谢再稍微推一步,就会瓦解它们的防御并恢复强效杀灭。对非专业读者而言,结论是:一些细菌能在抗生素下存活,并非因为药物未击中靶点,而是细胞迅速重连其化学网络以承受打击。通过发现并利用这种生存网络中的薄弱环节——在此为核苷酸代谢——研究人员或可将旧有抗生素转变为强效的联合疗法,战胜即使是高度耐受的病原体。
引用: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
关键词: 抗生素耐受, β-内酰胺类抗生素, 核苷酸代谢, 细菌持久性, 药物组合