Clear Sky Science · zh
机器学习促进的实时声学俘获在时变多介质环境中迈向磁共振成像引导的微泡操控
用声音和影像引导微小药物载体
现代癌症治疗越来越依赖智能药物载体,能够将药物直接输送到肿瘤处,同时尽量保护健康组织。该研究探索了一种将此类载体在体内引导的未来方法:利用超声“陷阱”并由磁共振成像(MRI)引导。通过将声波、医学影像和机器学习结合,研究者旨在将微观药物载体的气泡停驻在随呼吸移动的肿瘤附近,即便身体在不断移动也能保持它们的位置。
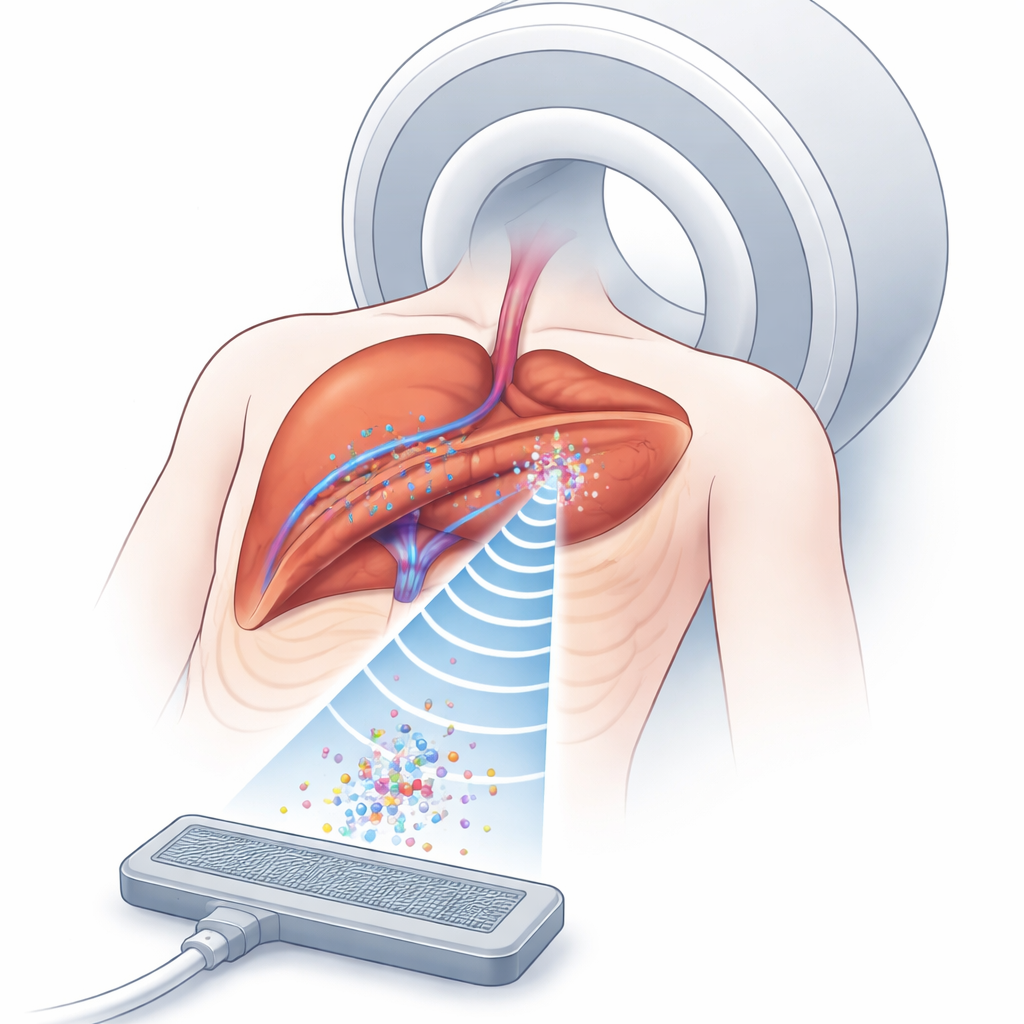
为什么俘获微小气泡很重要
载药微泡在血管中随流动传播,并可在受超声触发时释放药物。挑战在于如何在体内深处、精确部位长时间保持足够数量的这些气泡。超声可以在流体中形成无形的力腔——声学陷阱,在不接触物体的情况下将小颗粒悬浮。与此同时,MRI 能看到组织以及超声效应的分布,即使在器官内部也是如此。将这两种工具结合,可比单纯用药更精确地在肿瘤周围聚集药物载体。但在真实人体中,不同类型的组织——脂肪、肌肉、器官和随呼吸运动的肺——会弯曲并扭曲声波,导致在肿瘤精确位置形成并维持稳定陷阱变得非常困难。
移动且分层的体内环境问题
在空气或水等简单介质中,工程师已经知道如何使用相控阵列超声发射器推动、拉动和旋转微小物体。然而在体内,声波必须穿越具有不同密度和声速的多层介质,这些层之间的边界会引起折射和畸变。传统计算方法原则上可以通过计算从每个发射器到目标点的传播时间来校正这些效应。但这种方法将身体切分为数以百万计的小块并模拟波的传播——这是一个极其耗时的过程,而且仅在组织几乎静止时才有效。仅呼吸就能使腹部组织移动数毫米,很快就会让任何预先计算的解失效。
教模型预测声波路径
作者用基于学习的模型来解决这一瓶颈,该模型充当快速捷径:不必每次都模拟声波传播,而是训练一个神经网络来预测每个超声脉冲到达目标点所需的时间。他们首先构建了一个详尽的虚拟环境,使用一个充气腔室由薄塑料膜将气体与空气分隔,模拟声波通过不同组织层的传输。利用基于物理的仿真器,他们生成了大量目标点与一个14×14超声阵列之间的传播时间训练集。他们还让腔室在两个方向上移动以模拟运动,并通过跟踪三个可视标记来描述其位置,类似未来可被MRI看到的标记用于追踪患者呼吸运动。训练后的网络学会将期望的陷阱位置加上腔室位姿直接映射为196个发射器所需的时序模式,在大约26毫秒内达到微秒级精度。
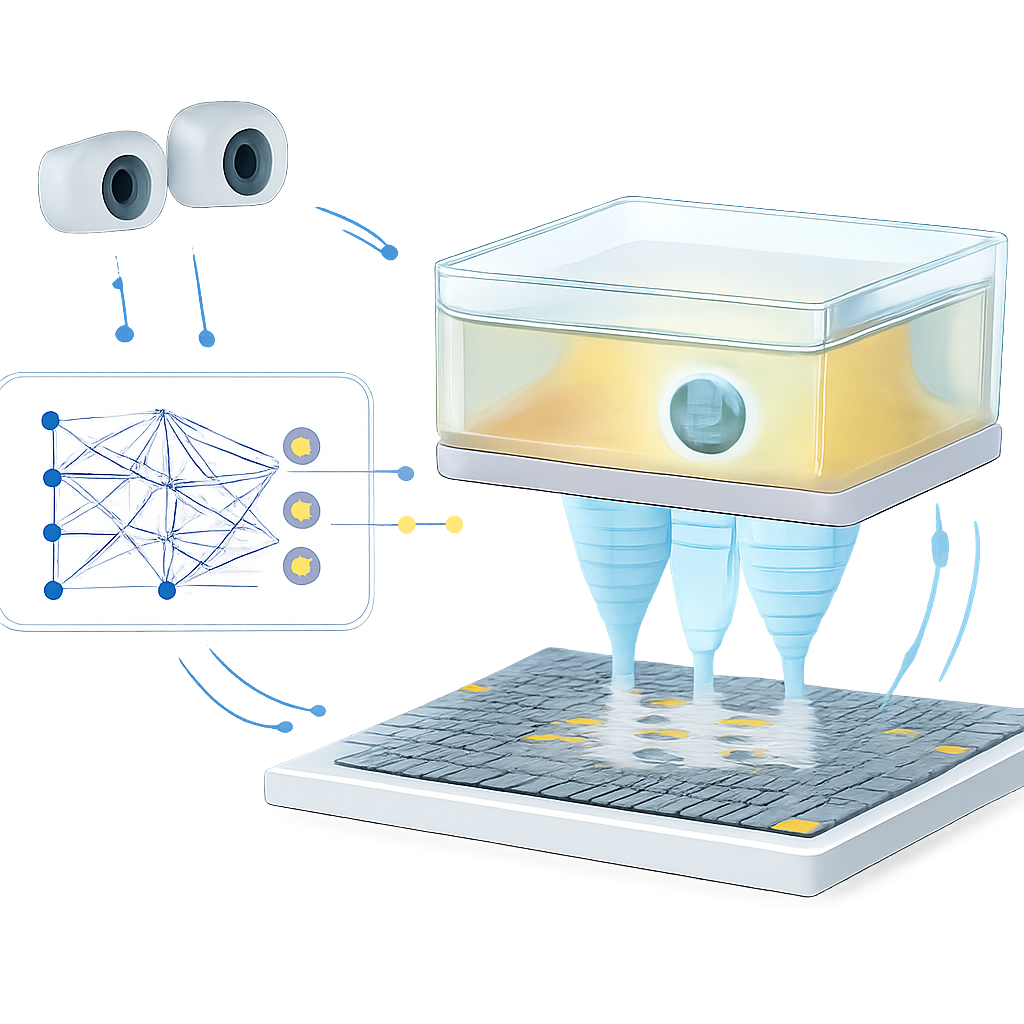
用视觉与快速更新闭环控制
速度本身还不够;当环境意外变化时,陷阱也必须随之调整。为证明这一点,团队构建了一个闭环控制系统。立体摄像机观察被声学陷阱在移动腔室内悬浮的小聚苯乙烯珠。当珠子偏离目标超过设定阈值时,系统会轻微调整目标位置,将更新后的坐标和腔室位姿输入学习模型,并快速刷新驱动阵列的相位模式。在实验中,系统能够每秒最多更新15次相位模式,将珠子沿H、K和U形路径引导,平均误差约为1毫米——相当于某些临床聚焦超声系统的定位精度。同样的反馈原理也缩短了腔室运动时珠子偏离目标的持续时间,表明控制回路可以补偿运动以及来自塑料膜和支撑结构的未建模效应。
这对未来治疗的意义
对非专业读者而言,核心信息是研究者构建了一种类似远程控制的非接触“牵引光束”,有朝一日可能将载药气泡停放在肿瘤附近并保持其位置,即便患者在呼吸。其机器学习模型用快速预测器替代了繁重的仿真,摄像机(以及未来的MRI标记)告诉系统身体如何移动,从而使陷阱能够实时重新调谐。尽管当前工作使用空气、气体和塑料而非真实组织,并悬浮的是塑料珠而非真实微泡,但它展示了在移动分层介质中实现实时控制的可能性。借助更强的硬件、更高的超声频率和基于MRI的运动跟踪,这一方法有望发展为一种用于MRI引导、机器人辅助超声疗法的临床工具,使深部药物递送更准确、更安全。
引用: Wu, M., Li, X. & Tang, T. Machine learning-facilitated real-time acoustic trapping in time-varying multi-medium environments toward magnetic resonance imaging-guided microbubble manipulation. Commun Eng 5, 52 (2026). https://doi.org/10.1038/s44172-026-00600-z
关键词: 声学俘获, MRI引导疗法, 微泡药物递送, 超声中的机器学习, 无创机器人操控