Clear Sky Science · zh
通过 Fbln2–Nupr1b 轴减弱心外膜激活和肌成纤维细胞丰度以刺激斑马鱼心脏再生
为何有些心脏能自我愈合
当人发生心肌梗死时,受损的肌肉通常被一块僵硬的瘢痕覆盖,永远无法真正恢复。斑马鱼——这种有条纹的小型观赏鱼——则表现出令人惊讶的能力:它们能重建心肌组织,并最终清除大部分瘢痕。本研究提出了一个看似简单但医学意义重大的问题:愈合中的心脏如何判断何时形成瘢痕、何时清除瘢痕以便新肌肉生长?通过解码斑马鱼中的这种平衡,研究指向了可能有朝一日帮助受损人类心脏自我修复而非衰竭的策略。
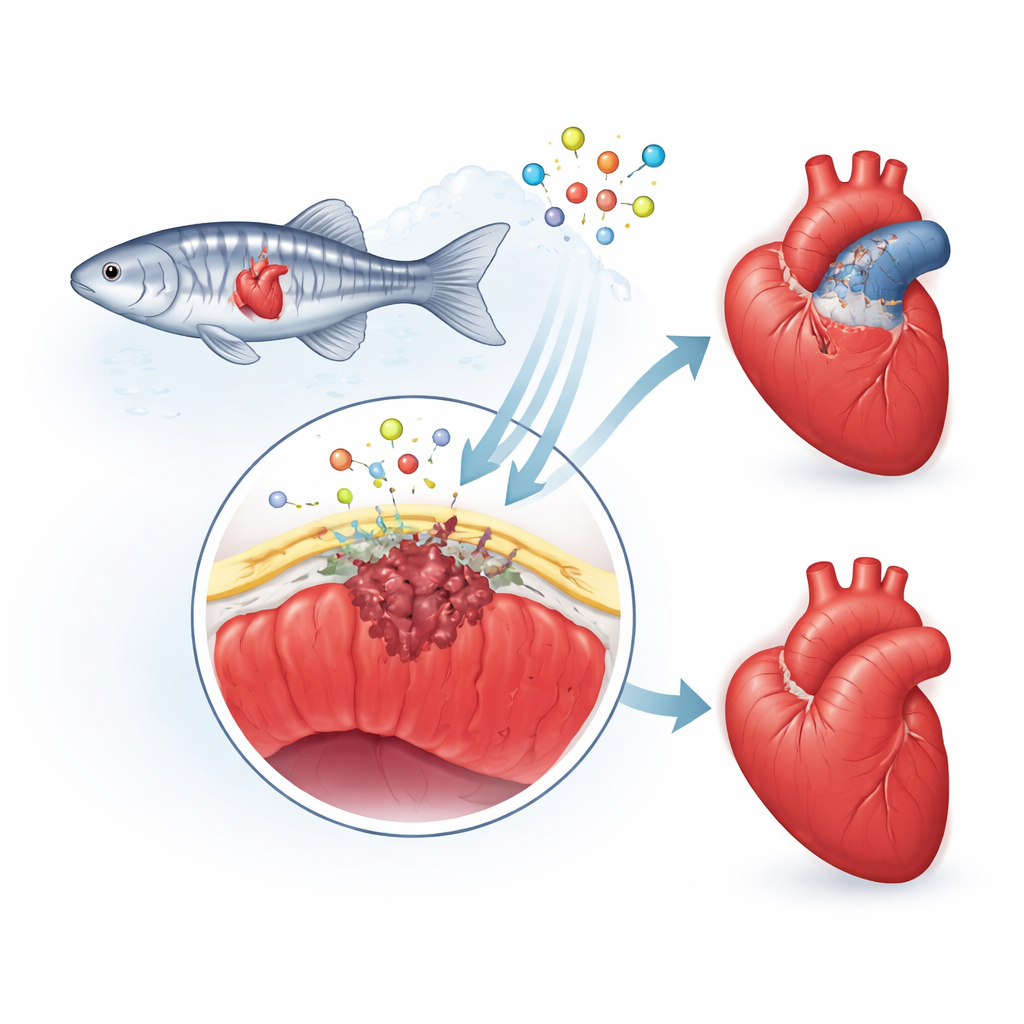
心脏的保护性外层
研究者将注意力集中在心外膜上——覆盖心脏的一层薄“皮”。受伤后,这一层被唤醒,细胞改变身份,有些细胞会进入受损区域。那里它们成为支持细胞和成瘢痕细胞,并释放化学信号,指导新血管和心肌的生长。在人类中,这种修复反应往往过度,留下厚而永久的瘢痕。然而在斑马鱼中,瘢痕是暂时的,随着健康肌肉的恢复逐步被拆解。团队怀疑一种名为纤维连结蛋白‑2(fibulin‑2,Fbln2)的蛋白——位于心脏周围的支架中——在设定心外膜反应的速度和强度方面发挥作用。
对瘢痕形成的分子调光开关
研究者在斑马鱼中使用基因编辑,制造出两类具有不同 Fbln2 水平的动物:一类是 Fbln2 降低的品系,另一类则完全缺失该蛋白。他们用冰冻探头造成心脏损伤,模拟心肌梗死,并在数周到数月内追踪愈合过程。当 Fbln2 水平降低时,早期心肌和血管内皮的细胞分裂减少,但形成的纤维性瘢痕更小且更易被重塑。到三个月时,这些心脏再生良好,且保留的胶原蛋白很少——胶原是瘢痕的主要成分。相反,完全缺失 Fbln2 的鱼表现出对一个关键生长与瘢痕通路(涉及 TGFβ 信号家族)的更强抑制,心外膜下的成瘢痕细胞明显减少。它们早期的瘢痕也较小,但后期这些心脏无法清除胶原,最终留下大而持久的瘢痕并导致再生不良。
放大观察心外膜状态变化
为了解心外膜细胞在单细胞层面的行为,团队在损伤后不久采用了单细胞 RNA 测序。他们鉴定出若干心外膜细胞“状态”,包括静默状态、刚被激活的细胞、适应低氧的应激细胞以及正在分裂的细胞。在正常 Fbln2 的鱼中,心外膜细胞从静默到激活再到成熟状态平滑过渡。而在 Fbln2 降低或缺失的鱼中,这一进程受阻:细胞滞留在早期阶段,更多成熟的激活群体代表性不足,尤其在完全缺失者中更明显。多种在心外膜激活及对 TGFβ 信号响应中通常被激活的基因表达下降,显示 Fbln2 是调节该通路的一个旋钮,决定心外膜在形成与重塑瘢痕方面的承诺强度。
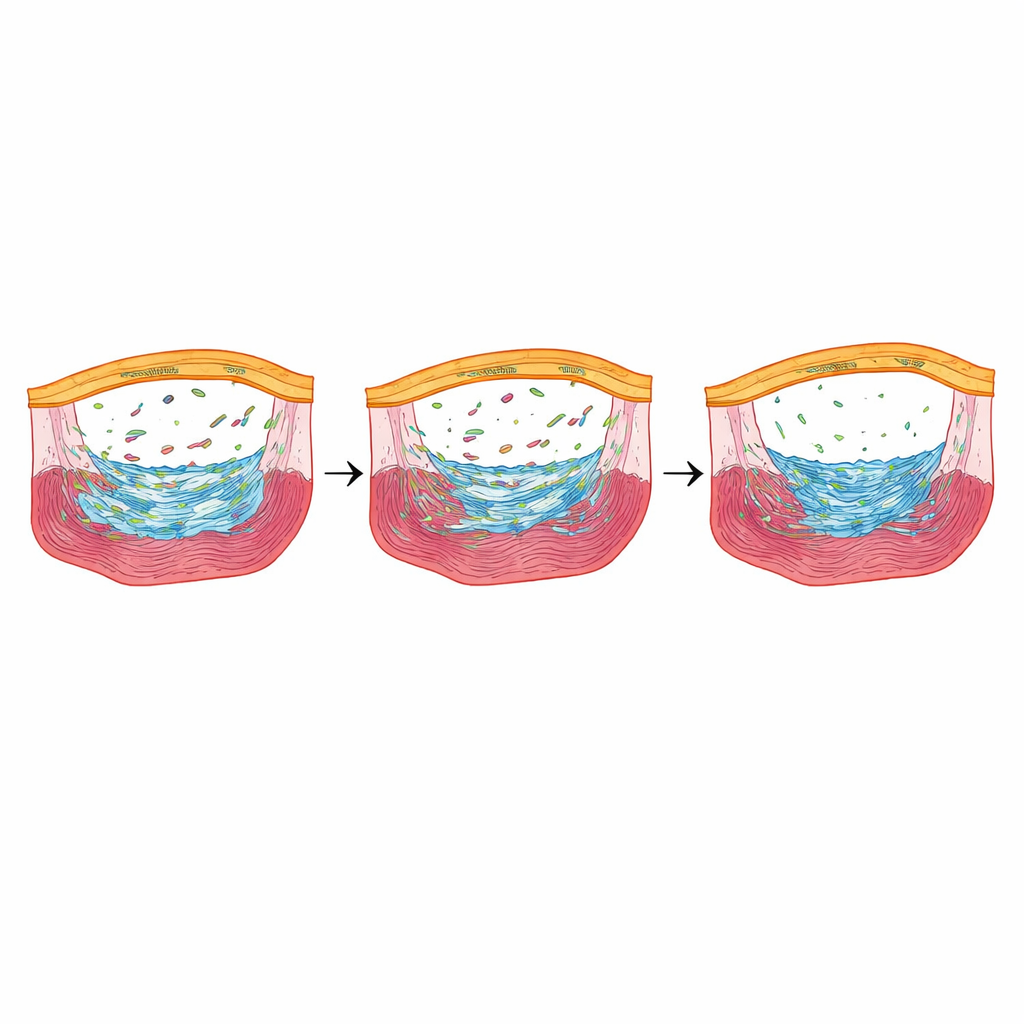
一种微调修复的应激响应因子
在 Fbln2 降低时显著下调的基因中,有一个特别突出:nupr1b,这是一种在早期愈合中于心外膜细胞内活跃的应激响应调控子。当研究者删除 nupr1b 时,斑马鱼显示出更少的心外膜成瘢痕细胞和减少的心肌细胞增殖,且在损伤数月后仍保留大量胶原沉积——这与完全缺失 Fbln2 的鱼相似。引人注目的是,当他们在 Fbln2 降低的鱼中仅在心外膜细胞里短暂强制重新表达 nupr1b 时,成瘢痕细胞数量和心肌细胞增殖恢复,且后期瘢痕增加。化学抑制 TGFβ 受体会降低 nupr1b 水平,表明 nupr1b 位于 Fbln2–TGFβ 信号轴的下游。
这对修复人类心脏意味着什么
这些发现共同揭示了一个“心外膜 Fbln2–Nupr1b 轴”,帮助斑马鱼心脏在纤维化过少与过多之间走钢丝。略微调低该轴可以抑制早期瘢痕爆发并促进高效的瘢痕清除,而完全关闭则破坏再生并留下僵硬的瘢痕。对人类医学的启示是,目标不应是全面阻断瘢痕形成,而是对其进行微调——保留足够的结构以防止破裂,同时确保瘢痕组织是暂时的并能被健康肌肉替代。理解并最终利用这一斑马鱼的控制系统,或能为未来的疗法提供思路,促使受损的人类心脏走向真正的再生而非慢性瘢痕化。
引用: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
关键词: 心脏再生, 纤维化, 斑马鱼, 心外膜, TGF-β 信号