Clear Sky Science · zh
术中活检成像评估肺癌风险
看见癌症的隐性足迹
肺癌外科医生面临高风险的难题:在手术中,他们必须迅速找到微小肿瘤及其精确边界,而现有工具有时会漏检危险部位或耗时太长。本研究提出了一种新的“观测”癌症的方式:不是直接看肿瘤细胞本身,而是观察包围它们的微观支架。作者将先进的激光成像与人工智能相结合,展示了快速且极为准确地识别肺癌及其边界的可行性。
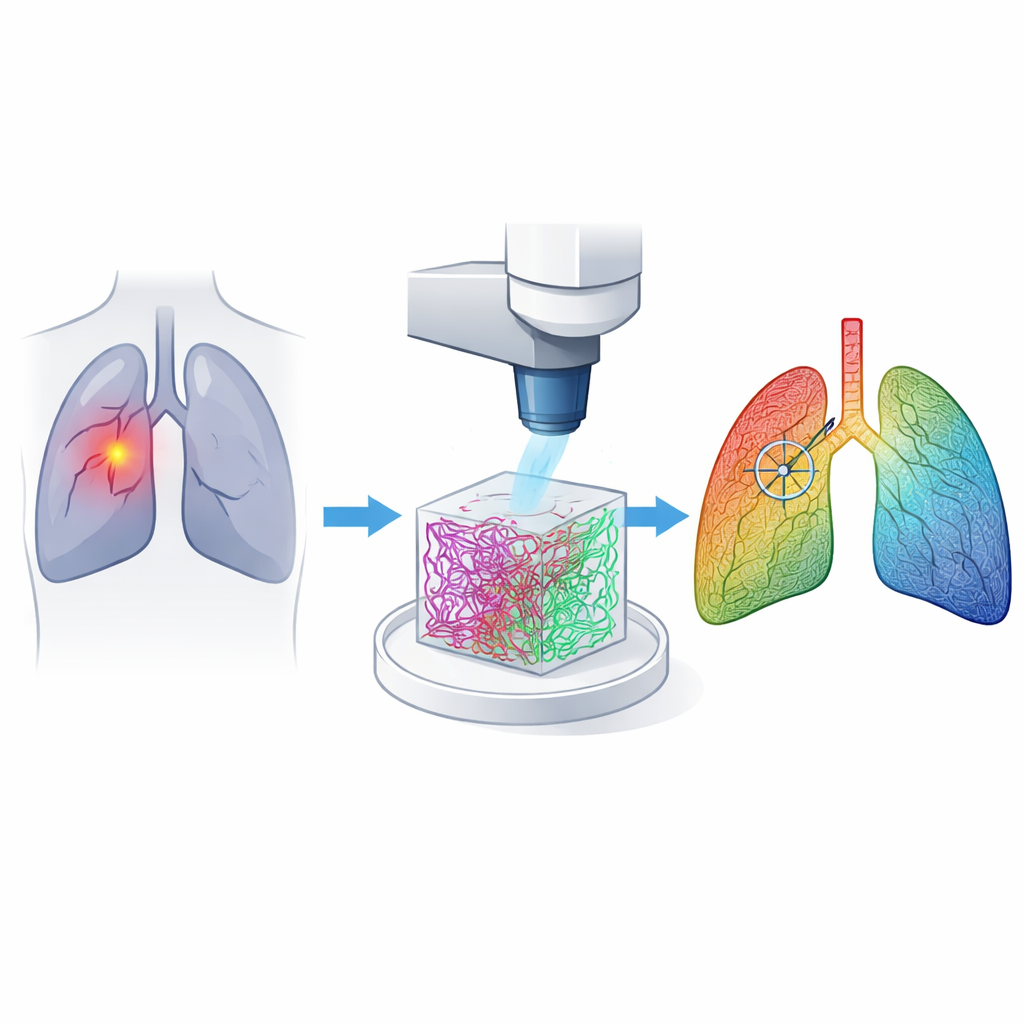
会讲故事的支撑组织
我们的肺由一种称为细胞外基质的蛋白纤维网维系。两种关键成分——胶原和弹性蛋白——赋予肺组织强度与弹性。当癌症发生时,这些纤维会被重塑:它们的排列方式、密度以及相互作用都会发生改变。研究者推断,这些微妙的结构变化可以作为癌症的可靠指纹,即使在普通手术摄像下肿瘤难以察觉时亦然。
手术室里的温和激光显微镜
研究团队构建了一台定制的多光子显微镜,这是一种可以在新鲜组织中穿透数百微米而无需染色的激光系统。通过单一近红外激光设定,它同时记录两种信号:一种突出显示胶原,另一种突出显示弹性蛋白。这种双通道成像能在每个取样点用几分钟时间获得清晰的三维肺纤维网络图像,速度足以在手术中实用。该方法在来自222例肺腺癌患者的组织上进行了测试,从肿瘤和正常区域采集了数百个小的三维图像堆栈。
教会人工智能解读纤维编码
研究者并非凭肉眼判断这些图像,而是对每个微小体素(voxel)测量若干特征:纤维的排列一致性、波动程度、填充空间的密度、弹性蛋白丝的粗细,以及相邻胶原与弹性蛋白在位置与方向上的相似性。他们引入了一个新的“相似度系数”,当胶原与弹性蛋白彼此靠近且方向一致时该系数升高。通过无监督学习,他们将数百万个体素分为重复出现的纤维“词汇”,以捕捉常见的结构模式。随后,标准的机器学习分类器学习这些词汇组合在正常与癌变组织间的差异。
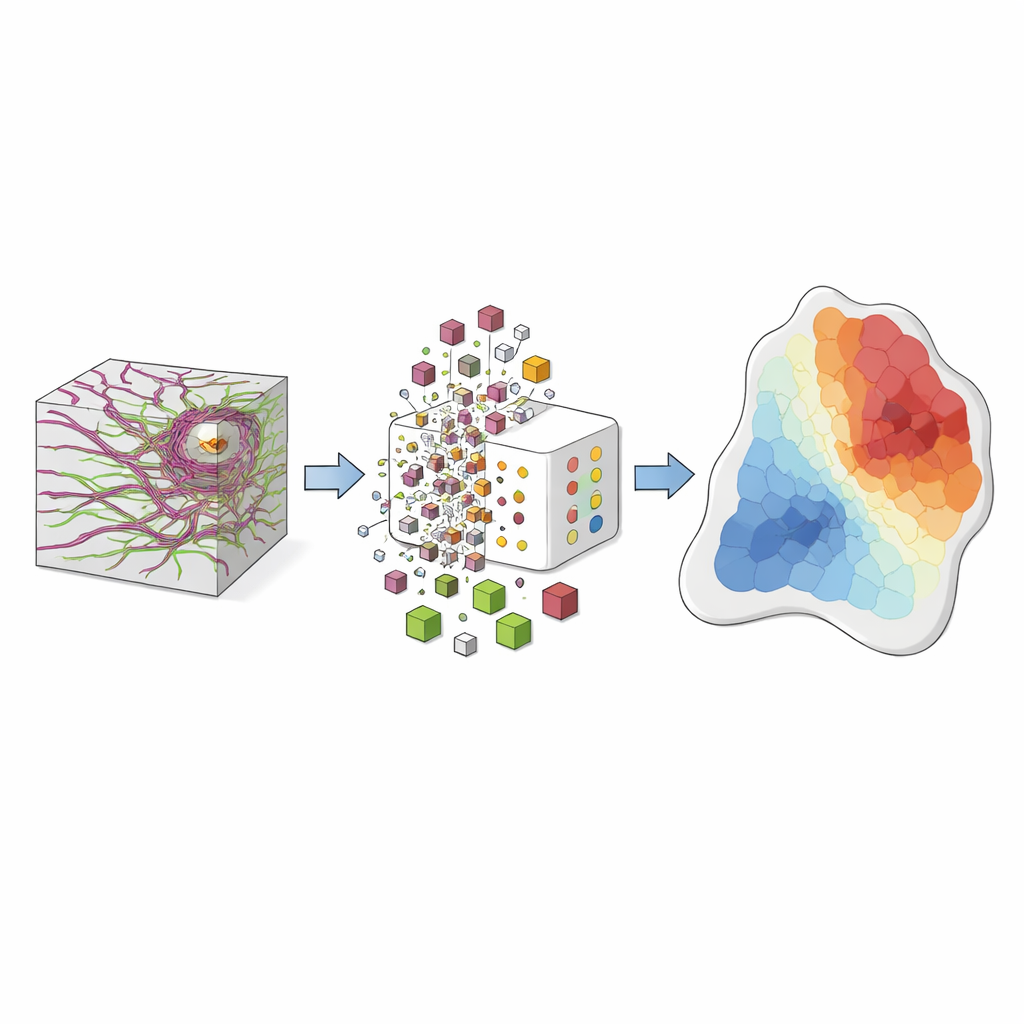
从肉眼不可见的模式到风险图
当在独立的一组肺组织样本上测试该框架时,其识别癌症的敏感性约为99%,也就是说几乎不会漏检肿瘤。研究人员进一步为每种纤维词汇创建了“癌症风险指数”,指示该词汇倾向于出现在健康组织还是病变组织。通过依据该指数为每个体素着色,他们生成了直观的风险图:肿瘤区域以暖色调显示,正常区域以冷色调显示,边界带则呈现混合色。这些风险图成功勾画出人体标本中的肿瘤—正常边界,并在活体小鼠模型成像中显示出相同的重塑趋势,表明该方法有可能转化为手术室中的实时引导工具。
这对患者可能意味着什么
未来,外科医生或可不再依赖冷冻切片病理来等待结果,而是用一根小型激光探针扫描可疑肺区,立即看到周围胶原与弹性蛋白重组所揭示的癌症高风险部位。本研究表明,肿瘤的支撑框架承载着强烈且可读的风险信号,人工智能能够将该信号转化为清晰的视觉提示。如果将该成像方法开发为临床工具,可能使活检更准确、减少二次手术,并在尽量保留健康肺组织的同时,确保切除危险组织。
引用: Qian, S., Yang, L., Meng, J. et al. Intraoperative biopsy imaging of lung cancer risk. Commun Med 6, 143 (2026). https://doi.org/10.1038/s43856-026-01406-y
关键词: 肺癌手术, 术中成像, 细胞外基质, 多光子显微镜, 人工智能诊断